您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-05-08 19:10
内容提要:当前,医疗美容类有源医疗器械在以注册为目的的型式检验阶段需要首先制定产品技术要求,产品技术要求的部分内容可参考相关行业标准或者国家标准。但为了体现医疗美容类有源医疗器械特点,切实保障产品使用过程中的有效性,需要在现有可参考标准的基础上增加专门的性能技术要求。通过对当前国家标准及行业标准的调研、分析,结合医疗美容类有源医疗器械的具体应用,对产品技术要求中体现产品特点的性能相关指标的制定提出技术建议,以期对制造商、型式检验和技术审评部门进一步完善和规范对医疗美容类有源医疗器械的安全有效性评价提供参考。同时,对后续针对医疗美容用途医疗器械的监管及标准制修订工作,进行分析和展望。
关 键 词:医疗美容 有源医疗器械 技术要求 探讨
近年来,医疗美容类产品愈发受到市场青睐,产业发展迅速,与之相伴随的是效果显著、使用方便的医疗美容类有源(见《医疗器械分类规则》[1] 中对于“有源”和“无源”的规定)医疗器械备受关注[2-6]。按照法规和相关制度要求,医疗器械在以注册为目的的型式检验阶段需要首先制定产品技术要求。对于各类新兴的医疗美容类有源医疗器械就面临了新的挑战:其在制定技术要求时,产品相关性能技术指标缺乏可参考的行业标准或国家标准。因此,就需要注册申请人自行制定相关性能部分的技术要求及对应的试验方法。如何科学合理、规范完整地制定该类产品技术要求是产业界和监管部门需要关注和解决的关键问题。
本文通过对国内外相关法规、文件和监管政策的调研与分析,结合目前的医疗器械监管工作要求,对医疗美容类有源医疗器械产品在型式检验阶段制定产品技术要求性能部分相关要求和试验方法提出建议,供产品及监管部门参考。
1.现有标准情况
当前的《医疗器械分类目录》[7] 等文件中已有一部分工作机制、使用方式及相关风险与美容用产品类似或相同的器械,如超声治疗仪、射频皮肤治疗仪和激光治疗仪等。这些产品可以主要依据现有的国家标准或行业标准制定自身产品技术要求中相关性能指标。表1 中列出了部分(并非全部)目前常见的医疗美容类有源医疗器械制定产品技术要求时可以参考的标准情况。
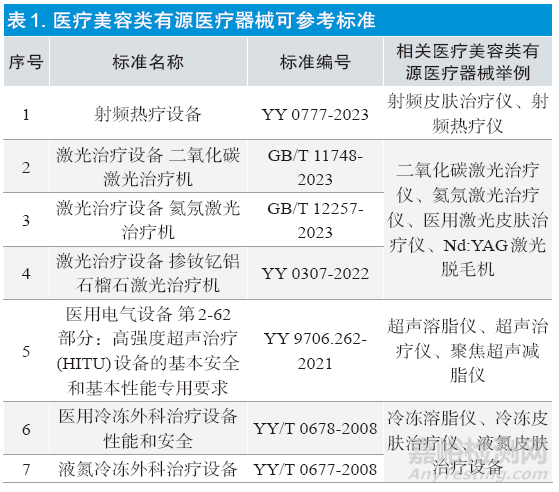
上述标准只是对常见有源美容类医疗器械的最低要求,制造商应根据适用情况在产品技术要求中作出规定。同时,制造商在产品注册受理阶段,还需要提供产品的环境验证材料。一般情况下,通常依据GB/T 14710-2009《医用电器环境要求及试验方法》进行检验。但是,按照最新的技术审查要求,相关环境验证材料需要单独提交,且不在产品技术要求中进行规范。因此,建议制造商在产品型式检验阶段一并提交环境验证申请,单独出具检验报告,与依据产品技术要求委托的检验报告一同提交注册受理。最后,也是对产品有效性进行验证的关键,即性能指标要求和试验方法应在产品技术要求中清楚写明。
2.体现产品临床特点的技术指标研究
目前的医疗器械国家标准或行业标准主要针对的是治疗传统认知疾病的医疗器械,其中的技术指标对于考量其在医疗美容方面的用途尚需完善。结合医疗美容类有源医疗器械的工作机制、结构组成和预期用途等,从以下几个方面分析能够体现产品特点的技术指标要求[8-10]。
2.1 产品外观、尺寸等
随着技术的进步和应用场景的多样化,医疗美容类有源医疗器械的使用通常需要长时间人手握持、移动等,所以该类器械的外形设计对人体工学的设计要求较高,其原理,形状、尺寸和重量等均应该符合其使用条件的要求;同时,产品外表面材料的粗糙度等也需要结合实际情况进行考量,以提高医疗器械的使用便捷性和舒适度,减轻医护人员的劳动强度为宗旨。以上要求尤其是一些预期可以家用的产品更应重视。
2.2 关键性能技术指标的确定
对于医疗美容类有源医疗器械来说,为精准实现医疗美容目的,尽量避免不必要的其他损伤是医疗美容用途医疗器械必须满足的条件。传统意义上的医疗器械以治疗疾病为最终目标,在涉及重要疾病等必要情况时可以对人体正常组织造成伤害,如消融、切割、组织变性等。医疗美容器械的要求则与之不完全相同,特别是涉及皮肤外观等情况时,应确保对于正常人体组织应尽量减少影响。这需要制造商在产品的研发过程中认真研究相关关键技术指标,以确保产品精准实现医疗美容目的,满足使用者需求。如《医用射频皮肤美容与治疗专家共识》[11] 中就指出射频美容仪器的加热机制与其工作频率的关系。另外,超声溶脂设备的输出功率/能量控制、聚焦准确度,激光美容器械的光斑尺寸等,也对医疗美容效果有至关重要的影响。器械的使用便利性要求。很多医疗美容类有源医疗器械在家庭中由使用者自行使用或者在医疗美容机构使用,其操作者较之专业的医疗人员不同,应确保该类医疗器械的使用简单易懂,包括直观、合理的操作界面,简单易懂的操作步骤等。智能化的操作系统、简明的操作按钮(或操作系统)、合理的提示(文字或语音等)都是产品技术要求中应该考虑进行规范的技术指标内容。
2.3 可靠性、效期/寿命验证要求
另外,器械的可靠性、效期/ 寿命验证也是需要关注的关键指标。尤其对于医疗美容类有源医疗器械来说,产品能够达到高可靠性、长使用寿命,是提供稳定、准确的医疗服务的关键因素。因此,在产品技术要求和相关技术研究资料中就需要报告相关可靠性验证要求、方法和结果。目前,可以参考的国家药监局发布的医疗器械稳定性监管标准包括:YY/T 1813-2022《医用电气设备使用可靠性信息收集与评估方法》、YY/T 1837-2022《医用电气设备 可靠性通用要求》、YY/T 1894-2023《医用磁共振设备可靠性验证方法》等。医疗美容类有源医疗器械可以参考上述这些标准中对于医疗器械可靠性的评价思路和指标,确定自身产品可靠性、效期/寿命等相关技术指标。
2.4 基本性能的确定
GB 9706.1-2020作为医用电气设备的通用安全标准,已经于2023 年5 月1 日正式实施,在此标准中也新提出了基本性能的概念:即与基本安全不相关的临床功能的性能,其丧失或降低到超过制造商规定的限值会导致不可接受的风险。从定义上可以看出,一款产品,其基本性能的确定,要综合考虑其临床功能及可能的风险,也就是说还是要靠风险管理来明确。因此,对于一款医疗美容类有源医疗器械,要确定其基本性能不能只考虑其临床功能,例如,超声治疗设备和射频美容设备的输出功率等。而是要通过风险管理过程,确定其基本性能要求和限值。
这里需要说明的一点就是,在实际检验过程中,部分医疗美容类有源医疗器械经过风险管理后,最终得到产品无基本性能的结论。对于此种情况,经过仔细研读相关国内外标准、查阅文献及广泛调研,在经过规范的风险管理过程实施后,得到的产品无基本性能的结论,对于检验和技术审评机构可以认可。但是,并不代表产品无基本性能就可以豁免相关检验项目(主要是电磁兼容抗扰度方面的检验项目),建议在型式检验阶段,尤其是在电磁兼容抗扰度检验项目的符合性准则方面,除了满足相关检验标准(YY 9706.102-2021及相关专用标准)符合性条款要求外,选择被测医疗美容类有源医疗器械产品技术要求中与其临床功能相关的、可量化考核的关键技术指标作为附加符合性条款,作为相关检验结果的判据。同时,上述附加符合性条款也要在产品技术要求及产品随附文件中予以明确。
2.5 设备标记和文件的规范性
美容用途有源器械应用场景多样,在非医疗监护条件(美容院、诊所或家用等)下使用时,操作者或者使用者相对欠缺安全防护意识,相关设备外部标记及说明书的规范性就显得尤为重要。这里需要注意:对于医疗美容类有源医疗器械的外部标记,相关内容应符合《医疗器械说明书和标签管理规定》《产品质量法》等法规文件要求。同时,应满足相关通用及专用标准的要求,例如:在GB 9706.1-2020标准中7.2 章节对设备外部标记进行了规范。以上只是对医疗美容类有源医疗器械产品外部标记的最低要求,如果制造商在此基础上,为了满足临床使用过程中对于特殊情况(报警、错误提示或紧急操作等)的提示和处理,在上述法规和标准要求之外,还要编制和使用附加符号,这种情况也是允许的,但在附加符号的编制需要满足标准要求。例如,在GB 9706.1-2020 标准中就明确规定了警告或者强制行为的符号编制模板,制造商应规范使用模板编制附加符号。同时,相关附加符号除了在医疗美容类有源医疗器械产品外部标记外,还应该在产品随附文件中明确记载并说明其含义。
这里还要提醒一点:部分专标中会有对设备随附文件(说明书)的补充要求,制造商应注意要在设备说明书中增加相关内容。这不仅是标准符合性的要求,也可以有效避免不良事件的发生。
3.展望与技术探讨
当前,我国在医疗美容类有源医疗器械的研发、制造及临床应用等方面已经在国际上占有重要位置,很多技术和产品已经处于世界领先地位,如激光类医疗美容设备和技术等。但在很多高端医疗美容产品领域,我国较之世界先进水平尚有一定的差距,比如射频类美容产品等。后续,可以在相关的国家或行业标准制修订中有针对性地考虑产品的医疗美容用途,以便于相关产品的注册检验及审评审批,从标准领域推动产业和技术发展,也能够为中国的相关产品标准走向国际标准,助推中国企业走向国际舞台,更好地参与国际竞争,把握技术制高点、奠定基础[12-14]。
4.小结
本文通过对医疗美容类有源医疗器械在注册检验时技术要求可参考的相关行业和国家标准的调研与分析,结合产品的具体应用,对产品技术要求中性能相关指标的制定提出技术建议,同时对后续针对医疗美容用途医疗器械的监管标准制修订工作进行了展望,以供制造商、技术检验和审评部门作为参考。

来源:中国医疗器械信息


