您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-07-23 08:42
随着2024年7月18日中国共产党第二十届中央委员会第三次全体会议审议通过《公报》的同日,国家药品监督管理局(NMPA)官方网站重磅推出了《药包材生产质量管理规范》(征求意见稿),旨在紧密衔接《药品管理法》及《药品生产监督管理办法》的最新要求,为药包材生产企业的合规操作树立标杆,并强化药品上市许可持有人(MAH)对药包材供应商的审核责任。
该规范,被业界亲切地称为“国家药监局版药包材GMP”,引发了业界的广泛关注与热烈讨论。不仅设定了药包材生产的高标准、严要求,还明确了实施细节与时间表——意见征求截止至2024年8月20日,预示着一场针对药包材行业的全面质量“大考”即将拉开帷幕。
本文梳理了药包材GMP实施的关键环节,旨在为企业提供内部质量控制与外部认证的实用指南,同时也可作为MAH在进行药包材供应商审计时的参考依据。此次规范的出台,无疑将推动药包材产业向更高质量、更严标准迈进,促进整个医药产业链的协同发展。
一、我国药包材生产和监管政策法规
药品包装用材料、容器(简称“药包材”),作为药品不可或缺的伴侣,贯穿其生产、流通至使用的全生命周期,直接关乎药品的安全性与有效性。因此,对药包材生产企业的严格审查与高效监管,成为保障药品质量的重要基石。
我国药包材的监督管理历程,是一部从无到有、日益完善的发展史,从初期的“自由放任”状态,逐步过渡到实施“生产企业许可证制度”,再到实施严格的“注册审批”制度,最终迈向当前的“关联审评审批”新纪元。这一系列的变革,彰显了国家对药包材质量安全的日益重视。然而,尽管监管体系不断完善,但药包材生产质量监管的基础仍显薄弱,加强药包材GMP管理,成为当前亟待解决的重要课题。
为此,从行业协会到省级药监部门,再到国家药品监督管理局,各级监管机构正积极行动,密集出台相关政策法规,旨在构建更加科学、规范的药包材监管体系。这些政策不仅体现了对药包材重要性的深刻认识,也标志着我国药品监管水平正迈向新的高度,为药包材行业的健康发展提供了坚实的制度保障,梳理如下:
1) 省药监局版药包材GMP:20151207广东省药包材生产质量管理指南,该指南推荐使用于广东省辖区内药包材生产企业生产质量管理全过程,本指南明确要求,所有药包材生产企业必须制定并实施符合药包材质量管理特性的质量方针与质量目标,确保企业质量管理工作的方向明确、目标具体。同时,企业需依据自身产品的独特性质,量身打造一套完善的生产质量管理体系,涵盖从原材料采购、生产加工、质量检验到成品出库的全链条管理,确保体系的有效运行与持续改进。
2) 行业协会版药包材GMP:2019年5月8日,中国医药包装协会在其官方网站上正式发布了《药包材生产质量管理指南》(标准编号:T/CNPPA 3005-2019),这一里程碑式的文件迅速在业界引起了广泛关注,并被业界人士亲切地称为“行业协会版药包材GMP”。
3) 国家药监局版药包材GMP:2022年6月2日,国家药品监督管理局在其官方网站上首次公布了《药包材生产质量管理规范》的征求意见稿,该稿共计14章72条,内容详尽,篇幅达9千多字,为药包材行业的质量管理提供了初步框架。经过近两年的深入研讨与广泛征求意见,2024年8月20日,国家药监局正式发布了修订完善后的《药包材生产质量管理规范》,新版本缩减为13章但增至76条,内容更加丰富,总字数约1.3万多字,标志着我国药包材生产质量管理迈入了一个全新的阶段。这一规范被业界广泛誉为“国家药监局版药包材GMP”,它不仅明确了其作为药包材生产企业建立质量管理体系的核心依据,还详细阐述了药包材生产管理和质量控制的基本要求。规范的核心目标在于,通过科学严谨的管理措施,最大限度地降低药包材生产过程中可能发生的污染、交叉污染、混淆和差错风险,确保每一批次的药包材都能持续稳定地符合药用要求及预定用途,为药品的安全性和有效性提供坚实的包装保障。
二、药包材GMP重点章节解析
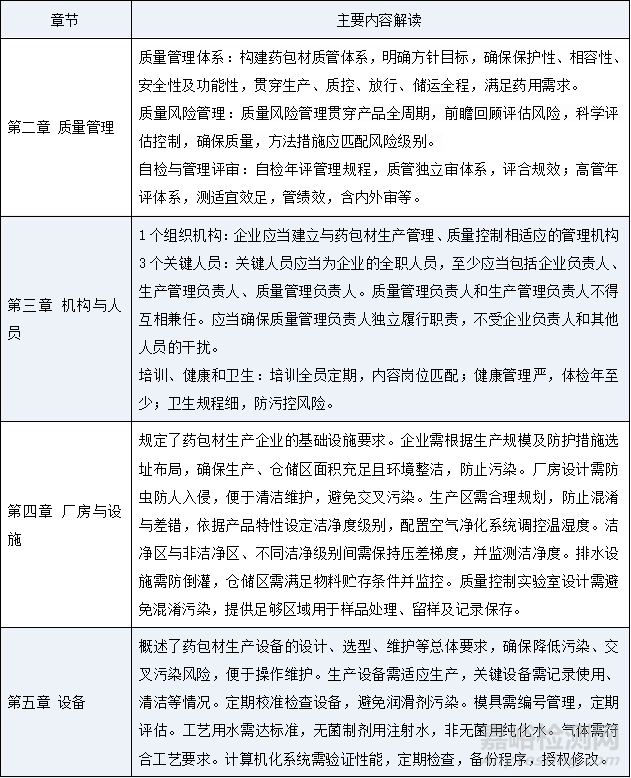
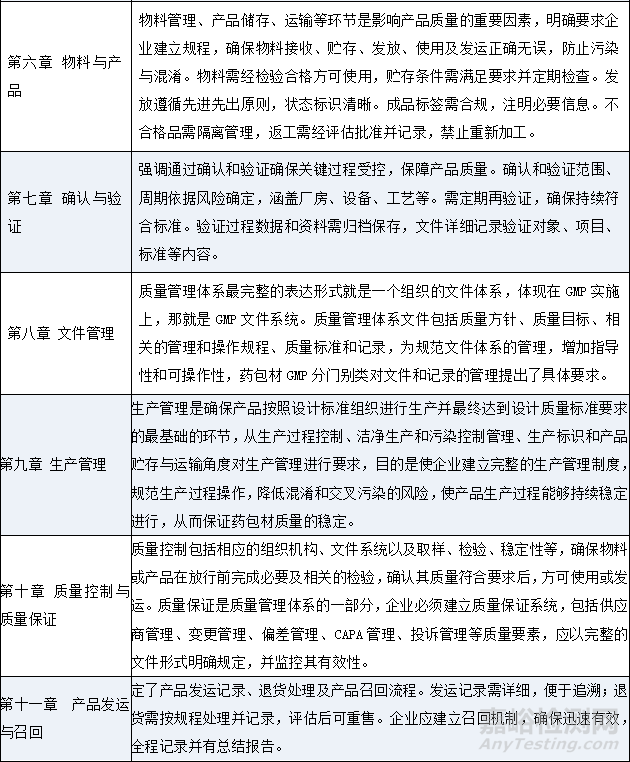
国家药监局版药包材GMP的发布与实施,是我国药品监管体系不断完善的重要体现,也是推动药包材行业高质量发展的关键举措。它将促使药包材生产企业全面提升质量管理水平,加强生产过程中的风险防控,推动技术创新与产业升级,为我国医药行业的持续健康发展注入新的活力,《药包材生产质量管理规范》(征求意见稿),共13章76条,总字数约1.3万多字,明确了药包材生产企业质量管理、机构与人员、厂房与设施、设备、物料与产品、确认与验证、文件管理、生产管理、质量控制与质量保证、产品发运与召回、合同管理等要求,主要条款内容解读详见下表:

参考文献:[1] www.nmpa.gov.cn、www.cnpharm.com

来源:药渡


