您当前的位置:检测资讯 > 行业研究
嘉峪检测网 2025-01-14 08:46
一年一度的FDA 新药批准报告,由CDER主任发布寄语。2024年FDA共批准了50个新药,接近近十年的平均水平。
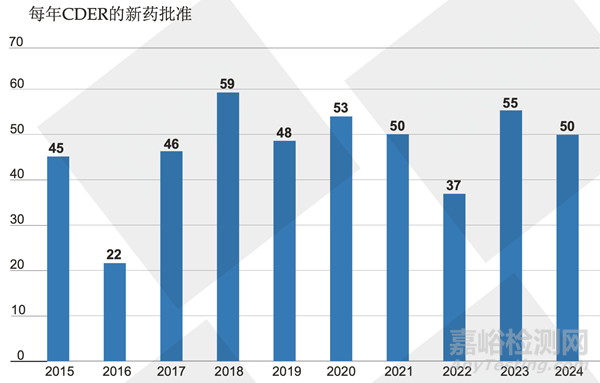
FDA以其审评严格、创新、高效为著称,50个新药中,有47个达到了PDUFA设定的目标。获批的新药中,以解决巨大未满足临床需求为目标,罕见病药达26个,同时还批准了多个用于罕见的肿瘤适应症。
以创新为已任,引领全球审评监管机构,有34个药是在美国率先批准。首创药高达24个,这些药产生的创新药理作用,药物对机体的靶标为首次用于新药上市。这些开新河的审评审批,为全球监管带来示范作用。
FDA为高效审评审批新药申请,为全球患者带来药物的使用,利用一些快速审评工具,比如孤儿药,优先审评,加速审批,突破性疗法等。
有26个药被认定为孤儿药,28个药被加优先审评,18个药拿到了突破性疗法。这些加速的审评审批工具,有力的帮助FDA识别到创新药,并助推它们快速进入市场,满足临床患者未被满足的巨大需求。
以上数字对于FDA来讲,具有很重要的现实意义。
本号将陆续更新学习与解读这些新药审评报告,选择部分有代表性的新药审评报告,将FDA在审评中发现的问题,及申请人回复和发补,总结给到大家,帮助大家了解FDA审评思路和最新关注点,让新药出海企业了解FDA的审评风格。
最后,附上2024年批准的50个新药名单。

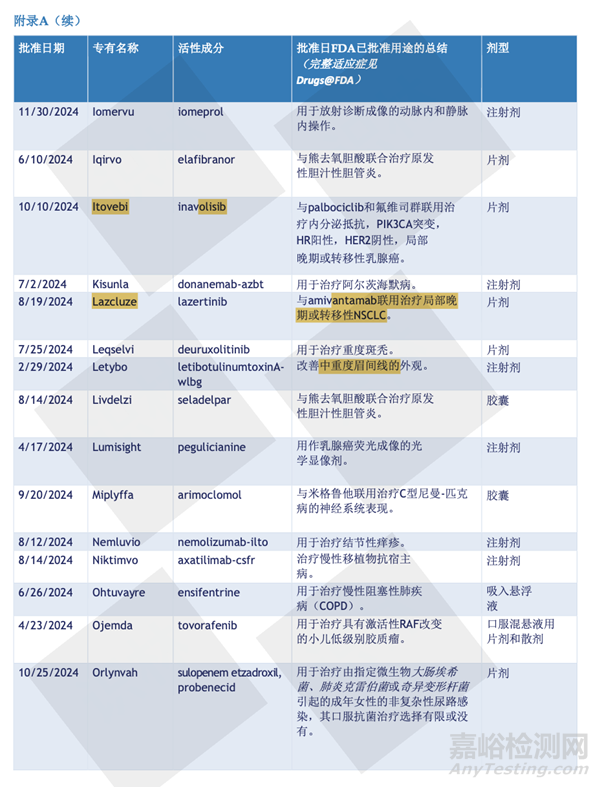
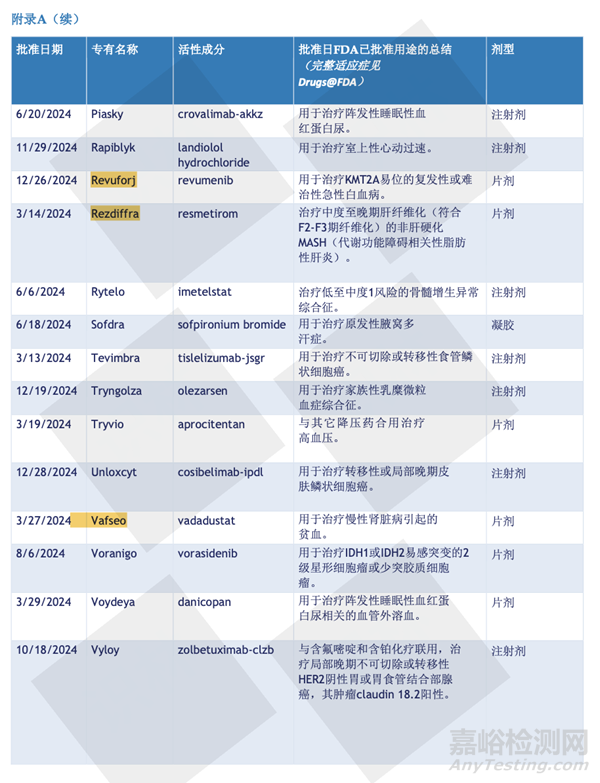
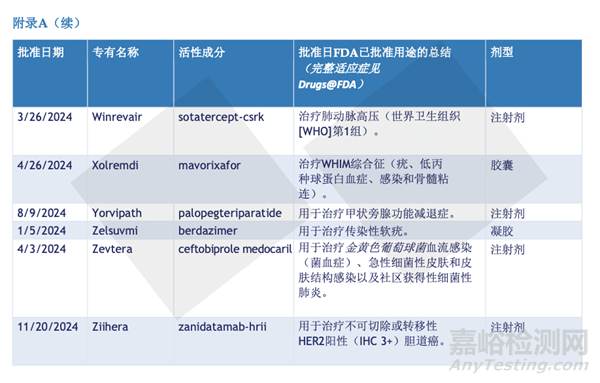
参考文献:2024年FDA新药审批总结报告,识林

来源:文亮频道


