您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-02-02 10:16
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「 本文共:16条资讯,阅读时长约:3分钟 」
今日头条
康希诺新冠疫苗Ⅲ期试验获积极结果。康希诺生物宣布其重组新冠病毒疫苗Ad5-nCoV在Ⅲ期临床中期分析中已达到主要安全性及有效性标准。该项试验由来自七个国家的全球主要研究者(global PI)、全球协同主要研究者(global co-PI) 及各国协同主要研究者(country co-PI)共同领导,已在三个大洲中的五个国家的78家临床研究中心完成对4万余受试者的接种,临床中未发生任何与疫苗相关的严重不良事件。目前该试验正在积极推进当中。
国内药讯
1.正大制药阿法骨化醇软胶囊首家通过一致性评价。正大制药(青岛)阿法骨化醇软胶囊以补充申请形式获批通过一致性评价,为国内首家。阿法骨化醇属于活性维生素D,主要用于骨质疏松症、肾性骨病、甲状旁腺机能亢进等适应症。2018年中国公立医疗机构终端阿法骨化醇胶囊剂销售额超过8亿元。该品种目前拥有生产批件的厂家有贝克诺顿制药、信谊延安药业、梯瓦制药和利奥等。
2.甘李药业CDK 4/6抑制剂获FDA快速通道资格。FDA授予甘李药业靶向抗癌药GLR2007快速通道资格,用于治疗胶质母细胞瘤患者。GLR2007是一款CDK 4/6抑制剂,拟用于治疗包括胶质母细胞瘤在内的晚期实体瘤。胶质母细胞瘤是一种侵袭性形式的脑癌,存活率很低,它是最常见的脑和中枢神经系统(CNS)恶性肿瘤,占恶性原发性脑和中枢神经系统肿瘤的45.2%。
3.呼吸道合胞病毒预防单抗nirsevimab获纳入突破性疗法认定。赛诺菲/阿斯利康长效单抗药物nirsevimab获CDE纳入突破性疗法认定程序。Nirsevimab采用被动免疫机制,来预防呼吸道合胞病毒感染性疾病的发生,适用于所有第一次经历呼吸道合胞病毒流行季的婴幼儿,以及第一次和第二次经历呼吸道合胞病毒流行季的慢性肺部疾病儿童或先天性心脏病儿童。nirsevimab有望成为中国首个获批上市的呼吸道合胞病毒预防用药物。
4.思路迪医药首个自主研发新药获批临床。思路迪医药自主研发的1类创新药3D011获国家药监局临床试验默示许可,拟开发适应症为晚期实体瘤。3D011是该公司首个自主研发的创新药,已在临床前研究中显示出能够显著地抑制肿瘤生长;并且对hERG通道没有抑制作用;小鼠和犬毒理学研究中,未见明显药物相关毒性反应。
5.百奥赛图联手LiberoThera开发GPCR抗体药物。百奥赛图与LiberoThera达成战略合作,双方将基于百奥赛图RenMab®抗体发现平台及LiberoThera的抗原制备技术,联合开发治疗型全人GPCR抗体药物。根据协议,第一阶段的合作双方将共同开展针对GPCR靶点的抗肿瘤抗体发现直到完成体内药效评价,确定先导抗体分子。LiberoThera负责抗原制备并参与抗体体外筛选,百奥赛图则将利用其RenMab®小鼠平台开展GPCR抗体发现并通过动物体内药效评价技术完成先导抗体候选分子的筛选。
国际药讯
1.诺华多发性硬化症新药Kesimpta欧盟即将获批。欧洲药品管理局(EMA)人用医药产品委员会(CHMP)推荐批准诺华新型靶向B细胞疗法Kesimpta(ofatumumab),用于治疗存在由临床或影像学特征定义的活动性疾病的复发型多发性硬化症(RMS)成人患者。值得一提的是,Kesimpta已于2020年8月获FDA批准上市,是首个也是唯一一个可以在家轻松给药和管理的B细胞疗法,采用Sensoready自动注射笔给药每月一次皮下注射。
2.Keytruda一线治疗转移性NSCLC头对头Ⅲ期数据公布。默沙东在WCLC 2020年会上公布PD-1疗法Keytruda一线治疗转移性非小细胞肺癌(NSCLC)Ⅲ期KEYNOTE-598研究的首次数据。与Keytruda单药治疗相比,Yervoy与Keytruda联用并不能提高这些患者的总生存期(OS)或无进展生存期(PFS),但增加了毒性。两组的中位OS分别为21.4个月和21.9个月(HR=1.08[95%CI,0.85-1.37];p=0.74),中位无进展生存期分别为8.2个月和8.4个月(HR=1.06[95%CI,0.86-1.30];p=0.72)。根据独立数据监测委员会(DMC)的建议,该研究已于2020年11月中止。
3.Tagrisso辅助治疗早期EGFR突变肺癌结果积极。阿斯利康在WCLC2020会议上公布第三代EGFR-TKI抑制剂Tagrisso(泰瑞沙,奥希替尼)治疗EGFRm突变非小细胞肺癌的Ⅲ期ADAURA研究一项探索性分析的结果。数据显示,Tagrisso辅助治疗使既往接受过辅助化疗的患者的疾病复发或死亡风险降低了84%、使既往未接受过辅助化疗的患者的疾病复发或死亡风险降低了77%。在疾病的各个阶段,无病生存期(DFS)的益处是相似的。
4.安进SotorasibⅡ期非小细胞肺癌临床试验成功。安进在WCLC2020年会上公布其KRAS G12C抑制剂Sotorasib治疗KRAS G12C突变的晚期非小细胞肺癌(NSCLC)患者的Ⅱ期临床CodeBreaK 100积极结果。数据显示,Sotorasib患者组的客观应答率为37.1%,疾病控制率达到了80.6%,中位应答持续时间为10个月。Sotorasib也是首个证明实现无进展生存的KRASG12C抑制剂(中位数时间为6.8个月)。临床中大多数与治疗相关的不良事件为轻中度,并没有发生与治疗有关的死亡案例。
5.GLP-1类似物PF1801获FDA孤儿药资格。FDA授予ImmunoForge公司候选药物PF1801孤儿药资格,用于治疗杜氏肌营养不良(DMD)。PF1801是重组胰高血糖素样肽-1(GLP-1)类似物,可结合并激动GLP-1受体。除DMD外,其在研疾病领域还涵盖多发性肌炎、老年肌肉衰减症和包涵体肌炎。ImmunoForge公司计划在2021年下半年启动该疗法治疗DMD的Ⅱ期临床试验。
6.Vertex胰岛细胞疗法在美获批临床。Vertex制药异基因人干细胞衍生胰岛细胞疗法VX-880(STx-02)的新药临床试验申请(IND)获FDA批准,该公司预计在2021年上半年开展一项Ⅰ/Ⅱ期临床,评估不同剂量VX-880用于治疗伴有低血糖意识受损和严重低血糖的1型糖尿病(T1D)患者的安全性和有效性。VX-880旨在通过恢复胰岛细胞功能(包括胰岛素的产生)来恢复机体调节血糖水平的能力。
医药热点
1.莫德纳对美国以外地区减量交付新冠疫苗。莫德纳公司29日证实,由于产能调整,该公司向美国以外地区交付的新冠疫苗暂时减量。意大利政府官员对莫德纳减量交付疫苗表达强烈不满。据路透社报道,莫德纳向欧盟地区供应疫苗需经“漫长复杂”流程,在瑞士生产,到西班牙封装,然后由比利时一处物流中心运往欧盟各国。由于产能问题,辉瑞、阿斯利康本月也先后通知欧盟,将减量交付新冠疫苗。
2.甘肃:村医可纳入编制管理。近日,甘肃省政府办公厅印发《甘肃省乡村医生管理办法(试行)》,对乡村医生执业准入、执业管理、培训考核、保障待遇等内容进行明确。《办法》提出,鼓励有条件的地区,将在村卫生室(所)连续执业10年以上、年龄45周岁以下、取得执业医师资格且群众反映好的乡村医生,通过事业单位公开招聘形式选拔录用,纳入编制管理。
3.通化方舱康复医院开舱。位于通化市全民健身中心篮球馆内的通化市方舱康复医院于1月30日正式开舱,拟陆续接收两次核酸检测阴性、临床治愈出院的新冠肺炎患者,在这里接受14天的巩固康复治疗。目前计划进驻方舱康复医院的100多名通化当地医务人员已全部部署到位,安保人员、保洁人员等所有进舱工作人员已接受了多轮培训。专业医护团队将制订中西医结合康复治疗方案,帮助治愈患者尽快恢复健康的身心状态。
4.四川长期护理险试点扩容。四川省医保局、财政厅、税务局联合发出《关于省本级基本医疗保险参保人员参加成都市长期护理保险制度试点的通知》,就参保对象、缴费标准等进行了明确。成都市是国家首批长期护理保险制度试点城市。在不新增全省试点城市情况下,这次将省本级基本医疗保险参保人员统一纳入成都市长期护理保险制度试点范围。
股市资讯
【九强生物】获3项专利证书,涉及(1)大肠杆菌β半乳糖苷酶受体的用途;(2)S-腺苷甲硫氨酸合成酶制剂、及其制备方法和用途;(3)苯巴比妥衍生物及其在免疫检测中的用途。
【上海医药】产品别嘌醇片通过仿制药一致性评价,主要适用于原发性或继发性痛风(急性发作,痛风石,关节破坏,尿酸结石和/或肾病)。
【正海生物】医疗器械注册证变更,产品“生物膜”名称变更为“可吸收硬脑(脊)膜补片”。
审评动向
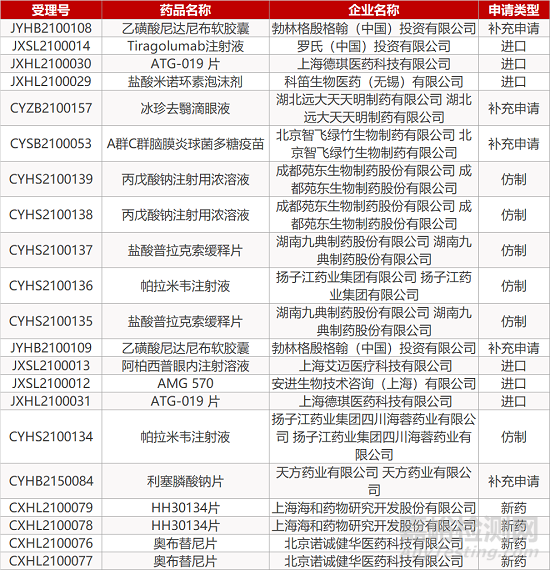
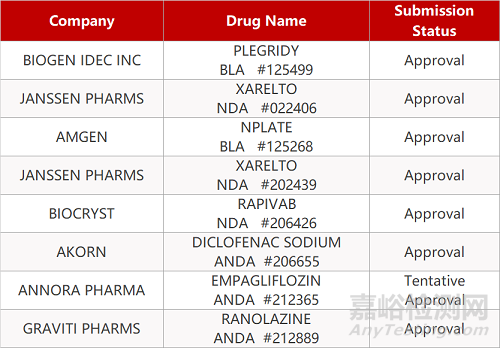
- The End -

来源:药研发


