您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-03-29 11:35
今日头条
Inovio首个DNA HPV疫苗启动国内III期临床。东方略合作品种VGX-3100项目通过遗传办审批,正式在国内开展VGX-3100与器械CELLECTRATM 5PSP 联合治疗HPV-16/18相关宫颈高度鳞状上皮内病变(HSIL)的III期临床。VGX-3100是Inovio开发的一款DNA免疫疗法,是全球首个开发用于HPV相关癌前病变的治疗性疫苗,目前正在开展两项国际关键性III期临床(REVEAL 1和REVEAL 2)。今年3月1日,Inovio宣布REVEAL 1研究达到主要和次要临床终点,据悉该研究是首个达到临床终点的DNA疗法。
国内药讯
1.恒瑞PD-1再提交两项上市申请。恒瑞医药注射用卡瑞利珠单抗两项新适应症上市申请获CDE受理,初步推测这两项适应症为:晚期食管癌一线治疗及晚期或转移性鳞状非小细胞肺癌一线治疗。卡瑞利珠单抗是该公司自主研发的一款PD-1单抗,于2019年5月在中国获批上市,目前已获批经典型霍奇金淋巴瘤、肝细胞癌、非鳞状非小细胞肺癌和食管鳞癌4项适应症。而且4项适应症已全部纳入最新版国家医保目录。
2.绿叶抗抑郁新药LY03005达III期临床终点。绿叶制药自主研发的1类新药盐酸安舒法辛缓释片(LY03005)治疗抑郁症的中国III期临床达主要终点。LY03005是一种5—羟色胺—去甲肾上腺素—多巴胺三重再摄取抑制剂(SNDRI)。与安慰剂组相比,LY03005 80mg组和160mg组8周末的MADRS总分较基线的变化值具有统计学上的显著差异(P<0.0001);其HAM-D17、CGI、HAM-A等评分较基线的变化值也具有统计学意义(P<0.0001或P<0.05);LY03005总体耐受性、安全性良好。
3.维眸生物VVN001滴眼液国内获批临床。维眸生物1类新药VVN001滴眼液获国家药监局2项临床试验默示许可,拟临床开发用于治疗干眼的症状和体征。VVN001是维眸生物自主研发的一款LFA1抑制剂,是该公司一系列眼科创新药管线中首个进入临床阶段的项目。在美国,维眸生物已于去年9月向FDA提交该新药的Ⅱ期临床申请。本次为该药首次在中国获批临床。
4.亚盛MDM2-p53抑制剂临床前研究发表。亚盛医药1类新药MDM2-p53抑制剂APG-115的临床前研究成果发表在国际期刊《自然免疫学》上。基于体内和其它实验模型,该研究证实T细胞MDM2缺陷小鼠生长速度更快,其肿瘤浸润CD8+T细胞数量呈减少趋势。同时,该研究还发现MDM2可维持信号转导子和转录激活因子5(STAT5)稳定性,后者蛋白对调节T细胞功能和存活至关重要。APG-115是首个在中国进入临床阶段的MDM2-p53抑制剂,已在中美展开多项治疗实体瘤及血液肿瘤的Ⅰb /Ⅱ期临床。
5.艾力斯医药肺癌靶向药艾弗沙启动患者援助项目。艾力斯医药1类肺癌治疗新药艾弗沙(甲磺酸伏美替尼)日前在全国30个省市自治区启动了患者慈善援助项目。该项目由北京康盟慈善基金会发起,为经指定医疗机构评估确认为适合艾弗沙治疗的非小细胞肺癌(NSCLC)患者提供药物援助。艾弗沙是第三代EGFR-TKI,已于今年3月获NMPA批准,用于治疗经检测确认存在EGFR T790M突变阳性的局部晚期或转移性NSCLC成人患者。
6.科伦博泰在研RET抑制剂海外授权。科伦控股子公司科伦博泰(Kelun-Biotech)宣布与Ellipses Pharma公司达成授权合作,将其小分子肿瘤靶向RET激酶抑制剂(A400项目)在欧美等区域的权益独家授权给后者。临床前研究表明,A400项目具有良好体内外激酶抑制活性和选择性;且对临床已报道的多种临床耐药突变有效,具有克服耐药突变和提高对脑转移癌临床疗效的潜力。该新药目前已在国内提交了新药临床试验申请。
国际药讯
1.FDA批准首款靶向BCMA的CAR-T疗法。FDA批准百时美施贵宝(BMS)和bluebird bio公司联合开发的靶向BCMA的CAR-T细胞免疫疗法Abecma(idecabtagene vicleucel)上市,用于治疗已接受过四种以上前期疗法的复发/难治性多发性骨髓瘤成年患者。在一项关键性Ⅱ期临床KarMMa中,Abecma在这类患者中的总缓解率为72%(95% CI:62%-81%),并且28%的患者达完全缓解(sCR; 95% CI:19%-38%)。Abecma也是FDA批准的首个靶向BCMA的CAR-T细胞疗法。
2.辉瑞启动用于儿童的新冠疫苗临床试验。辉瑞/BioNTech的mRNA新冠疫苗BNT162b2日前针对12岁以下儿童展开I / II期临床。该项研究拟招募144名儿童以三种不同的剂量(10、20和30微克)初步测试接种两剂疫苗的安全性;下一阶段将扩大到4,500名志愿者参与后期试验,进一步评估所选剂量水平的安全性和有效性。据悉,针对12岁至15岁未成年人的III期临床目前正在进行当中,有关这一年龄组的疫苗安全与有效性数据不久将发布。
3.奥拉帕利治疗卵巢癌Ⅲ期临床最终分析结果发布。阿斯利康/默沙东PARP抑制剂奥拉帕利(olaparib)用于BRCA1/2突变铂敏感型复发性卵巢癌维持治疗的Ⅲ期临床(SOLO2/ENGOT-Ov21)最终分析结果发表于《柳叶刀-肿瘤学》上。与安慰剂组相比,奥拉帕利为患者带来了显著的OS改善,奥拉帕利组中位OS为51.7个月,安慰剂组为38.8个月。奥拉帕利组死亡风险降低26%(HR=0.74)。
4.LAG-3抗体首次达到Ⅲ期临床主要终点。百时美施贵宝抗LAG-3抗体relatlimab与抗PD-1抗体Opdivo联用,在治疗转移性或不可切除的黑色素瘤初治患者的Ⅱ/Ⅲ期临床RELATIVITY-047试验中获积极结果。与Opdivo单药相比,relatlimab达到无进展生存期的主要终点。BMS计划在医学会议上公布结果并将结果递交给监管机构。LAG-3是一种表达在效应T细胞和调节性T细胞(Tregs)表面的免疫检查点蛋白。据悉,这是首个报告抗LAG-3抗体疗效的Ⅲ期临床试验。
5.辉瑞口服激素疗法治疗子宫肌瘤获Ⅲ期长效数据。辉瑞/Myovant口服GnRH拮抗剂relugolix与雌二醇和醋酸炔诺酮的联合疗法,在治疗女性子宫肌瘤的III期临床LIBERTY中获两年治疗数据。数据显示,relugolix组合使患者在长达两年的时间内症状显著缓解。目前relugolix联合疗法用于该适应症的上市申请正在接受FDA的审查;2020年12月,relugolix单药片剂已获FDA批准,成为了治疗成人晚期前列腺癌的首款口服激素疗法。
6.神经疾病药物公司拟加速推进两款临床期疗法。Eliem Therapeutics宣布已获得8000万美元的融资。这些资金将用于加速该公司两款候选疗法的临床开发。ETX-810是一款潜在“first-in-class”非阿片类口服前药(prodrug),在体内分解后可以提高棕榈酰乙醇酰胺(PEA)水平,用于治理慢性疼痛。ETX-155是一款新一代口服GABAA受体正向别构调节剂,可以增强GABA介导的抑制性信号,降低神经元的兴奋水平,拟用于治疗癫痫、抑郁症以及激素相关情绪障碍。
医药热点
1.省部共建中医湿证重点实验室。我国首个中医类省部共建国家重点实验室日前落户广州市。该实验室由广东省和科技部共建,将围绕中医湿证与主要慢性病防治过程中的科学问题、关键技术,开展系统、规范、深入的全链条研究。实验室依托建设单位为广州中医药大学。陈可冀院士受聘担任省部共建中医湿证国家重点实验室、广东省中医药科学院学术委员会主任。
2.北京首家互联网医院正式获批。北京协和医院互联网医院日前通过北京市卫健委审核,成为北京市首家获批的互联网医院。医院可为部分常见病、慢性病患者提供复诊服务,目前开通了心内科、内分泌科、皮肤科等19个科室,支持在院病例调阅、在线问诊,检查检验、处方开具等功能,北京市医保患者可在线进行互联网复诊费的脱卡直接支付。
3.甘肃加强卫生人才队伍建设。甘肃省卫健委日前印发《关于扎实推进“三个一批”人才计划 持续加强卫生健康人才队伍建设的通知》,明确今年年底前,省级各医疗卫生机构要完成高层次人才和急需紧缺人才引进任务。全省各县级医院完成5名~10名临床医学相关专业本科以上学历人才引进任务。各乡镇卫生院(社区卫生服务中心)完成2名~3名临床医学相关专业大专以上学历人才引进任务。
4.康希诺新冠疫苗继续在欧盟扩大市场。3月26日,继在匈牙利获得紧急使用授权后,康希诺生物与军事科学院陈薇院士团队合作研发的新冠疫苗有望继续在欧盟扩大市场。据彭博社26日援报道,3个欧盟国家已与该公司国际业务部接触,商讨可能的疫苗采购方案。康希诺生物同日也证实了这一消息。
审评动向
1. CDE新药受理情况(03月28日)
申请临床:
千红生化的ZHB111注射液、石药集团的注射用西罗莫司(白蛋白结合型)、派格生物的聚乙二醇化艾塞那肽注射液、轩竹生物的XZP-5955 片、青山利康的磷酸盐血滤置换液和磷酸盐血滤置换液(无钙)、百济神州的Ociperlimab注射液、轩竹生物的XZP-5955 片(2个规格)、勤浩医药的GH35片(2个规格)。
申请生产:
安若维他的盐酸帕罗西汀片(4个规格)、瑞迪博士(北京)药业的盐酸厄洛替尼片(2个规格)、奥鸿药业的注射用唑来膦酸浓溶液、盛迪亚生物的注射用卡瑞利珠单抗(2个规格)。
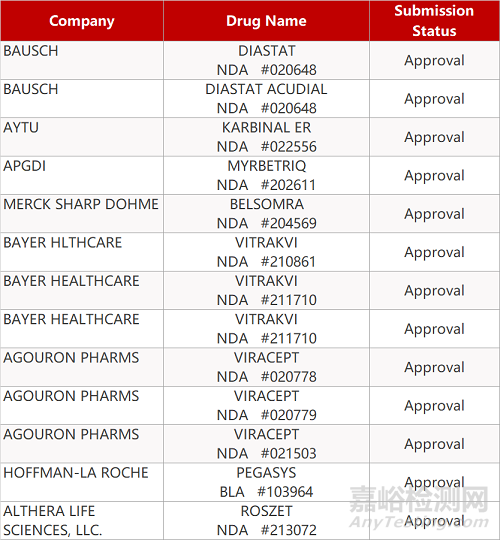
2. FDA新药获批情况(北美03月25日)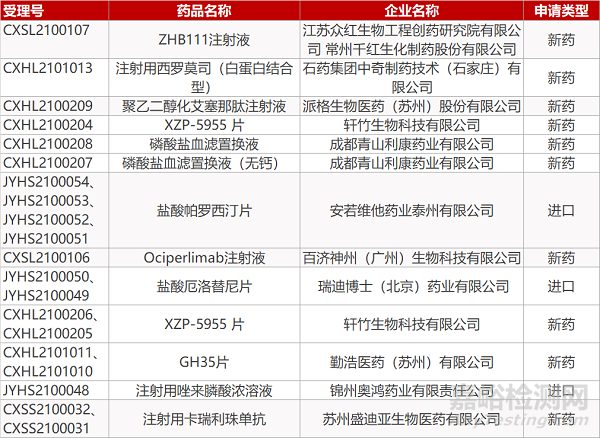
股市资讯
【恒瑞医药】近日公司子公司苏州盛迪亚收到国家药监局核准签发的关于贝伐珠单抗注射液及SHR-1701注射液的药物临床试验批准通知书。贝伐珠单抗适应症包括转移性结直肠癌、非小细胞肺癌、恶性胶质瘤、转移性肾细胞癌、转移性宫颈癌、腹膜癌、肝细胞癌等,国内目前有齐鲁制药和信达生物2个贝伐珠单抗注射液获批上市;SHR-1701可以促进效应性T细胞的活化,同时还可有效改善肿瘤微环境中的免疫调节作用,国内外尚无同类靶点产品获批上市,亦无相关销售数据。
【中国医药】(1)近日,公司子公司天方有限收到国家药监局批准通知书,药品那格列奈片通过仿制药质量和疗效一致性评价,该产品片可单独用于经饮食和运动不能有效控制高血糖的2型糖尿病病人,也可用于使用二甲双胍不能有效控制高血糖的2型糖尿病病人的联合应用。(2)公司拟聘任陈静担任公司副总经理职务。
【复星医药】近日,公司控股子公司复宏汉霖与润新生物签订《约束性条款书》,润新生物授予复宏汉霖就靶向人类BRAF蛋白V600E 突变的小分子抑制剂RX208进行研发、生产及商业化并使用相关知识产权的独家权利许可。

来源:药研发


