您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-12-10 11:25
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.艾力斯第三代EGFR-TKI拟纳入优先审评。艾力斯医药第三代EGFR-TKI甲磺酸伏美替尼片新适应症上市申请获CDE拟纳入优先审评,一线治疗具有表皮生长因子受体(EGFR)外显子19缺失或外显子21(L858R)置换突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。值得一提的是,该新药用于上述适应症已在11月被国家药监局纳入突破性治疗品种目录。
2.君实启动两款新药临床试验。君实生物IL21/HSA融合蛋白JS014登记启动一项Ⅰ期临床,评估单药及联合特瑞普利单抗在晚期肿瘤患者中的安全性、耐受性、药代动力学和初步疗效。该项研究由中国人民解放军陆军军医大学第二附属医院朱波医学博士担任主要研究者。同日,该公司还登记启动了另一个新药JS103的Ⅰ期临床,这是一款聚乙二醇化尿酸酶衍生物,拟用于高尿酸血症伴有痛风患者的治疗。
3.和黄医药抗肿瘤EZH2抑制剂报IND。和黄医药与Epizyme公司联合开发的抗肿瘤新药tazemetostat hydrobromide(tazemetostat)片的临床试验申请获CDE受理。tazemetostat是Epizyme开发的一款“first-in-class” EZH2甲基转移酶抑制剂,已在美国获批上市,用于治疗上皮样肉瘤和复发/难治性滤泡性淋巴瘤。tazemetostat还正在开发用于治疗弥漫性大B细胞淋巴瘤、前列腺癌和卵巢癌。和黄医药拥有这款新药在大中华区的开发和商业化权利。
4.百济神州TYK2抑制剂国内报IND。百济神州TYK2变构抑制剂BGB-23339的临床试验申请获CDE受理。BGB-23339是百济神州首款自主研发的炎症免疫类候选药物,正在澳大利亚开展Ⅰ期临床。在临床前研究中,BGB-23339展现出高度选择性,能强效抑制在免疫诱导中起关键作用的促炎细胞因子白细胞介素(IL)-12、IL-23和1型干扰素(IFN)。目前国内外尚无同靶点药物获批上市。
5.生物技术公司Avistone获战略投资。Avistone Pharmaceuticals宣布完成2亿美元的战略投资。本轮融资将支持Avistone与Pearl Biotechnology公司的合并,开发一个整合式的靶向肿瘤学疗法研发平台,以及推进Avistone现有候选药物的加速开发。Avistone总部位于中国北京,研发管线进展最快的是一款c-Met抑制剂,拟用于具有特定遗传特征的非小细胞肺癌和胶质母细胞瘤患者,该产品目前已被NMPA纳入突破性治疗品种。
国际药讯
1.阿斯利康长效新冠鸡尾酒EUA获批。FDA批准阿斯利康(AstraZeneca)长效抗体组合疗法Evusheld(tixagevimab+cilgavimab)的紧急使用授权申请,用于SARS-CoV-2暴露前的预防。这是获FDA批准的首个用于COVID-19暴露前预防的抗体疗法。在一项用于有症状COVID-19的暴露前预防的III期临床PROVENT中,6个月随访数据显示,一次性肌肉注射AZD7442使症状性COVID-19风险降低83%,且耐受性良好。
2.植物源性新冠疫苗Ⅲ期临床积极。葛兰素史克与Medicago联合开发的佐剂植物源性COVID-19疫苗在全球Ⅲ期临床中获积极结果。这款疫苗对SARS-COV-2所有变异株的总体疫苗效力达到71%(95% CI:58.7,80.0;符合方案分析:PP)。在未发生新冠肺炎暴露的、初始血清阴性状态的人群中,相应的效力为75.6%(95% CI:64.2-83.7;PP)。针对Delta和Gamma的防护效力分别为75.3%(95% CI:52.8,87.9;PP)和88.6%(95% CI:74.6,95.6;PP)。研究期间,奥密克戎尚未流行。
3.TROP2-ADC公布乳腺癌队列最新数据。第一三共和阿斯利康公布TROP2-ADC药物datopotamab deruxtecan(Dato-DXd)在Ⅰ期实体瘤试验(TROPION-PanTumor01)中治疗三阴乳腺癌(TNBC)的最新数据。亚组分析显示,在27例可评估、且既往未接受过ADC治疗的TNBC患者中,中位随访8.8个月时Dato-DXd治疗组ORR为52%(14/27),DCR为81%。Dato-DXd的总体安全性与既往报道一致。详细数据公布在SABCS21年会上。两家公司计划启动注册Ⅲ期临床研究。
4.诺华CDK4/6抑制剂治疗乳腺癌新数据积极。诺华在SABCS2021年会上公布CDK4/6抑制剂Kisqali(ribociclib,利柏西利)治疗各种基因组固有亚型的HR+/HER2-晚期或转移性乳腺癌(mBC)的一项探索性分析数据。与内分泌疗法(ET)相比,Kisqali联合ET显著提高这类患者的总生存期(中位OS:40.3个月vs29.4个月)。该结果与在惰性和侵袭性ET难治性亚型中显示出一致的总体生存益处。CDE已在10月受理Kisqali的上市申请。
5.Keytruda联合IL-15激动剂开展临床。SOTIO Biotech公司IL-15超级激动剂SOT101拟与默沙东PD-1抑制剂Keytruda(帕博利珠单抗,pembrolizumab)开展一项Ⅱ期临床,评估联合治疗晚期/难治性实体瘤的疗效与安全性。临床适应症将包括二线非小细胞肺癌、一线和二线皮肤鳞状细胞癌、一线微卫星高不稳定结直肠癌、二线肝细胞癌、一线转移性去势抵抗性前列腺癌、与二线卵巢癌。该项试验预计明年上半年启动。
6.默沙东暂停HIV新药两项III期临床。默沙东长效核苷逆转录酶易位抑制剂islatravir (ISL,MK-8591)暂停两项III期临床【IMPOWER 22 (MK-8591-022) 和IMPOWER 24 (MK-8591-024)】 的受试者入组工作,这两项研究均旨在评估每月口服1次的islatravir用于HIV-1感染高危人群的暴露前预防 (PrEP)效果。就在上一个月,由于发现参与试验的HIV感染患者因治疗而产生免疫细胞计数下降,默沙东叫停了这项评估islatravir与MK-8507(非核苷逆转录酶抑制剂)联合治疗的Ⅱ期临床IMAGINE-DR(MK-8591-013)。
医药热点
1.河南尝试将连锁药店纳入集采。河南省医保局近日印发《关于将部分零售连锁药店纳入我省药品集中带量采购范围(试点)的通知》。《通知》明确,凡是符合药品零售连锁企业实施统一企业标识、统一质量管理体系、统一计算机信息管理及追溯系统、统一采购配送、统一票据管理、统一药学服务规范管理的医保定点连锁药店均可参与试点申报。
2.3D打印安乐死胶囊舱计划在瑞士上市。近日,一款名为“Sarco”的3D打印安乐死胶囊舱在瑞士通过法律审核,计划明年在瑞士上市。这款胶囊仓由在澳大利亚注册的“解脱国际”组织创办人尼特舍克发明。希望自杀的当事人进入胶囊舱躺下并从内部启动自杀程序后,胶囊舱舱体下方的设备将向舱内注满氮气,舱内的氧气含量将从21%被迅速降低至1%。死亡过程约30秒。
3.“二代”奥密克戎常规核酸检测或难以发现。据美媒《Business Insider》报道,当地时间12月8日,奥密克戎变异毒株的一个新版本突变已被确认。这个新亚型被命名为BA.2,到目前为止,已经在南非、澳大利亚和加拿大被发现了七例。专家们表示由于它的遗传学特性,恐怕常规的核酸检测更加难以检测到。
评审动态
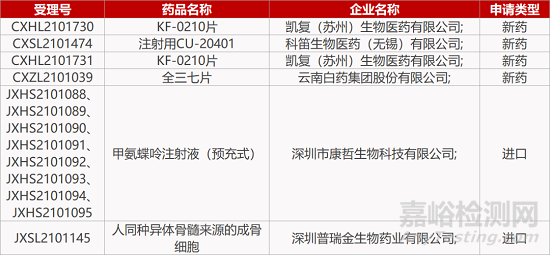
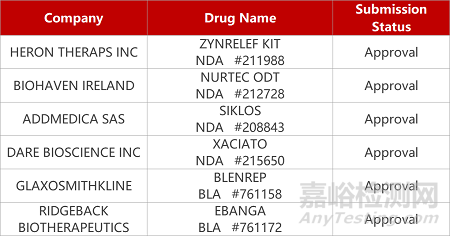

来源:药研发


