您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-02-07 15:59
一、医疗器械产品的海关税则号有哪些?
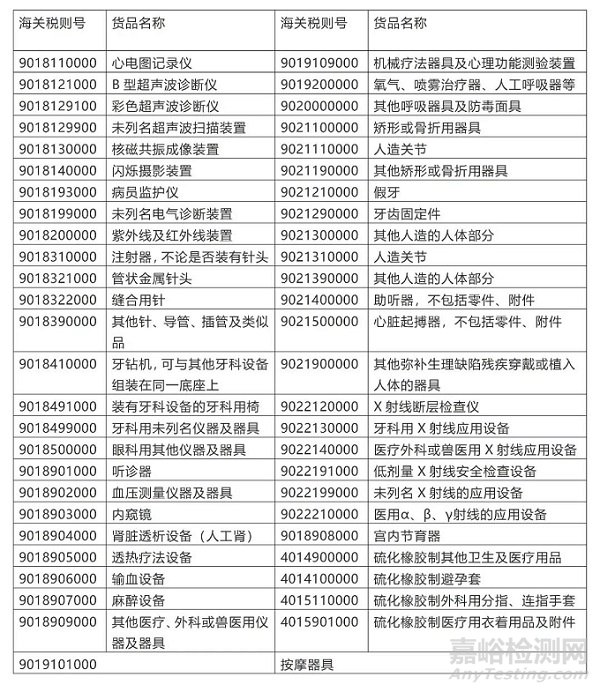
医疗器械的海关税则号主要集中在税则9018、9021、9022、9402等品目,在进出口报关和出口退税时根据不同产品查找对应的海关税则号,以下列举了部分医疗器械产品的海关税则号与名称以供参考。
二、医疗器械备案与注册
第一类医疗器械实行产品备案管理,第二类、第三类医疗器械实行产品注册管理。
向我国境内出口医疗器械的境外备案/境外注册申请人,由其指定的我国境内企业法人向国务院药品监督管理部门提交备案/注册申请资料和备案/注册申请人所在国(地区)主管部门准许该医疗器械上市销售的证明文件。未在境外上市的创新医疗器械,可以不提交备案人所在国(地区)主管部门准许该医疗器械上市销售的证明文件。
三、医疗器械产品进出口
1、出口医疗器械
出口医疗器械的企业应当保证其出口的医疗器械符合进口国(地区)的要求,一般不实施商品检验。
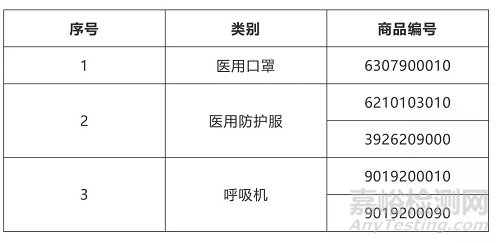
需要注意的是,根据海关总署公告2020年第53号及2020年第124号公告,对6307900010等5个10位商品编号项下的医疗物资实施出口商品检验。
温馨提示
对商品编号3005901000和3005909000项下属于危险货物的、商品编号3808940010项下属于危险化学品的,按出口危险货物或出口危险化学品检验监管要求执行。
2、进口医疗器械
2.1
■ 进口的医疗器械应当是已注册或者已备案的医疗器械,医疗器械注册证有效期为5年。有效期届满需要延续注册的,应当在有效期届满6个月前向原注册部门提出延续注册的申请。
■ 关于医疗器械注册证有效期。《食品药品监管总局关于执行医疗器械和体外诊断试剂注册管理办法有关问题的通知》(食药监械管2015年第247号):获准注册的医疗器械,是指与该医疗器械注册证及附件限定内容一致且在医疗器械注册证有效期内生产的医疗器械。

■ 医疗机构因临床急需进口少量第二类、第三类医疗器械的,经国务院药品监督管理部门或者国务院授权的省、自治区、直辖市人民政府批准,可以进口。进口的医疗器械应当在指定医疗机构内用于特定医疗目的。
2.2
■ 海关对进口医疗器械备案/注册证(包括医疗器械注册证、第一类医疗器械备案凭证)电子数据与进口医疗器械产品报关单电子数据实施联网核查。
■ 进口医疗器械报关时应提供合同、发票、装箱单、医疗器械备案/注册证。
2.3
■ 进口的医疗器械应当有中文说明书、中文标签。说明书、标签应当符合本条例规定以及相关强制性标准的要求,并在说明书中载明医疗器械的原产地以及境外医疗器械注册人、备案人指定的我国境内企业法人的名称、地址、联系方式。
2.4
■ 海关依法对进口的医疗器械实施检验;检验不合格的,不得进口。
(1)核对现场查验的商品信息、申报信息、准入信息三者是否一致。
(2)核实进口医疗器械铭牌的有关信息是否与备案或注册的制造商、商品名称、型号规格一致。
四、特殊要求
1、进口心脏起搏器特殊要求
1.1、海关总署指定海关对进口心脏起搏器实施检验监管,负责指定经国家认可的医疗器械检测机构对进口心脏起搏器进行检测。
2.2、北京海关、上海海关和海口海关为进口心脏起搏器指定检验实施机构。
2、进口呼吸机特殊要求
海关对进口高风险呼吸机进行重点监管,由北京、天津、大连、上海、青岛、武汉、广州等地海关开展相关检验监管工作。
五、进口捐赠医疗器械
禁止境外捐赠人在向国内捐赠的医疗器械中夹带我国列入《禁止进口货物目录》的物品。捐赠的医疗器械应为新品,并且已在中国办理过医疗器械注册,其中不得夹带有害环境、公共卫生和社会道德及政治渗透等违禁物品。
医疗器械产品禁止进口列举
禁止进口过期、失效、淘汰等已使用过的医疗器械。
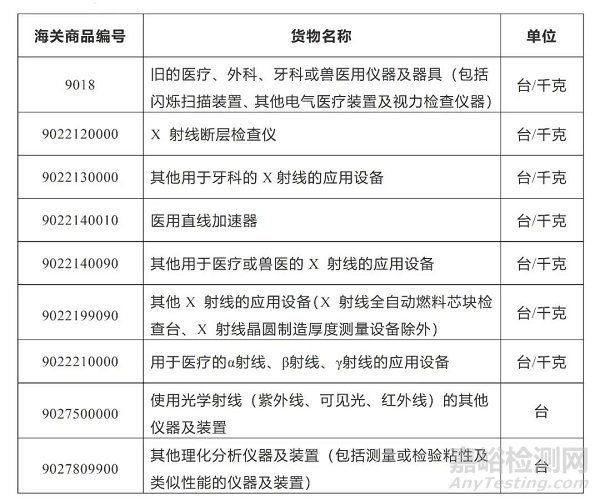
根据商务部海关总署2018年第106号公告,对禁止进口的旧机电产品目录进行了调整,自2019年1月1日起执行。

来源:海关发布


