您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-02-24 11:00
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.泽布替尼3项新适应症海外报产。 百济神州宣布,欧洲药品管理局(EMA)已受理BTK抑制剂百悦泽(泽布替尼)用于治疗慢性淋巴细胞白血病(CLL)患者和边缘区淋巴瘤(MZL)患者的两项新适应症的上市许可申请。同时,FDA已受理泽布替尼用于治疗成人慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)患者的新适应症上市许可申请(sNDA),PDUFA目标日期为2022年10月22日。
2.翰宇新冠多肽鼻喷剂对奥密克戎有效。翰宇药业日前发布“关于对深圳证券交易所关注函的回复公告”,其中详述了新冠多肽鼻喷剂对Omicron及Delta活毒感染体外细胞药效。采用5mmol小试实验室样品评估,结果显示针对Delta与Omicron毒株其EC50均达到纳摩尔级别,Delta的EC50为25.99纳摩尔,而Omicron在1纳摩尔浓度就达到100%的抑制效果。采用100mmol规模放大样品评估,Delta的EC50为12.99纳摩尔,Omicron在1纳摩尔浓度就达到100%的抑制效果。
3.瑞博ASO药物两项糖尿病Ⅱ期临床积极。瑞博生物从Ionis公司引进的反义寡核苷酸(ASO)药物ISIS449884注射液在针对2型糖尿病的两项Ⅱ期临床(RBGR1201和RBGR1202)均达到主要研究终点。ISIS449884治疗组较安慰剂组均可显著降低糖化血红蛋白(HbA1c)水平,且不增加低血糖事件和严重低血糖事件发生率。在二甲双胍治疗的基础上,ISIS449884显示出更强的具统计学意义的降HbA1c能力。此外,候选药物的安全性和耐受性良好。
4.复星PD-L1/FGFR抑制剂启动临床。复星医药PD-L1/FGFR小分子抑制剂FH-2001首次登记启动临床试验(CTR20220322),评估FH-2001胶囊在晚期实体瘤患者中的安全性和耐受性,并确定FH-2001胶囊的最大耐受剂量(MTD)或II期推荐剂量(RP2D)。主要研究者由中国科学院大学附属肿瘤医院(浙江省肿瘤医院)医学博士程向东担任。目前国内PD-L1小分子抑制剂已有6款进入临床;歌礼制药同类产品在今年1月已向FDA递交了IND申请。
5.康宁杰瑞双抗与再极TKI联合用药获批临床。康宁杰瑞PD-L1/CTLA-4双抗KN046获国家药监局临床试验默示许可,拟联合再极医药酪氨酸激酶抑制剂MAX-40279-01用于治疗晚期/转移性实体瘤。KN046采用机制不同的CTLA-4与PD-L1单域抗体融合组成;可靶向富集于PD-L1高表达的肿瘤微环境及清除抑制肿瘤免疫的Treg。KN046正在澳大利亚、美国、中国开展非小细胞肺癌等多项临床试验。MAX-40279-01是一款FLT3/FGFR双靶点的小分子药物,处于Ⅰ/Ⅱ期开发阶段。
6.复旦、沃森、蓝鹊合作开发新冠mRNA疫苗。复旦大学、云南沃森生物、上海蓝鹊生物签署三方战略合作协议,三方将共同促进“新冠mRNA疫苗”的开发及商业化。这款新冠突变体mRNA嵌合疫苗由复旦大学林金钟团队研发。动物实验和临床IIT研究均表明,这款疫苗对包括奥密克戎等多种新冠突变株均表现出良好的保护性。同时受试者两针接种不良反应低。
国际药讯
1.NICE推荐Bylvay治疗全部类型PFIC。英国国家卫生与临床优化研究所(NICE)发布指导意见,推荐将Albireo公司非全身性回肠胆汁酸转运抑制剂(IBATi)Bylvay(odevixibat)纳入国家医疗服务系统(NHS),用于6个月及以上人群,治疗所有类型的进行性家族性肝内胆汁淤积症(PFIC)。Bylvay是全球首个治疗PFIC药物,适用于治疗PFIC所有亚型(1、2、3型),该药已于去年7月获批在欧盟和美国上市。
2.艾伯维卡利拉嗪报抑郁症sNDA。艾伯维非典型抗精神病药物卡利拉嗪(cariprazine,Vraylar)在美国递交补充新药申请,用于辅助治疗重度抑郁症(MDD)患者。在一项Ⅲ期临床中,与安慰剂组相比,卡利拉嗪1.5 mg/天治疗组第6周时患者MADRS抑郁评定量表总分较基线的变化具有统计学显著性。此前,该药已获FDA批准用于治疗精神分裂症、I型双相情感障碍相关躁狂或混合发作的急性治疗、以及I型双相情感障碍相关抑郁发作的治疗。
3.默德纳RSV疫苗进入关键性Ⅲ期临床。默德纳公司宣布,数据和安全监测委员会(DSMB)已批准其预防呼吸道合胞病毒(RSV)的候选疫苗mRNA-1345展开关键临床试验的Ⅲ期部分。mRNA-1345是一种编码RSV融合前F糖蛋白的疫苗,与融合后状态相比,可引起更高的中和抗体反应。该疫苗使用与Moderna的新冠疫苗相同的脂质纳米颗粒(LNP),包含优化的蛋白和密码子序列。在Ⅱ期临床中,该疫苗在老年人中具有可接受的安全性特征。
4.杨森Tremfya/Simponi组合优效于单药。杨森在ECCO2022大会上公布IL-23拮抗剂Tremfya(特诺雅,古塞库单抗)联合TNF-α拮抗剂Simponi(欣普尼,戈利木单抗)治疗中重度活动性溃疡性结肠炎(UC)概念验证Ⅱa期VEGA研究(NCT03662542;EudraCT 2018-001510-15)积极数据。与Tremfya或Simponi单药治疗相比,联合治疗组第12周时的临床应答率更高(三组应答率分别为83.1%、74.6%、61.1%),而且该组的临床缓解率、内镜改善率、复合组织学内镜终点率也更优。各治疗组之间不良事件(AE)发生率具有可比性。
5.β蛋白干扰素抗新冠III期临床失败。Synairgen公司吸入式广谱抗病毒β蛋白干扰素SNG001治疗COVID-19住院患者的国际III期SPRINTER临床未达到主要或关键次要终点。结果显示,SNG001治疗组患者出院的可能性并不比安慰剂组高;两组在35天内进展为严重疾病或死亡的相对风险分别降低27%和36%;SNG001总体耐受性良好。标准护理的改变(如该试验中87%的患者在基线时曾接受系统性皮质类固醇治疗新冠,而在SNG001的II期临床中没有人接受)可能是未达疗效终点的部分原因。
6.肾细胞癌靶向新药长期疗效积极。AVEO Oncology公司在ASCO GU2022会议上公布VEGFR-TKI疗法Fotivda(tivozanib)治疗晚期肾细胞癌(RCC)Ⅲ期TIVO-3研究新数据。5年随访数据显示,在3线和4线RCC患者中,与拜耳靶向抗癌药Nexavar(多吉美,索拉非尼)相比,Fotivda治疗组3年和4年时疾病无进展生存(PFS)率分别为12% (vs 2%)和8% (vs 0%);研究人员对PFS的评估与独立审查委员会的结果一致。去年3月,FDA已批准Fotivda用于治疗接受过2种或2种以上系统治疗的复发/难治性RCC患者。
医药热点
1.国家儿童医学中心启动基因筛查“新巢计划”。国家儿童医学中心北京儿童医院日前启动一项“新巢计划”,发布了新生儿单基因遗传病筛查方案。“新巢计划”不仅涵盖了目前在新生儿疾病筛查领域应用较广泛的串联质谱筛查方法涉及的将近50种遗传代谢病,还将不同地区的高发病种整合其中,几乎涵盖我国发布的所有121种第一批罕见病目录。旨在提高我国遗传性出生缺陷的“早筛、早诊、早治”工作。
2.九大任务确保老年人安享晚年。近日,国务院印发《“十四五”国家老龄事业发展和养老服务体系规划》,部署了9方面具体工作任务。提出到2025年,我国养老服务床位总量要达到900万张以上,养老机构护理型床位占比达到55%,新建城区、新建居住区配套建设养老服务设施达标率达到100%,乡镇(街道)层面区域养老服务中心建有率达到60%,设立老年医学科的二级及以上综合性医院占比达到60%以上。
3.英格兰24日起取消一切防疫限制措施。英国政府21日宣布从24日起取消英格兰地区的所有新冠肺炎疫情限制措施:新冠检测阳性者将无须再自我隔离,政府也将不再追踪密切接触者,未完全接种疫苗的密切接触者也无须再自我隔离等。从4月1日起,该地区将不再为普通民众提供免费的新冠病毒检测,年长者和易感人群除外。
评审动态
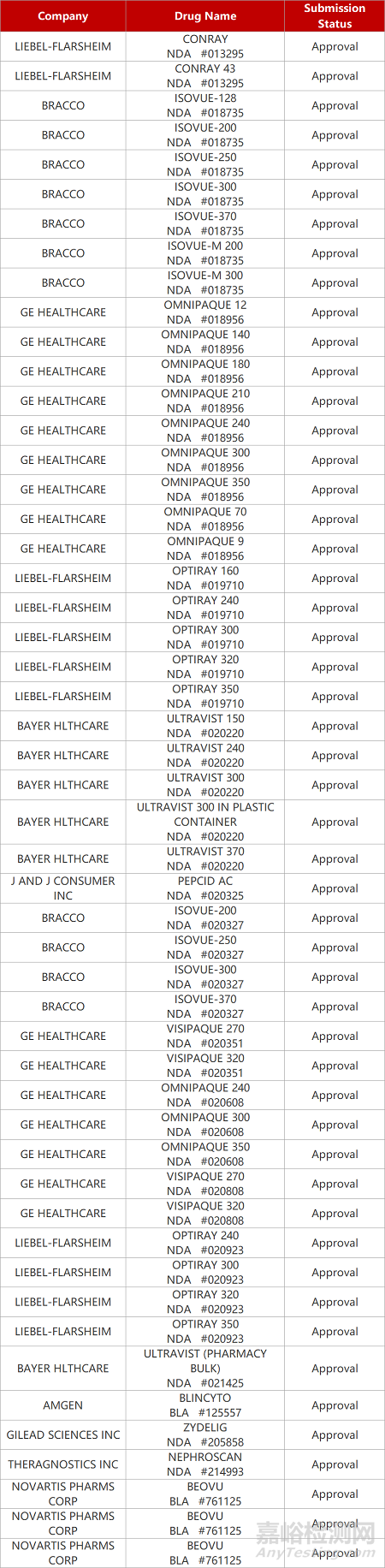
2. FDA新药获批情况(北美02月18日)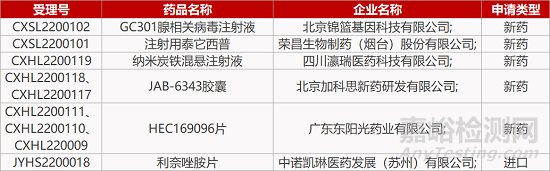

来源:药研发


