更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
上海红云EGFR-TKI在美获批临床。上海红云生物新一代EGFR-TKI抑制剂H002获FDA临床许可,即将在美国开展I/IIa期临床研究。H002是红云生物自主研发的一款具有广谱性和高选择性、拟用于治疗携带C797S突变的非小细胞肺癌的精准治疗候选药物,为该公司首个进入临床阶段的候选药物。在细胞和动物模型的试验中,H002均表现出对于多种单突变体、双突变体和三重突变体具有明显的抑制作用。
1.欧康维视新药结膜炎Ⅲ期临床积极。欧康维视与Nicox公司联合开发的新型眼用制剂Zerviate(0.24%盐酸西替利嗪滴眼液,OT-1001),在治疗过敏性结膜炎的中国Ⅲ期临床获积极结果。与对照药相比,OT-1001治疗第14天访视前24小时内眼痒分数与基线相比变化达到非劣效性标准,且安全性和耐受良好,不良事件发生率与对照药相似。FDA已批准Zerviate用于治疗过敏性结膜炎相关的眼痒。
2.科济CAR-T获批实体瘤Ⅱ期临床。科济药业自主研发的CAR-T产品CT041获国家药监局批准进入确证性Ⅱ期临床,用于治疗既往接受过至少二线治疗失败的Claudin18.2(CLDN18.2)表达阳性的晚期胃癌/食管胃结合部腺癌。CT041是一款靶向CLDN18.2的自体CAR-T细胞候选产品,该新药此前已分别获FDA和EMA授予的孤儿药资格,EMA授予的优先药物(PRIME)资格,以及FDA授予的再生医学先进疗法资格。
3.英派ATR抑制剂国内获批临床。英派药业ATR抑制剂IMP9064获国家药监局临床试验默示许可,拟临床用于评估IMP9064在晚期实体瘤患者的安全性、耐受性、药代动力学特征及疗效。IMP9064是英派药业自主研发并全球临床同步推进的一款1类新药,目前正在美国开展一项Ⅰ/Ⅱ临床,在晚期实体瘤患者中评估IMP9064单药治疗以及与PARP抑制剂senaparib联合治疗的安全性、药代动力学特征及疗效。
4.复星凯特第二款CAR-T获批临床。复星凯特从吉利德旗下公司Kite引进的CAR-T产品FKC889获国家药监局临床试验默示许可,拟用于既往接受过二线及以上治疗后复发或难治性套细胞淋巴瘤(r/r MCL)患者。Tecartus ®(FKC889)是首个也是唯一一个获批用于r/r MCL的CAR-T疗法,已于2020年7月和12月分别获得FDA和欧盟批准上市。在关键研究ZUMA-2中,中位随访17.5个月时,Tecartus的ORR为92%,CR率为67%。
5.天演药业与赛诺菲达成战略合作。天演药业与赛诺菲达成一项合作与许可协议,天演药业将利用其独特的安全抗体SAFEbody®技术,针对赛诺菲提供的新一代单克隆与双特异性抗体,合作开发新一代掩蔽抗体候选药物。根据协议,天演药业将获得1750万美元首付款,可能高达25亿美元里程碑潜在付款,以及产品销售的分成。赛诺菲将负责两款候选药物的独家开发和商业化,并有权提名额外两款候选药物进行开发与商业化。
国际药讯
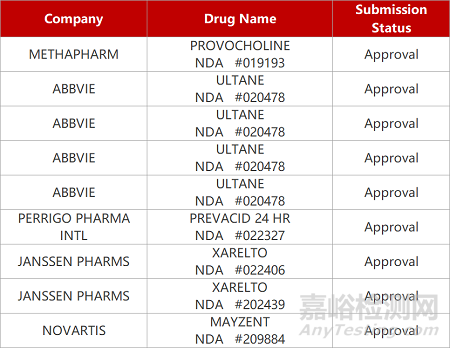
1.强生含药隐形眼镜获批上市。强生旗下Johnson & Johnson Vision Care开发的日抛型隐形眼镜Acuvue Theravision获FDA批准上市。这款隐形眼镜含有抗组胺药物酮替芬(ketotifen),可在眼部释放,缓解与眼睛过敏相关的症状。在Ⅲ期临床中,隐形眼镜佩戴者的眼部出现过敏性瘙痒时,无需使用治疗过敏的眼药水,在戴上Acuvue Theravision隐形眼镜3分钟后就能显著缓解眼痒,而且能缓解眼部瘙痒长达12小时。
2.Novavax新冠疫苗Ⅲ期临床积极。3月2日,Novavax公司公布重组蛋白新冠疫苗NVX-CoV2373在英国开展的关键性Ⅲ期临床的一项扩展分析。在6个月的监测期内(中位监测时间为101天),NVX-CoV2373保持较高的有效性,疫苗总体有效性为82.7%(95% CI:73.3,88.8),针对重症疾病的有效性为100%(95% CI:17.9,100),这与之前的初步分析一致。此前,这项Ⅲ期试验在中位监测时间为55天时,NVX-CoV2373的疫苗有效性达到89.7%(95% CI:80.2,94.6)。
3.三特异性T细胞激活疗法获快速通道资格。FDA授予Harpoon Therapeutics公司靶向BCMA的三特异性T细胞激活疗法HPN217快速通道资格,用于治疗既往至少接受过4种治疗的复发或难治性多发性骨髓瘤(RRMM)患者。目前,HPN217正在Ⅰ/Ⅱ期临床中评估治疗RRMM患者的潜力。2019年11月,Harpoon公司与AbbVie就HPN217达成了合作许可协议,艾伯维将在完成Ⅰ/Ⅱ期临床后行使其许可HPN217的选择权。
4.辉瑞RSV母体疫苗获突破性疗法认定。FDA授予辉瑞呼吸道合胞病毒(RSV)候选疫苗PF-06928316(RSVpreF)突破性疗法认定,用于通过产妇的主动免疫,预防从出生到6个月大的婴儿患上RSV相关下呼吸道疾病。RSVpreF包含融合前(prefusion)F糖蛋白,旨在对RSV A和RSV B两个亚型提供最佳保护。RSVpreF已在Ⅱb期概念验证临床中取得积极结果,该研究评估RSVpreF用于妊娠28-36周期间接种的18-49岁健康妊娠女性、及其婴儿中的安全性和免疫原性。辉瑞将在未来发表这项研究成果。
5.AAV基因疗法治疗AD早期临床积极。LEXEO公司AAV基因疗法LX1001治疗APOE4纯合子阿尔茨海默病患者的Ⅰ/Ⅱ期临床数据积极。在低剂量LX1001治疗队列(n=4)中,随访超过3个月时间的患者均观察到脑脊液中的APOE2蛋白表达;随访超过12个月时间的2例患者脑脊液中的tau蛋白水平和磷酸化tau蛋白水平与基线相比降低;LX1001的总体耐受性良好。此前,LX1001已获FDA授予的快速通道资格。
6.艾伯维IL-23抑制剂新适应症审查遭FDA延期。FDA延长对艾伯维新型抗炎药IL-23抑制剂Skyrizi(risankizumab,150mg)用于治疗年龄≥16岁的中重度克罗恩病(CD)患者的sBLA申请的审查期,将PDUFA日期延长3个月,以审查艾伯维提交的额外数据。在美国和欧盟,Skyrizi已获批用于治疗中重度斑块型银屑病(PsO),和活动性银屑病关节炎(PsA)。Skyrizi在2021年的全球销售额达到29.39亿美元,较上一年增幅达84.9%。
1.上海龙华医院江西医院揭牌。3月2日,上海中医药大学附属龙华医院江西医院在江西省中医院正式揭牌。龙华医院江西医院是江西省人民政府与上海中医药大学附属龙华医院合作共建医院,并以此为载体建设国家区域医疗中心。龙华医院江西医院选址位于江西省南昌市。项目规划编制床位1000张,总建筑面积19.5万平方米,总投资估算为16亿元, 预计2024年底投入使用。
2.江苏梳理家医中医诊疗项目。江苏省卫健委、省中医药管理局日前印发《江苏省家庭医生签约中医诊疗服务项目库(2022版)》,分类梳理出肺病、脾胃、脑病等13类60项适合基层开展的中医诊疗服务项目。江苏省计划大力推进中医药签约服务项目开展,健全签约服务中医药项目考核管理机制,推进家庭医生团队中医药服务全覆盖,满足群众对中医药服务的诊疗需求。
3.张锋胜诉CRISPR真核基因编辑专利纠纷。当地时间 2月28日,美国专利和商标局裁定来自哈佛和麻省理工学院博德研究所(Broad Institute)的张锋团队拥有在真核细胞中使用CRISPR的专利。根据这一裁决,张锋创立的基因编辑公司Editas Medicine 在美国可获得涵盖所有人类细胞的CRISPR-Cas9和CRISPR-Cas12a的基因编辑专利。诺奖得主Jennifer Doudna 和 Emmanuelle Charpentier 所属的CVC团队表示,将继续向联邦巡回上诉法院上诉。