您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-07-15 11:02
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
国际药讯
1.Novavax新冠疫苗获批EUA。FDA授予Novavax新冠重组蛋白疫苗NVX-CoV2373紧急使用授权(EUA)。一项III期临床数据显示,该疫苗的总体疗效为90.4%,其中针对65岁及以上人群的保护力达到78.6%。但由于该研究是在Delta和Omicron变种出现之前进行的,因此该疫苗没有针对Omicron毒株的保护力数据。至此,FDA已批准4款新冠疫苗,分别为辉瑞/BioNtech和Moderna的mRNA疫苗、强生的腺病毒载体疫苗、Novavax的重组蛋白疫苗。
2.卡博替尼治疗肾细胞癌Ⅲ期临床积极。Exelixis公司卡博替尼(cabozantinib)联合纳武利尤单抗和伊匹单抗方案治疗晚期肾细胞癌的关键Ⅲ期临床COSMIC-313达到主要终点。与安慰剂联合纳武利尤单抗和伊匹单抗相比,cabozantinib与纳武利尤单抗和伊匹单抗联合治疗使患者的疾病进展或死亡的风险显著降低(HR:0.73;95% CI:0.57-0.94;P=0.01),提高了患者的无进展生存期。
3.安进KRAS组合疗法早期临床积极。安进KRAS G12C抑制剂Lumakras(sotorasib)联合SHP2酪氨酸激酶受体(RTK)抑制剂RMC-4630治疗非小细胞肺癌(NSCLC)和结直肠癌(CRC)等肿瘤患者的Ⅰb期临床结果积极。在11例NSCLC患者中,达到27%的确认部分缓解率和64%的疾病控制率;在6例结直肠癌患者中,有5例达成疾病控制,包含其中1例患者有达26%肿瘤负担的减少。研究中无具临床意义的药物交互作用。
4.早期莱姆病分子诊断产品获突破性器械认定。T2 Biosystems公司分子诊断检测产品T2Lyme Panel获FDA授予突破性医疗器械认定,用于莱姆病早期检测。莱姆病是由蜱虫叮咬导致疏螺旋体菌等进入人体,引起系统性感染的一种疾病。T2Lyme Panel可同时检测引起莱姆病的伯氏疏螺旋体菌、阿氏疏螺旋体菌和加氏疏螺旋体菌。该产品拟开发用于检测具有莱姆病体征和症状的个体,并辅助诊断早期莱姆病。
5.EVEON拟开发鼻腔给药干细胞疗法。EVEON宣布启动欧洲INDENEO(INtraNasal Device for NEOnates)项目以开发一种新型的鼻对脑递药装置,用于新生儿脑病包括干细胞再生疗法等生物制品及先进疗法治疗。鼻腔给药方式不仅具有微创、药物起效迅速的优点,而且感染风险更低。研究表明,鼻腔内给药可以完全绕过血脑屏障,并允许直接进入脑组织,从而实现大量鼻对脑新疗法的开发。
6.默沙东达成前列腺癌创新疗法合作。默沙东与Orion公司就后者一款临床期口服非类固醇CYP11A1抑制剂ODM-208达成全球研发合作协议。ODM-208正在Ⅱ期临床中用于治疗转移性去势抵抗性前列腺癌(mCRPC)。根据协议,Orion将获得2.9亿美元前期付款。在默沙东选择ODM-208的全球开发和商业化权益时,Orion还将获得潜在的研发和商业化里程碑付款。默沙东将承担所有已有和未来开发和商业化费用。
医药热点
1.方舱医院装备配置指南出台。国家卫健委印发《方舱医院装备配置指南(试行)》,要求方舱医院装备配置应做好空间规划,提前预留装备安装空间和条件。方舱医院装备配置建议清单主要包括基本医疗装备及部分必要的非医疗装备。其中,医疗装备包括心电监护仪/多参数监护仪、输液泵、无创呼吸机等53项装备,非医疗装备主要包括手腕带、氧气瓶、床单元、消毒机等23项装备。各地可结合自身实际情况,合理调整装备配置品目,并做好相关医用耗材的储备。
2.坦桑尼亚3人因“神秘疾病”死亡。坦桑尼亚卫生部首席医疗官13日宣布,该国东南部出现一种“神秘疾病”,已造成3人死亡。坦桑尼亚卫生部首席医疗官称,这种疾病类似于埃博拉病毒和马尔堡病毒,患者会出现发烧、头疼、疲劳和流鼻血等症状,与此同时,患者的新冠检测都呈阴性。目前在坦桑尼亚东南部林迪区已有13例神秘疾病确诊病例,只有1人康复,除了3名死亡病例之外,其余患者目前均被隔离。
评审动态
1. CDE新药受理情况(07月14日)
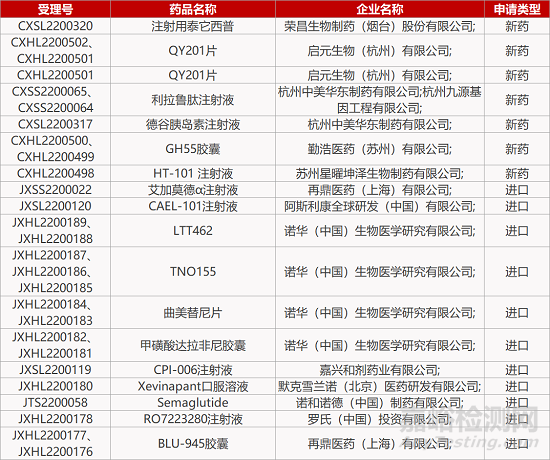


来源:药研发


