您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-08-01 15:01
新药的开发之初着重于新化学实体的筛选,通常在筛选之初不会注重固态形式的药物所具有的基本理化性质(如溶解度),主要通过构效关系选择最具有活性的药物分子。筛选最佳化学结构后,根据化合物的性质,如酸碱性,进一步筛选酸/碱/盐的形式。最后,进行固态晶型的筛选,即使选择开发形式为盐型,仍需要多晶型的筛选,选择优势晶型。多晶型现象在新药开发中屡见不鲜,如何不在“乱花渐欲迷人眼”中迷离,找到适合的固态形式开发,推进项目向申报快速进发,才是硬道理。一般来说,对于多晶型的筛选首选最稳定的晶型。晶型的稳定性受同一化合物所呈现的不同理化性质所决定,所以深刻的理解多晶型形成的原理以及同一化合物不同晶型在理化性质上的差异,有助于最终决策新药固态开发形式。下面我们深入了解一下:多晶型及其理化性质。
同一化合物具有不同的晶体结构的现象,称之为“多晶型现象”。从分子水平上看,相同化合物结构的晶格具有不同的分子排列和(或)构像。药物分子在结晶时受各种因素的影响,使分子骨架与取代基以及分子中碳原子手性等发生变化,同时药物分子之间、药物分子与溶剂分子之间的相互作用或结合力发生变化,都将导致构成晶体的分子或原子在晶格中的空间排列不同,从而形成了不同的晶体结构。由上可知,药物晶型的差异,造成药物分子在晶格中的排列方式的不相同,进而影响晶体中分子间的相互作用,从而造成了不同晶型间性质的差异。

引用自参考文献1
一般多晶型性质的差异如图1所示,包括以下几个方面:①化学性质,化学反应活性/稳定性、光化学反应活性;②动力学性质,溶出速率、固态反应动力学、稳定性、结晶生长速率;③机械性能,可压性、硬度、粉体流动性,可压片性、抗张强度;④堆积/物理性质,导电性,密度(摩尔体积),吸湿性、折射率、颜色、颗粒形态;⑤表面性质,界面张力,表面积,表面自由能;⑥热力学性质,化学势、自由能、溶解度、焓、熵、热容、熔点、升华温度、蒸汽压。同一药物不同的晶型具有不同的物理性质,如熔点,溶解度,溶出速率,进而影响药物的体内吸收,影响制剂的生物利用度;药物对于光,热,湿的敏感程度上的差异,造成了不同不同晶型间在化学性质上的差异,如水解,氧化。下面我们具体谈谈不同晶型间常用理化性质的差异。
1.熔点
熔点是固液两相达到平衡时的温度。同时,熔点也是衡量用于克服将晶体结合在一起的吸引力所需要的能量的参数。一般来说,药物晶型的差异来源于晶格中,原子间或者分子间距离及作用力的不同,造成了破坏晶格所需要的能量不同,造成了多晶型熔点,熔化热的差异。一般,熔点低,熔化热低的晶型中分子以弱相互作用力结合,熔点高,熔化热高的晶型分子间的作用力要强。从上可知,不同的晶型具有不同的熔点,可以通过熔点的检测间接证明化合物的晶型及晶型稳定型。
普通固体制剂开发过程,比较理想的化合物熔点在100℃以上。普遍认为低于60℃的物质将难以开发,高速剪切制粒和压片过程,温度常常超过40℃,而流化干燥温度将接近甚至超过80℃。但是,需要注意如果化合物熔点过高,比如大于200℃,可能由于晶格能较强,影响固态物质的溶解度,熔点如何影响溶解度见方程1。
2.溶解度
化合物的溶解度,一般指平衡溶解度,即在一定温度和压力之下,固体物质在一定溶剂中达到固液平衡时所溶解的溶质的量,是化合物的固有性质。但是,对于溶解度的数值并不一定是固定不变的,其和化合物的固态形式(无定形态,亚稳定型晶型,稳定型晶型),溶解化合物的溶剂成分(比如不同缓冲溶液体系)以及测量方法(平衡时间,样品处置方法等)都有关系。固体物质的溶解度一般与其自由能相关,一般稳定型的结晶熵小,熔点高,溶出速率慢,溶解度小;亚稳定型相反,无定形型更甚不同,具有更大自由能,热力学不稳定,提高固态物质的溶解度和溶出速率。
由Jain和Yalkowsky在2001年建立的修改后的一般溶解度方程(GSE)可以阐明logP和Tm在溶解度中的作用,方程1如下:

其中S0是固有溶解度,即非电离(中性)物质的溶解度。利用GSE和亲脂性(logP为2、4和6)和熔点(Tm为50、150和250°C)的假设值可以帮助确定哪些特性主导溶解度,反映了物质晶格能(熔点)和脂溶性(分配系数)与溶解度的重要关系。
API分子的堆积形式的差异造就了多晶型现象,多晶型化合物具有不同的晶格能进而影响了同一分子不同晶型的溶解度差异,具体实例如表1,2。
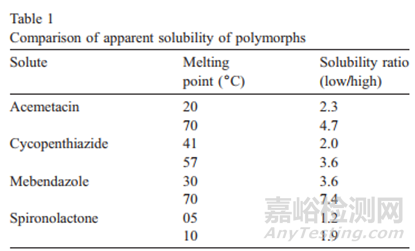
引用自参考文献2

引用自参考文献3
3.溶出
溶出是固体物质溶解的过程。作为固体的基本属性,它受固体和围绕它的液体介质之间的亲和力控制。描述药物溶出过程的理论有很多。Noyes-Whitney方程可能是最常用来描述药物溶出过程和阐明药物溶出中起关键作用的物理化学性质的影响(方程式2):
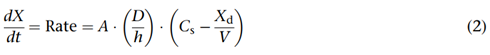
其中dX/dt是溶出速率,A是可用表面积,D是扩散系数或扩散率,h是与溶解药物表面相邻的扩散层或边界层的厚度,Cs是平衡或饱和溶解度药物,Xd是溶解固体的量,V是溶出液的体积。

图2 影响溶出的理化性质(引用自参考文献4)
在同一化合物不同晶型具有不同的溶解度,从而影响药物的溶出速率,如图2可见,影响溶出的因素,包括平衡溶解度,粒径,多晶型和扩散系数。同一晶型,具有不同的粒度/晶癖,将具有不同的表面积和形态,溶出速率也会不同,因为溶出速率与溶出的粉末表面积成正比。

图3 粒径对非那西丁在 0.1 N 稀释胃液中溶出率的影响(引用自参考文献4)
图3说明了粒径减小对非那西汀溶出的影响。对于难溶性药物,通常采用减小粒径(至约3-5μm)作为提高药物溶出率的成功策略。重要的是要注意,对于某些药物,粒径过小会导致表面电荷暴露,从而延缓药物溶出速度。粉末的可用有效表面积在一定程度上取决于溶出介质润湿颗粒的能力。如果溶出介质的润湿性较差,则微粉化会产生粉末颗粒的团聚,由于表面积增加,会导致溶出速率降低。
4.化学稳定性
制剂中的药物分子应该有一定的稳定性以保证药品有一个符合要求的贮存期。对于普通口服固体制剂一般贮存期/货架期为两年。片剂/胶囊是最常开发的固体剂型,其固态的稳定型更加尤为重要。由于不同晶型的自由能不同,其化学性质存在差异,受处方因素(辅料)及非处方因素(光,热,水)的影响,将影响其化学反应(常见的化学反应:水解,氧化,光解)的速度与程度。
不同固体形式暴露不同的晶体表面的反应基团不同,这样可以加速或者抑制特定反应的发生。不同的固态形式引湿性是不一样,水分作为化学反应的参与者或者提供场所,增加化合物分子的流动性,对于化学反应产生不利的影响。
5.生物利用度
药物溶出是药物吸收的先决条件,而吸收反过来又影响给药剂量到达全身循环的速率和程度。对于许多容易穿过肠黏膜的药物,胃肠道中的药物浓度将由制剂释放其药物成分然后药物溶解所需的时间来控制。同一药物不同晶型具有不同的溶解度和溶出,进而影响药物吸收,进而影响生物利用度。
总结
药物分子结构-药物固态形式-药物制剂三个不同层级之间具有千丝万缕的联系,前期药物的发现阶段,致力于找寻活性最佳的化合物结构,开发优势晶型,只有这样,后期制剂开发才具有意义,三者又缺一不可。深刻的理解多晶型背后的逻辑与内涵,了解不同固态形式所具有的理化性质,依据理化性质以及其可生产性,助力固态形式开发,推动新药项目向着申报,上市扬帆起航。
参考文献:
1.Crystal Polymorphism in Chemical Process Development
2.Preformulation Studies and Enabling Formulation Selection for an Insoluble Compound at Preclinical StagedFrom In Vitro, In Silico to In Vivo.
3. 现代药剂学-第三节 药物的同质多晶现象.
2. Drug dissolution: significance of physicochemical properties and physiological conditions.
3. Computational prediction of drug solubility in water-based systems: Qualitative and quantitative approaches used in the current drug discovery and development setting.
4. Preformulation Studies and Enabling Formulation Selection for an Insoluble Compound at Preclinical Staged From In Vitro, In Silico to In Vivo.

来源:药事纵横


