您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-09-01 11:16
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.默沙东九价HPV疫苗适用人群扩大。默沙东九价人乳头瘤病毒(HPV)疫苗(酿酒酵母)获国家药监局批准新适应症,适用人群从19-26岁拓展至9-45岁适龄女性,用于接种预防HPV相关疾病。目前,国内博唯生物、康乐卫士、瑞科生物、万泰生物、瑞科生物等企业的九价HPV疫苗已进入Ⅲ期临床阶段;更高价次的HPV疫苗在研发中,包括中国医药集团的11价HPV疫苗、神州细胞的14价HPV疫苗等。今年3月,成大生物和康乐卫士合作开发的重组十五价人乳头瘤病毒疫苗(大肠埃希菌)也获得CDE临床批件。
2.恩格列净在华获批新适应症。勃林格殷格翰与礼来联合开发的SGLT2抑制剂恩格列净片(欧唐静)获国家药监局批准一项新适应症,用于降低心力衰竭成人患者的心血管死亡和因心力衰竭住院的风险。这是欧唐静在中国获批的第3项适应症。此前,恩格列净已被批准用于改善2型糖尿病患者的血糖控制,以及用于治疗射血分数降低的心力衰竭成人患者。
3.诺诚健华CD19抗体在香港报产。诺诚健华从Incyte引进的CD19单抗tafasitamab的生物制品许可申请(BLA)获得中国香港卫生署受理,联合来那度胺治疗不适合自体干细胞移植条件的复发/难治弥漫性大B细胞淋巴瘤(DLBCL)成人患者。在海外,这一组合疗法用于上述适应症已获得FDA和EMA有条件批准上市。在国内,tafasitamab联合来那度胺正在开展Ⅱ期注册临床试验。诺诚健华拥有该单抗的大中华区权益。
4.万泰二价HPV疫苗5.5年随访数据积极。万泰沧海双价人乳头瘤病毒(HPV)疫苗(大肠杆菌)馨可宁(Cecolin)III期临床66个月随访数据在《柳叶刀-感染病学》杂志上发表。结果显示,在符合方案(PPS)的人群中,接种疫苗组预防HPV16/18型相关病变的效果为100.0%(95%CI: 67.2%-100.0%),预防HPV持续感染的效果为97.3%(95%CI: 89.9%-99.7%),均显著优于对照组;不同年龄组预防HPV16/18型相关病变的效果均为100.0%。疫苗组和对照组的严重不良事件发生率相似,均与疫苗接种无关。
5.达石长效不成瘾镇痛药拟在美报IND。达石药业NGF单抗DS002治疗癌痛的Pre-IND申请获FDA受理。一项在国内健康受试者中完成的I期临床结果显示,DS002的耐受性良好,药代特征可以支持每8周给药一次的超长效。目前,该新药正在国内IIa期临床中评估用于癌痛病人的安全性和镇痛效果。该公司拟在美国跳过健康受试者中的安全性和代谢研究,直接在癌症病人中开展安全性和药效研究。
国际药讯
1.Moderna新冠二价疫苗获澳大利亚批准。澳大利亚治疗用品管理局(TGA)批准Moderna公司新冠加强疫苗mRNA-1273.214上市,用于18岁及以上成人的预防接种。mRNA-1273.214是一款二合一的二价疫苗,可以同时对抗原始毒株、Omicron变异株BA.4/5以及BA.1亚型。在一项II/III期临床中,mRNA-1273.214加强剂量针对Omicron的中和抗体水平提升8倍。与目前授权的加强剂(mRNA-1273)相比,mRNA-1273.214对Omicron亚变体BA.4和BA.5均产生有效的中和抗体反应。
2.西地那非乳膏女性性冷淡IIb期临床积极。Daré Bioscience公司PDE5抑制剂西地那非乳膏治疗女性性唤起障碍(FSAD)的IIb期Respond研究中期结果积极。西地那非乳膏是在性活动前局部应用于阴道组织,以促进血管舒张并增加生殖器血流量,从而改善与FSAD相关的生殖器唤醒反应症状并改善性体验,同时也避免了口服制剂的全身副作用。目前全球共有5款针对FSAD的在研产品,进展最快的是辉瑞的CP-866087和Daré Bioscience的西地那非乳膏,均已进入II期临床阶段。
3.安进PCSK9类降脂药长期疗效积极。安进在2022 ESC大会上更新PCSK9抑制剂依洛尤单抗(瑞百安、Repatha)治疗动脉粥样硬化性心血管疾病(ASCVD)的III期FOURIER-OLE研究长期疗效数据。最新数据显示,Repatha显著并持续降低了LDL-C水平,80%的患者在第12周达到了LDL-C水平<55mg/dL。LDL-C水平较基线下降了58%,与长期随访(第260周)的结果一致。此外,没有观察到新的安全性信号。另一项探索性分析数据显示,Repatha可使主要不良心血管事件发生率下降22%,包括心血管死亡风险下降23%。
4.安进KRAS抑制剂肺癌Ⅲ期临床积极。安进KRAS G12C抑制剂Lumakras(sotorasib)治疗KRAS G12C突变的非小细胞肺癌(NSCLC)经治患者的Ⅲ期临床(CodeBreaK 200)达到主要终点。与静脉输注多西他赛相比,Lumakras显著提高患者的无进展生存期。去年5月,Lumakras已获FDA加速批准上市,用于治疗携带KRAS G12C突变的NSCLC患者。这项研究积极结果将为Lumakras的加速批准转化为完全批准提供试验证据。
5.赛诺菲长效血友病疗法获FDA优先审评。赛诺菲与Sobi联合开发的新型凝血因子VIII重组蛋白疗法efanesoctocog alfa(BIVV001)获FDA授予优先审评资格,用于血友病A的治疗,PDUFA日期为明年2月28日。在一项Ⅲ期临床中,每周一次efanesoctocog alfa预防性治疗的患者中位与平均年出血率(ABR)分别为0.00(四分位距:0.00-1.04)与0.71(标准差:1.43);治疗组与对照组的平均ABR分别为0.69与2.96,预估BIVV001降低了约77%的年出血率。
6.法布里病创新基因疗法早期临床积极。Sangamo公司一次性输注、肝脏靶向的基因疗法isaralgagene civaparvovec(ST-920),在治疗法布里病(Fabry disease)的Ⅰ/Ⅱ期临床STAAR最新结果积极。5例治疗时间最长的患者,其体内所递送GLA基因所编码之α-半乳糖苷酶A(α-Gal A)活性持续上升;在最后一次测量时,达到将近高于3-17倍正常平均值的α-Gal A活性。第6例患者的α-Gal A活性则在治疗后两周内达到正常范围。药物的总体耐受性良好,Sangamo正在规划可能的Ⅲ期临床试验。
医药热点
1.福建调整公立医院专家门诊诊查费。近日,福建省医保局、福建省卫健委印发《关于调整公立医院专家门诊诊查费有关问题的通知》指出,医院每周可安排开展1~2次诊治疑难杂症为主的专家门诊;专家门诊区域须与普通门诊分开,每半天诊疗的患者数不超过10~15名(一档10名、二档12名、三档15名),每位患者平均诊疗时间不少于15~20分钟;专家门诊诊查费分三档实行最高限价管理。其中,一档:两院院士、国医大师和专技一级;二档:全国名中医、专技二级和国务院政府特殊津贴享受者;三档:福建省名中医。
2.美国现首例猴痘死亡病例。美国得克萨斯州的卫生官员当地时间8月29日宣布,他们正在调查一例确诊猴痘同时“严重免疫力低下”的死亡病患的死因。这是迄今为止在美国公开宣布的首个猴痘死亡病例。目前尸检正在进行中。截至29日,美国范围内已经报告了18000多例猴痘病例,得克萨斯州共有1604例病例。
3.阿斯利康新副总裁上任。8月30日,阿斯利康宣布,任命刘明为阿斯利康中国副总裁,肿瘤事业部肺癌治疗及肿瘤免疫治疗相关领域事业部负责人,并加入中国管理团队,直接向阿斯利康肿瘤事业部总经理陈康伟汇报。刘明在医药领域有超过20年经验,加入阿斯利康前,他在诺华制药任肿瘤副总裁,实体肿瘤事业部负责人,负责诺华包括乳腺癌,肺癌,黑色素瘤,神经内分泌肿瘤罕见病等领域。
评审动态
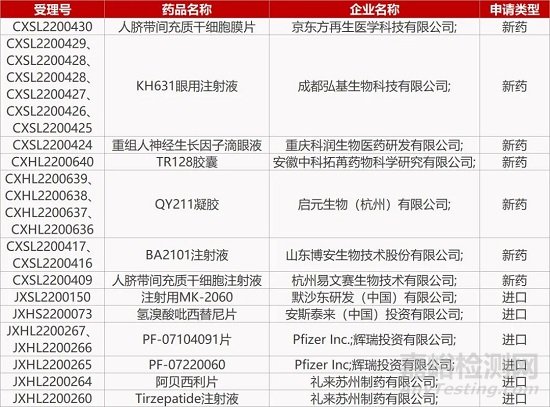
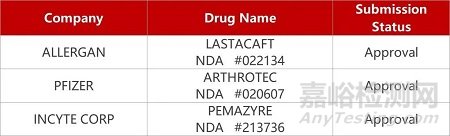

来源:药研发


