今日头条
嘉晨西海srRNA药物上I期临床。嘉晨西海自复制型RNA(srRNA)产品JCXH-211注射液在治疗恶性实体瘤的I期临床首例患者入组。该项试验旨在评估JCXH-211用于头颈癌、肝癌、黑色素瘤、三阴乳腺癌和食道癌等实体瘤治疗的安全性和耐受性,并为II期临床确定推荐剂量。JCXH-211能够以较低剂量在体内长效表达白介素-12(IL-12)。去年11月,该新药已获FDA临床许可。
国内药讯
1.GSK美泊利珠单抗新适应症在华报产。葛兰素史克IL-5抗体美泊利珠单抗注射液新适应症上市申请获CDE受理,用于治疗嗜酸性粒细胞性重度哮喘(SEA)。在III期MENSA研究中,美泊利珠单抗可将患者的哮喘发作频率降低53%。在SIRIUS研究中,美泊利珠单抗组患者的每日口服糖皮质激素药物剂量降低可能性是安慰剂组的2.39倍。该新药也是在国内申报SEA适应症的首款药物。
2.康方PD-1/CTLA-4双抗胃癌III期临床完成入组。康方生物自研PD-1/CTLA-4双抗卡度尼利单抗注射液(开坦尼®)联合化疗一线治疗不可手术切除的局部晚期或转移性胃腺癌或胃食管结合部腺癌(GC/GEJC)的关键III期注册临床完成患者入组,预计试验的期中分析时间为2023年底。这是全球首款获批上市、基于PD-1的双抗药物,已获CDE批准用于复发或转移性宫颈癌患者。目前,该新药正在开展多项临床试验,涉及肝细胞癌、鼻咽癌和非小细胞肺癌等适应症。
3.硕迪小分子GLP-1R激动剂启动Ib期临床。硕迪生物口服小分子GLP-1R激动剂GSBR-1290在ClinicalTrials.gov官网上登记注册一项Ib期临床试验,拟评估用于超重/肥胖受试者中的安全性、耐受性和药代动力学。该项试验预计2023年9月21日完成。全球范围内共10款GLP-1R多肽药物上市,但尚无口服GLP-1R小分子药物上市。硕迪生物计划开发GSBR-1290用于治疗2型糖尿病和肥胖症。
4.中源协和干细胞疗法报新IND。中源协和旗下武汉光谷中源开发的1类生物制品“VUM02注射液”的两项新适应症临床试验申请获CDE受理。VUM02注射液(人脐带源间充质干细胞注射液)是中源协和公司自主研发的冷冻保存型干细胞制剂,是由健康胎儿脐带组织经体外分离、筛选、扩增后制备的人脐带源间充质干细胞(UC-MSC)悬液。此前,该新药已获批开展用于治疗失代偿肝硬化的临床试验。
5.安进/百济神州DLL3/CD3双抗在华报IND。安进1类生物药Tarlatamab(AMG 757)的临床试验申请获CDE受理。Tarlatamab是一款半衰期延长的双特异性T细胞接合剂(HLE BiTE®),结合DLL3和CD3形成细胞溶解突触,诱导T细胞活化和扩增以及T细胞依赖性肿瘤细胞杀伤,拟用于小细胞肺癌(SCLC)的治疗。在I期临床中,Tarlatamab的确认ORR为23%,疾病控制率为51%。
6.加科思将公布三项临床前研究数据。加科思药业宣布,将在AACR2023年会上公布三项临床前研究数据,包括KRASmulti抑制剂JAB-23425、CD73-STING iADC JAB-X1800和极光激酶A抑制剂JAB-2485。其中,加科思KRASmulti系列分子的先导化合物JAB-23425,可显著抑制包括G12D、G12V、G13D在内的多种KRAS突变肿瘤,以及KRAS野生型扩增肿瘤;而且对非KRAS依赖的细胞无影响。该新药有望为KRAS突变肿瘤患者的提供新的治疗选择。
国际药讯
1.施维雅IDH1/2抑制剂胶质瘤Ⅲ期临床成功。施维雅IDH1/IDH2双重抑制剂vorasidenib单药治疗残留或复发IDH突变低级别胶质瘤患者的Ⅲ期临床(INDIGO)达到主要终点和次要终点。中期分析显示,与安慰剂组相比,vorasidenib治疗组患者的无进展生存期和至下一次干预的时间的统计均显示出显著改善。Vorasidenib治疗的安全性特征与之前公布的数据一致。目前,该新药的上市申请已获得FDA授予快速通道资格。
2.FIC心房颤动药物Ⅱ期临床积极。Acesion Pharma潜在“first-in-class”的SK离子通道抑制剂AP30663治疗心房颤动(AF)患者的概念性验证Ⅱ期临床(AP30663 IV)达到主要终点。分析显示,接受5 mg/kg AP30663治疗组患者自AF转换为正常窦性心律的比率超过50%(安慰剂转换率:0),且观察到在接受3、5 mg/kg药物治疗患者间存在剂量反应关系。试验中未观察到室性心律失常事件。
3.AMPK激活剂将启动减肥概念验证临床。Amplifier公司宣布其泛AMPK(腺苷酸活化蛋白激酶)激活剂ATX-304计划在今年晚些时候在欧洲开展评估用于快速消耗脂肪的Ⅰb期临床概念验证试验。AMPK的活化可促进脂质代谢,在代谢、心血管、肾脏疾病和癌症中具有广泛的治疗潜力。临床前研究显示,即便食用高脂肪含量的食物,接受ATX-304药物治疗的小鼠仍然纤瘦并维持健康。
4.诺和诺德司美格鲁肽复方启动I期临床。诺和诺德开发的NNC0194-0499/司美格鲁肽复方制剂在clinicaltrials.gov网站上登记注册一项I期临床试验,拟评估用于健康受试者中的安全性、耐受性和药代动力学特征。NNC0194-0499/司美格鲁肽复方制剂拟开发的临床适应症为非酒精性脂肪肝炎(NASH)的治疗。NNC0194-0499是诺和诺德开发的一种成纤维细胞生长因子21(FGF21)类似物,拟用于治疗非酒精性脂肪肝炎(NASH)和肥胖。
5.第一三共启动HER2-ADC联合疗法I期临床。阿斯利康与第一三共联合开发、靶向HER2的ADC药物德曲妥珠单抗在clinicaltrials.gov网站上登记注册一项I期剂量递增和剂量扩展研究,拟评估与DS-1103a联用治疗实体瘤患者的安全性和有效性。DS-1103a是第一三共开发的一种靶向信号调节蛋白α(SIRPα)的单抗药物,目前处于I期研究阶段。在国内,宜明昂科、石药集团、信达生物、礼新医药等药企也布局SIRPα靶点药物开发。
6.mRNA疫苗治疗HPV感染临床前数据积极。来自巴西圣保罗大学与宾夕法尼亚大学的联合研究团队开发的三种可编码产生gDE7蛋白组分的mRNA疫苗在治疗感染HPV的小鼠的临床前研究中获积极数据。所有接种修饰碱基对的mRNA疫苗或经过自扩增RNA技术修饰的疫苗的小鼠存活率100%。三种mRNA疫苗中的任何一种都能够清除小鼠的肿瘤,在实验结束前,绝大多数小鼠保持着无癌症的状态。
7.MacroGenics扩大与Synaffix的ADC合作。Synaffix宣布扩大与MacroGenics的许可协议,MacroGenics追加4个ADC项目。此交易包括22亿美元的潜在付款总额以及净销售额的分层版税,MacroGenics合作开发的ADC项目将达7款。2022年2月,两家公司已达成5.86亿美元合作,Synaffix基于GlycoConnect、HydraSpace和toxSYN三项ADC技术平台,以支持MacroGenics研发3款ADC药物。
医药热点
1.13位医学专家当选十四届全国政协常委。3月10日,全国政协十四届一次会议第三次全体会议选举产生第十四届全国委员会主席、副主席、秘书长和常务委员。根据公布名单梳理,呼吸病学专家王辰院士、胸外科专家王俊院士、心血管病专家葛均波院士,以及刘旭光、阮诗玮、赵家军、胡刚、徐涛、高秀梅、黄宇光、舒红兵、蔡威、蔡秀军等十多位医学专家,当选第十四届全国政协常委。
2.《医疗保障基金飞行检查管理暂行办法》印发。为进一步加强医保基金监管工作,持续严厉打击欺诈骗保行为,国家医保局日前印发《医疗保障基金飞行检查管理暂行办法》,将于2023年5月1日起实施。2022年,全国医保系统共检查定点医药机构76.7万家,处理违法违规机构39.8万家,共追回医保资金188.4亿元。2022年,国家医保局组织飞行检查24组次,检查23个省份的定点医疗机构48家、医保经办机构23家,查出涉嫌违法违规资金9.8亿元。
3.全球代谢疾病负担:肥胖每年导致500万人死亡。近日,新加坡国立大学联合美国和中国研究人员在Cell子刊Cell Metabolism上发表的2000-2019年全球疾病负担(GBD)代谢疾病数据显示,所有代谢性疾病的发病率都有所增加,包括高血压、2型糖尿病、高脂血症、肥胖和非酒精性脂肪性肝病(NAFLD)。在代谢性疾病的死亡总体趋势中,肥胖的绝对负担最高,年龄标准化DALY(伤残调整生命年)每年增长0.48%(男性增长0.74%,女性增长0.25%),其次是高脂血症、2型糖尿病、高血压和NAFLD,DALY的趋势相似。2019年,死亡人数最多的肥胖,死亡人数为500万人。
评审动态
1. CDE新药受理情况(03月15日)
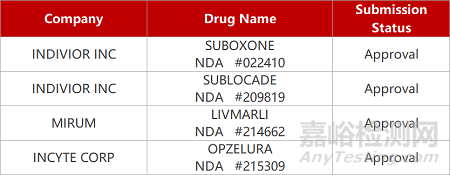
2. FDA新药获批情况(北美03月13日)