今日头条
锐明眼科翼状胬肉新药I期临床积极。苏州锐明新药公司自主研发的RMP-A03滴眼剂针对翼状胬肉适应症的美国I期临床获积极结果。RMP-A03旨在抑制相关靶点介导的通路,达到抑制翼状胬肉新生血管及成纤细胞的形成。在健康成年人受试者中开展的I期临床数据显示,在多次给药剂量递增研究中,该滴眼剂在所有剂量组的安全性和耐受性均良好,试验期间未发生不良事件。
国内药讯
1.歌礼FASN抑制剂痤疮II期临床成功。歌礼制药潜在“first-in-class”口服脂肪酸合成酶(FASN)抑制剂ASC40(Denifanstat)治疗痤疮II期临床达到主要及关键次要终点。与安慰剂相比,ASC40(25mg、50mg、75mg)显著降低患者第12周总皮损计数,降幅分别达到53.1%、61.3%和53.1%(vs34.2%);ASC40在所有剂量下的安全性和耐受性良好,药物相关不良事件发生率与安慰剂相当。
2.奥布替尼治疗MCL临床长期疗效积极。诺诚健华BTK抑制剂奥布替尼治疗复发/难治性套细胞淋巴瘤(MCL)的长期疗效数据发表于Blood子刊上。中位随访为23.8个月时,奥布替尼经IRC评估的总缓解率(ORR)达到81.1%,其中完全缓解(CR)率为27.4%;研究者评估的ORR和CR分别为82.1%和34.9%。中位反应持续时间(DOR)和无进展生存期(PFS)分别为22.9个月和22.0个月,24个月的OS率为74.3%。奥布替尼显示出良好的安全性和耐受性。
3.华东医药引进创新双抗获批SLE临床。华东医药从Provention Bio引进的CD32B/CD79B双抗PRV-3279(HDM3002)获国家药监局临床试验默示许可,拟开展评估用于中重度系统性红斑狼疮(SLE)患者治疗的Ⅱa期临床试验。PRV-3279可同时结合CD32B和CD79B受体,触发对B细胞功能和自身抗体产生的抑制,从而在不引起B细胞耗竭的情况下调节B细胞。目前,该新药正在美国和香港针对SLE开展概念验证IIa期PREVAIL-2研究。
4.康哲VEGF/Ang-2双抗获批眼科临床。康哲药业从武汉友芝友引进的1类生物制品Y400获国家药监局临床默示许可,拟开发用于新生血管性年龄相关性黄斑变性的治疗。Y400是一种抗VEGF/ANG2双抗,拟通过两种不同的通路有效抑制新生血管异常生长。Y400具有亲和力高、抑制活性强、制剂浓度高、稳定性好、给药频率低的优势,可减少患者因频繁的玻璃体腔内注射所造成的潜在风险。
5.九天生物将公布多项基因疗法研究进展。九天生物宣布将在ASGCT年会上公布基因治疗药物SKG0106和SKG0201的临床前研究数据。SKG0106是一款携带编码独特的抗VEGF蛋白的转基因序列的AAV基因疗法,拟通过玻璃体腔注射导入眼内,高效转导视网膜细胞以表达抗VEGF蛋白,以抑制人源VEGF的作用,该产品拟开发治疗新生血管性年龄相关性黄斑变性(nAMD);SKG0201是一款新型的AAV介导的基因替代疗法,包含由独特启动子调控并全面优化的人源SMN1 cDNA,拟开发用于治疗脊髓性肌萎缩症(SMA)。
国际药讯
1.全球首款RSV疫苗获批上市。葛兰素史克开发的呼吸道合胞病毒(RSV)疫苗Arexvy(RSVPreF3 OA/GSK3844766A)获FDA批准上市,成为全球首款获批的RSV疫苗,用于老年人群体预防RSV感染导致的下呼吸道疾病(RSV-LRTD)。在Ⅲ期临床AReSVi-006中,Arexvy的总体疫苗效力为82.6%(96.95% CI:57.9–94.1),对严重RSV-LRTD(定义为至少2种症状)的预防效力为94.1%(95% CI:62.4–99.9);对RSV-A亚型和RSV-B亚型的预防效力一致(84.6%vs80.9%)。
2.礼来Aβ单抗Ⅲ期临床积极。礼来Aβ单抗donanemab在治疗早期症状性阿尔茨海默病Ⅲ期临床(TRAILBLAZER-ALZ 2)达到主要和所有关键次要终点。与安慰剂相比,donanemab治疗显著改善患者的iADRS(综合评估患者认知能力和日常自理能力)评分,患者的临床衰退速度减缓35%,有47%的患者在1年内CDR-SB评分没有衰退(vs29%,p<0.001);患者进展到疾病下一阶段的风险降低39%(HR=0.61;p<0.001)。礼来预计将在本季度向FDA递交其上市申请。
3.恩扎卢胺治疗nmHSPC的Ⅲ期临床积极。辉瑞与安斯泰来合作开发的特异性雄激素受体(AR)抑制剂Xtandi(enzalutamide,恩扎卢胺)治疗非转移性激素敏感性前列腺癌(nmHSPC)的Ⅲ期临床EMBARK最新数据积极。与安慰剂联合亮丙瑞林(leuprolide)相比,Xtandi联合leuprolide治疗和Xtandi单药治疗分别降低患者58%(HR:0.42;95% CI:0.30-0.61;P<0.0001)和37%(HR:0.63;95% CI:0.46-0.87;P=0.0049)的转移或死亡风险;分别降低93%(HR:0.07;95% CI:0.03-0.14;P<0.0001)和67%(HR:0.33;95% CI:0.23-0.49;P<0.0001)的前列腺特异性抗原(PSA)进展风险。药物的安全性与已知研究一致。
4.PPAR⍺拮抗剂联合治疗肝癌早期临床积极。Tempest公司小分子PPAR⍺拮抗剂TPST-1120治疗不可切除或转移性肝细胞癌(HCC)的国际Ib/II期临床结果积极。与阿替利珠单抗和贝伐珠单抗标准治疗方案相比,TPST-1120联合标准治疗方案显著提高患者的客观缓解率(ORR);TPST-1120组未确认的ORR相对改善74.4%(30%vs17.2%),确认的ORR相对改善69.9%(17.5%vs10.3%)。三联疗法安全性数据与对照组一致。
5.新型TCR-T末线治疗实体瘤临床积极。Immatics公司靶向PRAME的T细胞受体(TCR)细胞疗法IMA203(ACTengine®)治疗复发/难治性实体癌的Ib期临床结果积极。在包括皮肤黑色素瘤、卵巢癌、葡萄膜黑色素瘤、头颈癌、滑膜肉瘤在内的接受末线治疗的实体癌患者中,第3个月确证的ORR达到67%(6/9)。中位随访8.5个月时,未达到中位缓解持续时间。临床中没有观察到3级或更高级别细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)。
6.FDA拒批甲状旁腺功能减退症新药上市。Ascendis公司长效甲状旁腺激素前药TransCon PTH(palopegteriparatide)治疗成人甲状旁腺功能减退症(HP)的新药申请(NDA)收到FDA完整回复函。FDA在CRL中对TransCon PTH药品或设备无法保证均一的递送剂量表示担忧,但并未对其临床数据提出异议。在Ⅲ期临床中,TransCon PTH组患者实现不依赖常规治疗并保持血清钙水平在正常范围内的比例较安慰剂组更高(78.7%vs4.8%,p<0.0001)。
医药热点
1.打击骗保专项整治工作启动。近日,国家医保局联合最高人民检察院、公安部等多部门印发《2023年医保领域打击欺诈骗保专项整治工作方案》,要求对“假病人”“假病情”“假票据”等欺诈骗保行为进行重点打击。专项整治工作将从3个方面着力:一是聚焦骨科、血液净化、心血管内科、检查、检验、康复理疗等重点领域;二是聚焦医保结算费用排名靠前的重点药品、耗材,对其基金使用情况予以监测,对其他出现异常增长的药品、耗材等也予以重点关注;三是聚焦虚假就医、医保药品倒卖等行为。
2.郑大一附院高场强MRI介入手术室改建投用。日前,郑大一附院高场强MRI介入手术室改建成功并投入使用。改建后的MRI复合手术室采用高档大空间双室设计,一间是宽敞的主手术室,用于神经外科颅脑手术功能导航与监测;另一间较小是超大孔径的3.0 T磁体扫描探测器停留区的设备间。二者之间由活动的磁场屏蔽门相隔,通过天轨可以使巨大的磁体扫描探测器在几十秒内实现手术室和设备室之间移动传送,从而在手术病人保持不动的情况下完成颅脑手术导航。
3.美国宣布取消国际航空旅客新冠疫苗接种要求。当地时间5月1日,美国白宫宣布将在5月11日取消对联邦雇员、联邦承包商和国际航空旅客的新冠疫苗接种要求。美国也将在5月11日正式结束因新冠疫情而开始的公共卫生紧急状态。据美国CDC统计数据显示,截至4月10日,美国确诊感染新冠病毒病例数超过1.04亿例,死亡病例数超过112万例。
4.中疾控:全国超8成人口已感染过新冠。4月28日,中国疾控中心周报发表《预先计划的研究:新冠疫苗对新冠病毒奥密克戎变异株感染和症状的有效性——中国,2022年12月至2023年2月》。文中推测,2022年12月至2023年2月期间,全国超过82%的人口感染新冠病毒。接种新冠疫苗加强针6个月内,对预防新冠病毒感染和症状方面是有效的。
评审动态
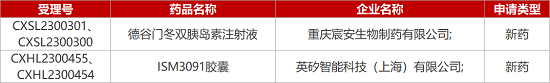
1. CDE新药受理情况(05月04日)
2. FDA新药获批情况(北美05月03日)