您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-12-14 12:11
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.腾盛博药新冠鸡尾酒对奥密克戎有效。腾盛博药新冠中和抗体组合疗法(安巴韦单抗/罗米司韦单抗)在体外嵌合病毒实验中获积极数据。数据显示,安巴韦单抗对抗“奥密克戎”变异株的活性显著下降,但罗米司韦单抗并不受“奥密克戎”变异株所影响;联合疗法保持了对“奥密克戎”的中和活性。具体数据将发布在科学刊物上。目前,FDA正在审核这一联合疗法紧急使用授权申请。
2.信达/驯鹿BCMA CAR-T早期临床积极。信达生物与驯鹿医疗开发的全人源BCMA CAR-T将在ASH2021年会上公布治疗复发/难治性多发性骨髓瘤(RRMM)的最新Ⅰ/Ⅱ期注册性临床数据。79例受试者中,ORR为94.9%,完全缓解/严格意义的完全缓解(CR/sCR)为58.2%;回输后6个月、9个月和12个月的PFS分别为78.0%、76.0%和71.0%。此外在合并髓外MM受试者的ORR为100%,CR/sCR为72.7%。临床中,IBI326的安全性可控。
3.药明巨诺CD19-CAR-T治疗临床数据公布。药明巨诺CD19靶向CAR-T产品瑞基奥仑赛注射液(倍诺达®)将在ASH2021年会上公布用于治疗复发/难治性滤泡淋巴瘤中国成人患者的研究成果。在27例可评估患者中,基于研究者评估的客观缓解率(ORR)达到100%(27/27),最佳完全缓解率(CRR)为92.6%(25/27)。中位随访时间8.84个月,未达到中位缓解持续时间、中位无进展生存期及中位总生存期。
4.科济BCMA CAR-T早期临床积极。科济药业BCMA CAR-T产品CT053将在ASH2021年会上公布治疗复发/难治多发性骨髓瘤患者的Ⅰ/Ⅱ期研究(LUMMICAR-1)积极结果。中位随访13.6个月时,ORR为100%(14/14),其中78.6%的患者达到严格意义的完全缓解(sCR),并且有9例患者持续完全缓解及以上(CR/sCR)超过12个月,92.9%的患者达到非常好的部分缓解(VGPR)及以上。12个月的无进展生存率为85.7%。中位缓解持续时间(mDOR)和中位无进展生存期(mPFS)还没有达到。CT053总体耐受性良好。
5.德琪医药与百时美施贵宝达成临床合作。德琪医药ERK1/2选择性口服抑制剂ATG-017拟联合百时美施贵宝PD-1抑制剂欧狄沃®(纳武利尤单抗)开展一项Ⅰ/Ⅱ期临床研究,评估联合用药治疗晚期实体瘤的安全性、药代动力学和初步疗效。德琪医药公布在SITC2021年会上的临床前研究数据显示,ATG-017联合PD-L1单抗在对免疫检查点抑制剂抗药的小鼠肿瘤模型中达到肿瘤由“冷“至“热”的转化。
国际药讯
1.强生EGFR-MET双抗获欧盟批准上市。欧盟委员会(EC)附条件批准强生旗下杨森EGFR-MET双抗Rybrevant(amivantamab-vmjw)上市,用于治疗携带EGFR外显子20插入突变的晚期非小细胞肺癌(NSCLC)。Rybrevant也是欧盟首个获批治疗这类患者的靶向药。在一项Ⅰ期CHRYSALIS研究中,中位随访12.5个月时,经研究者评估的总缓解率为37%,中位缓解持续时间为12.5个月,其中有64%的病情缓解的患者缓解持续时间≥6个月。
2.新型PI3Kγ抑制剂乳腺癌II期临床积极。Infinity公司口服PI3Kγ抑制剂Eganelisib联合阿替利珠单抗 (Tecentriq)和白蛋白紫杉醇(Abraxane),一线治疗转移性三阴性乳腺癌(TNBC)的II期MARIO-3研究数据积极。中位随访为9.9个月时,在PD-L1阳性和阴性患者中观察到肿瘤缩小的比例分别为92.8%和85.2% ,疾病控制率分别为92.8% 和81.4%,中位PFS分别为11.0个月和7.3个月。与IMpassion 130研究中单独使用atezolizumab和Abraxane报告的数据相比,mPFS分别提高47%和30%。
3.心肌病新药获FDA突破性疗法认定。FDA授予Cytokinetics公司下一代心肌肌球蛋白抑制剂aficamten突破性疗法认定,用于治疗症状性梗阻性肥厚型心肌病(oHCM)。在一项II期REDWOOD-HCM研究中,与安慰剂相比,aficamten治疗组患者10周后平均静息左心室流出道压力梯度(LVOT-G)和Valsalva术后平均LVOT-G较基线显著降低;临床中无aficamten相关严重不良事件和中断治疗事件发生。箕星药业拥有该新药的中国权益。
4.诺华白血病新药Ⅲ期临床新数据积极。诺华STAMP抑制剂Scemblix(ABL001)治疗费城染色体阳性慢性髓性白血病慢性期(Ph+CML-CP)的Ⅲ期ASCEMBL试验新数据积极。公布在ASH2021会上的48周数据显示,Scemblix治疗组主要分子学反应(MMR)与辉瑞博舒替尼治疗组相比提高1倍多(29.3%vs13.2%)、因不良事件导致的停药率低3倍多(7.1%vs25%)。与24周时的数据一致。今年10月,FDA已加速批准Scemblix用于治疗至少经2种TKI治疗的Ph+CML-CP患者。
5.艾伯维JAK1抑制剂新增安全信息。艾伯维宣布更新口服JAK1抑制剂Rinvoq(乌帕替尼)治疗成人中重度类风湿性关节炎(RA)美国处方信息和药物指南。此次更新基于今年9月FDA发布的一份药物安全通讯(DSC)。来自ORAL Surveillance研究的结果显示,Xeljanz(一种JAK抑制剂)与TNF阻断剂相比,使RA患者的主要不良心脏事件(MACE)、恶性肿瘤、死亡、血栓形成的发生率增高。这份DSC以及此次标签更新,适用于经FDA批准用于治疗RA和其他炎症性疾病的全身性用药的JAK类别药物。
6.OncoMyx公司完成新一轮融资。溶瘤病毒免疫疗法公司OncoMyx宣布完成5000万美元的B轮融资。该公司独有的溶瘤病毒平台,运用一种名为粘液瘤病毒的双链DNA(dsDNA)痘病毒作为载体。在临床前研究中,这种粘液瘤病毒免疫疗法单药或与免疫检查点抑制剂联用,显著减缓了多种肿瘤类型的生长。此轮融资将主要用于推进其粘液瘤病毒免疫疗法产品管线,用于治疗实体瘤和血液性恶性肿瘤。
医药热点
1.2021中国肿瘤学大会(CCO)延期召开。12月13日,中国抗癌协会在其官网发布延期举办2021中国肿瘤学大会(CCO)的通知。鉴于近期国内多个地区连续发生本土确诊病例,疫情传播的风险持续增大,2021年CCO大会未能得到河南省相关部门的正式批复,经研究决定,2021中国肿瘤学大会(CCO)将延期至2022年3月底召开,具体召开时间另行通知,会议地点不变。
2.2022年国家下发公卫补助资金588.55亿元。12月3日,国家财政部、国家卫健委联合下发《关于提前下达2022年基本公共卫生服务补助资金预算》的通知。《通知》指出,提前下达2022年基本公共卫生服务补助资金预算指标,共计588.55亿元,较2021年的542.97亿元增加了45.58亿元。其中,西部和中部地区获得公卫补助资金较多。西部、中部和东部地区所分配的补助分别为218.12、245.50、124.93亿元。
3.日本开发出一种抗衰老疫苗。日本顺天堂大学研究人员参与团队开发出一种抗衰老疫苗,在动物实验中成功改善了小鼠与年龄增长相关的病症,还能延长早衰症模型小鼠寿命。这项成果有望用于与年龄增长有关疾病的治疗。相关论文已发表在英国《自然·老化》杂志网络版上。研究团队认为,这一发现将来有可能用于治疗阿尔茨海默病等与年龄增长相关的疾病。
评审动态
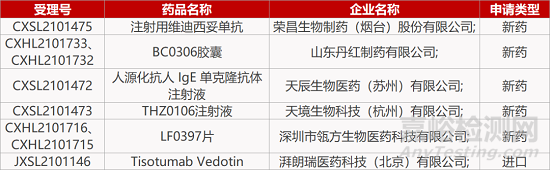
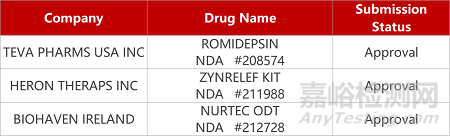

来源:药研发


