您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2023-01-16 12:45
本文适用于按第二类医疗器械管理,与腹腔镜配套使用,供腹腔手术切口闭合的一次性使用微创筋膜闭合器。分类编码:02-15。
一、一次性使用微创筋膜闭合器结构组成与工作原理
一次性使用微创筋膜闭合器(以下简称“筋膜闭合器”)产品通常包括闭合固件(翼式或盾式)和缝线穿引装置(穿引针或抓取器)两部分。闭合固件主要由器身、传动器、近端翼组成。缝线穿引装置主要由头部、杆部和手柄组成,穿引针一般为实心不锈钢针,头部有线槽,抓取器通过手柄操作传递、控制头部工作,头部为钳喙。产品经灭菌,一次性使用。
筋膜闭合器(翼式结构):闭合固件通过微创口进入腹腔内,张开近端翼后形成支撑;由缝线穿引装置,将缝合线通过闭合固件上的导引孔经出线口由腔外带入腔内,缝合线两端线头分别夹持于近端翼两侧的夹持块上,收拢近端翼抽出闭合固件,将缝合线头端带出腔外,线头打结后即可实现缝合。
筋膜闭合器(盾式结构):将缝合线预先缠绕于闭合固件的近端翼(闭合固件为非张开状态),通过微创口进入腹腔内,张开近端翼后形成支撑;缝线穿引装置通过闭合固件上的导引孔由腔外进入腔内,将缝合线从近端翼上夹取带出腔外,收拢闭合固件,线头打结后即可实现缝合。
产品常见结构示意图如下:
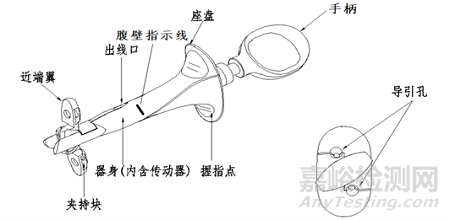
图1 闭合固件(翼式)
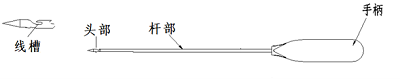
图2 缝线穿引装置(穿引针)
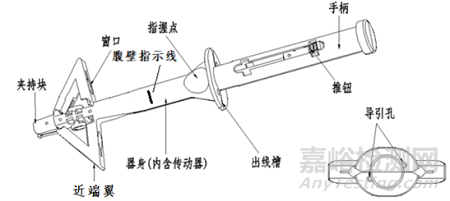
图3 闭合固件(盾式)

图4 缝线穿引装置(抓取器)
注:示意图仅说明筋膜闭合器的结构,并非唯一型式。
二、一次性使用微创筋膜闭合器主要风险
根据YY/T 0316《医疗器械风险管理对医疗器械的应用》附录E表E.2初始事件和环境示例,对筋膜闭合器已知或可预见的风险进行判定,产品在进行风险分析时至少应包括以下的主要危害(见表1),开发人还应根据自身产品特点确定其他危害。
表1 产品的主要风险
|
风险类别 |
具体示例 |
|---|---|
|
设计不当风险 |
机械系统设计不当,闭合固件或缝线穿引装置各部分连接强度不足,使用过程中出现断裂、支撑性不足等情况; 机械系统设计不当,闭合固件或缝线穿引装置灵活性不足,产品卡涩无法满足使用要求; 穿引装置头部设计不当,造成头部断裂、刺穿力不足等情况; 夹持块掉屑或脱落; 标识不完全,指引性不足造成产品临床使用不当或损坏。 |
|
生物相容性风险 |
选用不适当的材料; 灭菌未确认或未按已确认的参数灭菌; 包装不符合要求或老化; 未能按运输储存要求对产品进行防护,造成产品破损,污染产品; 超过有效期使用; 产品零件生锈; 未按要求对生产环境进行控制; 零部件未按要求清洗; 清洗用水不符合要求。 |
|
制造过程风险 |
零部件要求不明确,采购不当; 零部件加工精度不当,装配调整不当; 加工助剂使用不当; 不合格品未被识别; 包装不当; 灭菌有效性未被充分确认/验证。 |
|
运输和贮藏风险 |
防护不当,造成包装破损、产品污染; 防护不当,造成缝线穿引装置头部受损; 贮存环境不当。 |
|
处置和废弃风险 |
未提供信息或提供信息不充分; 未按规定要求处置。 |
|
使用风险 |
未明示应由经培训的专业人员使用; 包装标记不当,可能产生重复使用的危害,引起交叉感染; 不完整的使用说明书,造成操作错误; 性能特征不恰当的描述,造成错误使用; 不适当的预期使用规范,造成错误使用; 操作说明书的遗失,造成错误使用; 使用者未按规范程序使用; 使用过程中打结不牢。 |
|
其他风险 |
同缝合线配合使用时,缝合线损伤、断裂或无法被顺利夹持。 |
三、一次性使用微创筋膜闭合器性能研究实验要求
1.主要性能指标
通常应考虑(但不限于)以下性能指标:
1.1 外观
1.2 基本尺寸
1.3 模拟使用性能
1.4 物理性能
1.4.1 各组件间连接牢固性
1.4.2 表面粗糙度
1.4.3 硬度、韧性、针尖强度(穿引针适用)
1.4.4 刚性、韧性(抓取器适用)
1.4.5 刺穿力
1.5 金属部件的耐腐蚀性能
1.6 无菌
1.7 化学性能
根据不同材料特性、生产工艺,结合实际情况制定化学性能要求。具体开展的项目包括:外观(浊度、色泽)、酸碱度、重金属、还原物质、蒸发残渣、紫外吸光度。
1.8 环氧乙烷残留量(若适用)
2.化学和物理性能研究
应当开展产品化学和物理性能研究,确定包括有效性、安全性指标以及与质量控制相关的其他指标的确定依据,所采用的标准或方法、采用的理由及理论基础。应根据产品的结构特征、预期用途,开展相应的研究,如刺穿力。
3.生物相容性评价研究
预期与人体直接或间接接触的部分,均需要进行生物相容性评价,必要时进行生物学试验。生物相容性评价应包括:
(1)生物相容性评价的依据和方法。
(2)产品所用材料及与人体接触的性质。
(3)实施或豁免生物学试验的理由和论证。
(4)对于现有数据或试验结果的评价。
本产品属于短期外部接入组织产品,目前根据GB/T 16886《医疗器械生物学评价》系列标准,需考虑的生物学评价试验项目应包括但不限于:细胞毒性、致敏、皮内反应。
4.灭菌工艺研究
明确用于保证产品无菌的质量保证体系,明确灭菌工艺(方法和参数)和无菌保证水平(SAL)。筋膜闭合器的无菌保证水平(SAL)需达到10-6。进行灭菌确认,确认内容应符合GB 18279《医疗保健产品灭菌环氧乙烷》系列标准、GB 18280《医疗保健产品灭菌辐射》系列标准等标准的规定。若灭菌使用的方法容易出现残留,应当开展研究明确残留物信息及采取的具体处理方法和条件。
5.产品货架有效期和包装研究
货架有效期验证试验应采用与常规生产相同的终产品进行。加速稳定性试验方案设计参考标准YY/T 0681.1《无菌医疗器械包装试验方法第1部分:加速老化试验指南》进行,其中“室温或环境温度(TRT)”应选择能代表实际产品储存和使用条件的温度。验证项目包括产品自身性能验证和包装系统性能验证两方面。前者需选择与医疗器械货架有效期密切相关的物理、化学检测项目,涉及产品生物相容性可能发生改变的,还需进行生物学评价。后者包括包装完整性、包装强度和微生物屏障性能等验证项目。其中,包装完整性验证项目可包括在设定的时间间隔点目力检测产品包装(是否污染、破损等)及标签(完整性、粘附牢固度、印刷内容清晰度等)、泄漏试验等,包装强度测试项目包括软性屏障材料密封强度试验、无约束包装抗内压破坏试验和模拟运输试验等。
6.其他研究
结合产品的特点,开展证明产品安全性、有效性的其他研究。

来源:嘉峪检测网


