今日头条
和铂FcRn抗体重症肌无力Ⅲ期临床成功。和铂医药宣布FcRn抗体巴托利单抗治疗全身型重症肌无力(gMG)的Ⅲ期临床达到主要终点和关键次要终点。在IIa期临床中,与安慰剂组相比,HBM9161组患者重症肌无力日常生活 (MG-ADL) 量表平均改善3.8分 (p=0.029),重症肌无力复合 (MGC) 量表平均改善8.0分 (p=0.006)。此前,该新药用于gMG适应症已被CDE纳入突破性治疗品种。
国内药讯
1.正大天晴PD-1/TGFβ双抗启动Ib/II期临床。正大天晴1类新药TQB2868注射液登记启动一项Ib/II期临床,拟评估用于治疗晚期肝细胞癌受试者中的初步疗效与安全性。TQB2868为一款PD-1/TGFβ双抗。国内同靶点新药君实生物的JS201注射液和维立志博的注射用LBL-015已在临床开发中。值得一提的是,正大天晴是国内唯一同时布局PD-1/TGFβ(TQB2868)和PD-L1/TGFβ(TQB2858)双抗的创新药企。
2.福贝“渐冻人症”新药启动I期临床。福贝生物拟开发用于治疗肌萎缩侧索硬化(ALS,俗称“渐冻人症”)的小分子CSF-1R抑制剂FB-1071在复旦大学附属华山医院正式启动I期临床。该项研究由华山医院张菁教授担任主要研究者,拟评价FB-1071单次给药剂量递增的安全性、药代动力学/药效动力学特征,同期进行食物影响评价、药物-药物相互作用评价以及代谢产物的鉴定。
3.海雁双腺苷受体抑制剂获批临床。海雁医药1类化药YZJ-5053片获国家药监局临床试验默示许可,拟定适应症为:经标准治疗后或在治疗中发生肿瘤进展,或目前无标准治疗可用、已不适合接受根治性治疗的晚期/转移性实体瘤。YZJ-5053是一款双腺苷(A2aR/A2bR)靶点受体抑制剂,已在临床前研究中显示出与PD-1/PD-L1抑制剂类药物联用具有协同增效作用,在多个小鼠肿瘤模型中观察到免疫联合治疗作用下的肿瘤消退现象。去年8月,该新药已在美国获批临床。
4.阿斯利康心血管疾病新药在华报IND。阿斯利康1类生物制品AZD3427注射用浓溶液的临床试验申请获CDE受理。AZD3427是一款松弛素模拟物(内源性异二聚胰岛素样肽),可通过增强内皮介导的血管舒张机制、促进心血管系统中的心脏保护和抗纤维化作用,对心脏和血管产生有益作用。该新药目前正在海外针对心力衰竭和肺动脉高压患者开展一项Ⅱ期临床研究,评估AZD3427治疗24周后降低患者肺血管阻力的能力。
5.香雪生命科学TCR-T疗法报新IND。香雪生命科学1类生物制品TAEST16001注射液的临床试验申请获CDE受理。TAEST16001是一款NY-ESO-1抗原特异性高亲和性T细胞受体转导的TCR-T细胞治疗产品,针对的靶点是HLA-A*02:01及NY-ESO-1抗原肽组成的复合物,使用无自我复制能力的慢病毒转导自体T细胞,表达NY-ESO-1抗原特异性的TCR。2019年3月,该新药已首次获CDE批准开展临床。
国际药讯
1.拜耳达罗他胺获欧盟批准新适应症。拜耳口服雄激素受体抑制剂达罗他胺获欧盟委员会批准新适应症,联合雄激素剥夺疗法(ADT)与多西他赛治疗转移性激素敏感性前列腺癌 (mHSPC) 患者。在III期ARASENS研究中,与安慰剂联合ADT和多西他赛相比,达罗他胺联合ADT与多西他赛治疗可使mHSPC患者的死亡风险显著降低32.5%。此前,达罗他胺已获批治疗非转移性去势抵抗性前列腺癌患者。
2.强生PARP抑制剂联合用药报NDA。强生旗下杨森PARP抑制剂niraparib的新药申请(NDA)获FDA受理,联合醋酸阿比特龙以及强的松,用于治疗BRCA阳性的转移性去势抵抗性前列腺癌(mCRPC)患者。在III期MAGNITUDE研究中,联合治疗显著延长HRR(同源重组修复)阳性患者的影像学无进展生存期(rPFS)(16.5vs13.7个月;HR=0.73)和BRCA1/2突变患者的rPFS(16.6vs10.9个月;HR=0.53)。
3.Verrica创新皮肤病药械组合报NDA。Verrica公司重新提交的药械组合VP-102(商品名Ycanth)的新药申请(NDA)获FDA受理,用于治疗传染性软疣。PDUFA日期为2023年7月23日。VP-102包含蛋白磷酸酶2A抑制剂斑蝥素(0.7%溶液),通过一次性涂抹器局部给药。软疣是一种具有高度传染性的常见病毒性皮肤病,主要感染对象为儿童等免疫力低下的人群。
4.创新庞贝病口服疗法Ⅰ期临床积极。Maze公司针对庞贝病适应症开发的新型口服糖原合成酶1(GYS1)抑制剂MZE001在健康受试者中开展的Ⅰ期临床获积极结果。MZE001旨在抑制庞贝病的致病原因——糖原累积。研究人员使用了一种新型生物标志物——外周血单核细胞(PBMC)糖原对MZE001在受试者中的疗效进行评估。结果显示,MZE001各剂量水平下PBMC糖原呈暴露依赖性降低;每日两次720 mg的剂量下耐受良好。
5.阿尔茨海默症激越复方暂缓报NDA。Axsome公司在2022年财报中透露,由于FDA顾虑复方片剂AXS-05(右美沙芬+安非他酮)治疗阿尔茨海默病患者激越症状的用药安全,该公司计划在完成ADVANCE-2研究和开放标签安全扩展试验后,再向FDA提交AXS-05的上市申请。去年11月,AXS-05已在Ⅲ期研究(ACCORD)中达到主要和次要终点,使患者激越症状复发风险下降3.6倍(HR:0.275,p=0.014)。ADVANCE-2研究预计2024年上半年完成。
6.阿替利珠单抗联合卡博替尼肾癌III期临床失败。Exelixis公司酪氨酸激酶抑制剂卡博替尼联合罗氏PD-L1单抗阿替利珠单抗治疗局部晚期或转移性透明细胞或非透明细胞肾细胞癌(RCC)的III期CONTACT-03研究未达到无进展生存期(PFS)主要终点。与卡博替尼相比,联合疗法未能显著改善患者PFS。研究中,组合疗法的安全性与每种单药的已知安全情况一致,没有发现新的安全信号。
7.阿斯利康加码罕见病领域。日前,阿斯利康宣布在加拿大成立一个新的罕见病发展中心,该中心将专注于罕见病研究。此举将进一步强化阿斯利康在加拿大密西沙加市的研发业务,并预计将增设500个高技术工作岗位。该中心的临床研究覆盖乳腺癌、肺癌、前列腺癌、肺炎和慢性肾病等多个治疗领域。
医药热点
1.安徽省再添一家大型公立医院。安徽省发改委在官网就《首都医科大学附属北京安贞医院安徽医院项目可行性研究报告(代项目建议书)》日前进行审批前公示。根据披露的信息,首都医科大学附属北京安贞医院安徽医院建设地点位于合肥市高新技术开发区皖水路与文曲路交口西北角;建设单位为安徽医科大学第一附属医院;建筑面积约14.5万平方米。项目估算总投资14.96亿元。
2.国家集采价格管理文件出台。3月1日,国家医保局发布《关于做好2023年医药集中采购和价格管理工作的通知》,要求进一步完善医药价格形成机制,促进医保、医疗、医药协同发展和治理。在推进医疗服务价格改革和管理方面,通知明确唐山、苏州、厦门、赣州、乐山5个国家试点城市要监测首轮调价运行情况,持续完善价格形成机制。
3.新加坡新冠超额死亡5000多人。3月3日,新加坡公布新冠疫情期间最新超额死亡数据,本次报告涵盖的时间范围为2020年1月至2022年12月。数据显示,三年疫情期间,平均全因死亡为每10万人有555.7人,而疫情之前的四年平均只有549.1。换算到超额死亡率,疫情三年期间每年每十万人超额死亡30.7人。按人口570万计算,三年新冠疫情期间,新加坡出现大约5250起超额死亡,包括直接死于冠病的以及间接死亡的,如疫情管控造成的次生伤亡。
评审动态
1. CDE新药受理情况(03月06日)
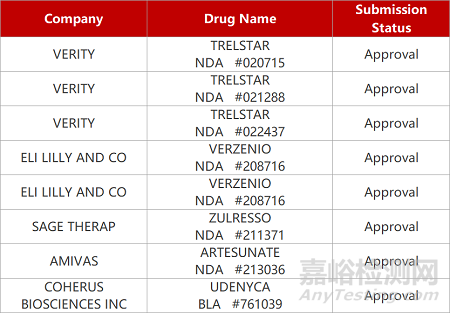
2. FDA新药获批情况(北美03月04日)