今日头条
通化金马口服AD新药III期研究积极。通化金马药业1类化药琥珀八氢氨吖啶片用于治疗轻、中度阿尔茨海默病的III期临床达到主要终点。琥珀八氢氨吖啶片是一种新的乙酰胆碱酯酶抑制剂,具有双重胆碱酯酶抑制功能,可以同时抑制乙酰胆碱酯酶和丁酰胆碱酯酶。结果显示,琥珀八氢氨吖啶片对AD评定量表认知部分(ADAS-cog)的改善具有显著的临床意义;治疗组不良事件及不良反应的发生率均低于两个对照组。
国内药讯
1.诺华预防偏头痛新药中国获批上市。诺华与安进开发的CGRP抑制剂依瑞奈尤单抗(Erenumab)注射液获国家药监局批准上市,用于预防成人偏头痛。在III期DRAGON研究中,Erenumab(70mg)治疗显著降低患者每月偏头痛天数(MMD);Erenumab(70mg)组每月偏头痛天数相比基线减少50%以上的应答率显著高于安慰剂组。2018年5月,Erenumab获得FDA批准上市,成为全球首个CGRP抑制剂。
2.AZ奥希替尼新适应症在华报产。阿斯利康第三代EGFR抑制剂奥希替尼新适应症上市申请获CDE受理。今年5月,奥希替尼联合化疗治疗EGFR突变非小细胞肺癌(NSCLC)的III期Flaura2研究已取得积极结果。与奥希替尼单药相比,研究者和BICR评估的奥希替尼联合化疗将患者中位PFS分别延长8.8个月和9.5个月。此前,该新药针对NSCLC患者已获NMPA批准三项适应症。
3.亚虹宫颈癌药械组合III期临床积极。亚虹医药用于非手术治疗宫颈高级别鳞状上皮内病变(HSIL)的光动力药械组合产品APL-1702的国际III期临床达到主要研究终点。APL-1702是集药物和器械为一体的光动力治疗产品,有望为HSIL患者提供非创伤性的新治疗选择,免除手术治疗的痛苦和副作用。详细数据将在学术会议及期刊上公布。
4.云顶新耀创新抗生素组合拟纳入优先审评。云顶新耀注射用盐酸头孢吡肟/注射用盐酸他尼硼巴坦组合包装获CDE拟纳入优先审评,用于治疗包括肾盂肾炎的成人复杂性尿路感染(cUTI)。在III期临床CERTAIN-1中,与美罗培南相比,该组合达到临床和微生物学应答的患者比例具有优效性(70.0%vs58%)。今年8月,FDA已受理该组合的新药上市申请(NDA) 并授予优先审评资格,PDUFA日期为2024年2月22日。
5.云顶新耀引进一款肾病药物。云顶新耀宣布与Kezar Life Sciences就后者已处于Ⅱ期临床开发的选择性免疫蛋白酶体抑制剂药物zetomipzomib达成合作许可协议,获得zetomipzomib在大中华区、韩国和部分东南亚国家的临床开发和商业化权益。zetomipzomib主要治疗包括狼疮性肾炎(LN)在内的系列自身免疫性疾病。根据协议,Kezar将获得700万美元的预付款,可能达1.325 亿美元的开发、监管和商业化里程碑后期付款,以及产品的销售分成。
国际药讯
1.辉瑞JAK3抑制剂获欧盟批准上市。辉瑞口服特异性JAK3/TEC抑制剂Ritlecitinib(商品名:Litfulo,利特昔替尼胶囊)获欧盟委员会(EC)批准上市,用于治疗12岁及以上重度斑秃患者。在IIb/III期ALLEGRO研究中,24周治疗结果显示,Ritlecitinib(50mg)较安慰剂使患者达到头皮实现毛发覆盖率≥90%的比例更高(13.4%vs1.5%)。今年6月,该新药已在美国批准上市,用于治疗12岁及以上青少年和成人斑秃。
2.右美沙酮抑郁症长期疗效积极。Relmada公司新型NMDA受体通道阻断剂REL-1017(右美沙酮)治疗重度抑郁症(MDD)的Ⅲ期扩展REL-1017-310研究结果积极。与基线平均(33.8分)相较,REL-1017治疗导致患者MADRS总分获得改善,第7天为11.3分,第1个月为16.8分,第3个月和第6个月为19.9分,第12个月为22.5分;这四个时间点达到MADRS总分改善≥50%的患者比例分别为26.6%、51.0%、60.7%、63.4%与77.2%。1年期间未检测到新的安全性信号。
3.明尼苏达大学NK细胞早期临床积极。美国明尼苏达大学的研究人员使用IL-15和烟酰胺联合单克隆抗体体外扩增的自然杀伤细胞用于过继转移治疗复发或难治性非霍奇金淋巴瘤和多发性骨髓瘤患者的Ⅰ期临床结果积极。在19例晚期非霍奇金淋巴瘤患者中,13例患者表现出完全缓解,1例患者部分缓解,总有效率达到74%。在血液、骨髓和肿瘤组织中检测到转移后的NK细胞长达14天,并保持良好的代谢特征。
4.首款自体TIL疗法上市被延期。FDA由于自身的资源限制,延长了Iovance公司肿瘤浸润淋巴细胞(TIL)疗法Lifileucel用于治疗晚期黑色素瘤患者的生物制剂许可申请(BLA)的优先审查时间,PDUFA日期由今年11月25日延长至2024年2月24日。FDA表示没有重大审查问题,也没有召开咨询委员会会议的计划。目前,对临床场所的所有批准前检查,内部和外部制造和测试设施已成功完成。
5.罗氏与Orionis合作开发分子胶药物。罗氏旗下基因泰克与Orionis Biosciences将利用后者专有Allo-Glue小分子技术平台,针对基因泰克指定靶点,联合开发分子胶类创新药。Allo-Glue分子诱导的相互作用可导致靶蛋白被细胞的天然蛋白质处理机制降解、抑制或改变功能。根据协议,Orionis将获得4700万美元的预付款,可能超过20亿美元的开发和商业化里程碑潜在付款,以及产品销售的分级特许权使用费。
6.德国默克逾12亿美元布局AI药物开发。德国默克与BenevolentAI公司将利用后者端到端AI平台技术,聚焦于肿瘤学、神经病学和免疫学三个靶点,合作开发新型候选药物。根据协议,BenevolentAI将获得高达5.94亿美元的款项,包括预付款以及发现、开发和商业等里程碑款项。默克同时也与Exscientia公司达成AI药物发现合作。根据协议,Exscientia将获得2000万美元的现金预付款,总额高达6.74亿美元的发现、开发、监管和销售里程碑付款。
医药热点
1.大连医科大学二院儿童血液肿瘤诊疗中心成立。9月19日,大连医科大学附属第二医院正式成立儿童血液肿瘤诊疗中心,以多学科协作(MDT)为基础,旨在为儿童血液病及肿瘤性疾病等疑难病例提供化疗、放疗、手术、造血干细胞移植治疗及护理一体化诊疗服务。中心开展包括儿童白血病、再生障碍性贫血、血小板减少症、淋巴瘤、髓母细胞瘤、神经母细胞瘤以及儿童先天免疫缺陷病及遗传代谢性疾病等罕见病的诊治工作。
2.JAMA:久坐可显著增高痴呆症风险。来自亚利桑那大学和亚利桑那阿尔茨海默病研究中心的Alexande教授团队在《美国医学会杂志》(JAMA)发表的一项研究论文表明,老年人久坐时间越长,特别是每天久坐10小时及以上,发生全因痴呆症的风险就越高。数据显示,相比于久坐行为中平均9.27h/d的受试者,平均10h/d、12h/d和15h/d的受试者痴呆症风险分别升高了8%、63%和221%。久坐行为中平均9.27h/d、10h/d、12h/d和15h/d的痴呆症发病率分别为7.49/1000人-年、8.06/1000人-年、12/1000人-年和22.74/1000人-年。
3.日本便当食物中毒者增至约300人。20日,日本青森县八户市保健所发布消息称,由当地便当公司“吉田屋”引发的大规模食物中毒事件,已有295人出现症状,涉及范围增至1都23县。据报道,“吉田屋”为八户当地的一家便当生产厂家,涉事这批便当主要食材为海鲜,保质期到9月16日和17日。这批便当在东北和关东地区的超市、大型活动和车站售出后,大量消费者出现不同程度的腹泻和呕吐症状。
评审动态
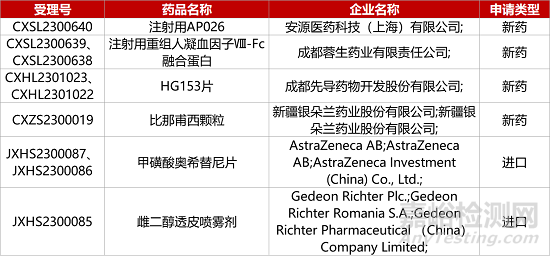
1. CDE新药受理情况(09月21日)
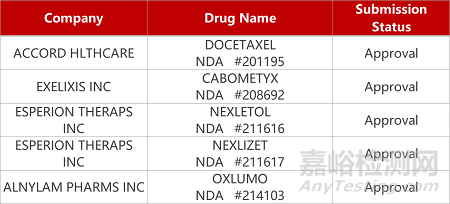
2. FDA新药获批情况(北美09月20日)