您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-06-20 12:27
助听器是由传声器、放大器和耳机组成,并由电池供电,用来放大声音、补偿听力损失的电子装置。根据《医疗器械分类目录》,该类设备按第二类医疗器械管理,分类编码为19-01-07,包括耳背式助听器、耳内式助听器、盒式助听器、骨传导式助听器。
一、助听器的结构组成和工作原理
1、结构组成
助听器一般由输入换能器、信号调理单元、输出换能器、电源(不可充电电池或内置充电电池)、耳模(耳塞)、附件(如有)和软件(如有)组成。附件可由电池充电器(如有)、导线、导声管等组成。
输入换能器一般由传声器(麦克风或话筒)、磁感线圈等组成。传声器的作用是将输入的声能转为电能传至信号调理单元;磁感线圈的作用是接受磁感应信号并转换成电能传至信号调理单元。
信号调理单元一般由放大器、信号处理器组成。信号调理单元可以使用模拟放大电路,将电信号放大;或者将输入信号进行A/D转换后,利用数字信号处理器进行一系列处理、放大。信号调理单元将电信号进行处理放大后传至输出换能器。
在输出换能器方面,气导式助听器和骨传导式助听器有明显的区别。气导式助听器的输出换能器一般为耳机和受话器。耳机将放大的电信号转换成声信号后传入耳道。常见的有盒式、耳背式、耳内(耳甲腔)式、耳道式。骨传导式助听器的输出换能器则是骨振器。骨振器将放大的电信号转换成机械能后,通过振动颅骨把动能信号传到耳蜗。骨振器一般放在乳突等部位。
图示举例如下:

图1 盒式助听器



图2 耳背式助听器

图3 耳内(耳甲腔)式助听器、耳道式助听器
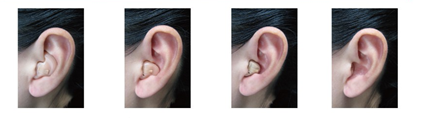
图4不同的助听器佩戴效果图

图5 眼镜式助听器
2、工作原理
助听器实质是一放大器,它将声音以某种方式放大,使听力损失者能以一定方式有效地利用其残余听力。目前的数字助听器技术对声音信号进行放大之余,还能实现频率压缩、噪声抑制等功能。
声音传到内耳有气导和骨传导两种机制,正常情况下气导起主要作用。从传导途径上看,气导机制是振动的声波被耳廓收集,经外耳道、中耳最后传入内耳;骨传导机制是声波转换后的机械振动沿颅骨传至内耳。
听力损失按照病变性质分为传导性听力损失、感音神经性听力损失、混合性听力损失。传导性听力损失主要是外耳和中耳病变所致(如鼓膜穿孔),一般骨导听力正常,气导听力下降。感音神经性听力损失是耳蜗毛细胞、听神经或听中枢等部位发生障碍所致,大多表现为气导和骨导听力一致性下降。混合性听力损失既有传导性的病因,又有感音神经性的病因存在,一般气导和骨导听力均下降,但气导听力下降更明显。
因助听器的主要作用是将声音以某种方式放大,使听力损失者能以一定方式有效地利用其残余听力。所以无论是气导式助听器还是骨传导式助听器,当放大后的信号能被患者的残余听力(包括气导听力、骨传导听力)所利用,助听器就能起到听力补偿的作用。
二、助听器的主要风险
助听器的危害清单见表
表 危害清单
|
危害类型 |
形成因素 |
|
|---|---|---|
|
能量危害 |
电磁能 |
可触及金属、外壳、应用部分等与带电部分隔离/保护不够,电介质强度不够,可能对使用者或患者造成电击危害 |
|
产品外壳、应用部分绝缘/隔离不够,可能引起过量漏电流伤害使用者或患者 |
||
|
抗电磁干扰能力差、特定环境下工作不正常,或干扰其他设备正常工作 |
||
|
热能 |
可触及的外壳温度过高,可能引起使用者或患者烫伤 |
|
|
机械能 |
产品外壳机械强度和刚度不足,佩戴固定件不牢固,产品面、角、边粗糙,都可能对使用者或患者造成机械损伤 |
|
|
坠落导致机械部件松动、或导致元器件损坏,造成输出异常 |
||
|
生物学和化学危害 |
生物学和 化学危害 |
产品清洁或消毒不完全、一次性使用的配件重复使用等现象,可能会使患者耳道感染,细菌、病毒等进入患者体内 |
|
使用清洗剂或消毒剂的残留物导致的化学危害; 长时间不使用的电池未经取出,导致电池漏液引发的危害等 |
||
|
生物相容性 |
产品直接与患者接触的组件,接触材料应进行生物相容性评价 |
|
|
操作危害 |
不正确的 输出 |
验配前未经专业检查及测试,导致选配不当 |
|
使用时声能输出过大导致患者的听力损害 |
||
|
使用错误 |
日常使用、维护、校准未按规定进行,导致产品偏离正常使用状态 |
|
|
信息危害 |
不适当的标记 |
标记缺少或不正确,标记的位置不正确,不能被正确的识别,不能永久贴牢和清楚易认等 |
|
不完整的说明书 |
说明书中对产品性能特征、预期用途、使用限制等描述不规范、不完整,导致产品的非预期或超范围使用 |
|
|
不适当的操作说明 |
未规定验配前应进行专业听力测试 |
|
|
日常使用、维护、校准规定不明确、不适当 |
||
|
警告 |
未对一次性使用附件可能再次使用的危害作出适当的警告 |
|
三、助听器性能研究实验要求
1.化学和物理性能研究
助听器通常与编程器、验配软件联合使用,开展联合使用安全有效的研究,包括验配流程(验配软件名称、软件版本及验配公式)、联合使用风险及控制措施、联合使用上的限制,兼容性研究等。
2.软件研究
应按照《医疗器械软件注册审查指导原则(2022年修订版)》开展软件研究(含现成软件研究、互操作性研究、GB/T 25000.51-2016自测等),安全性级别通常为中等。
若具备电子数据交换、远程访问与控制、用户访问三种功能当中一种及以上功能,需按照《医疗器械网络安全注册审查指导原则(2022年修订版)》开展网络安全研究,安全性级别通常为中等。
3.生物学特性研究
应对产品结构组成中与患者和使用者接触部分的生物相容性进行评价。助听器预期与患者接触的部件主要是外壳、耳模、耳塞,按照GB/T 16886.1标准的要求,生物相容性评价应至少考虑以下方面的要求:细胞毒性、致敏反应、刺激或皮内反应。
4.清洁、消毒、灭菌研究
助听器一般为单用户重复使用产品,由用户进行清洁消毒。应当明确推荐的清洗和消毒工艺(方法和参数)的确定依据并进行验证。
5.稳定性研究
可参考《有源医疗器械使用期限注册技术审查指导原则》要求,开展产品使用期限的研究。助听器是精密的电子产品,有效期应重点考虑使用环境(包括外部环境及患者耳道环境,如温湿度等)对元器件老化的影响。
开发人应在声称的储运条件下开展包装和环境试验研究,证明在运输和环境测试后产品仍能保持其完整性和功能性。助听器应参照GB/T 14199开展产品环境试验研究。含有源附件(如充电器)的,还应参照GB/T 14710开展环境试验研究。
6. 证明产品安全性、有效性的其他研究
耳背式助听器、耳内式助听器(包括耳甲腔式和耳道式助听器)、盒式助听器产品属于列入《免于临床评价医疗器械目录(2023年)》中的产品,可参考《列入免于临床评价医疗器械目录产品对比说明技术指导原则》开展等同性论证。

来源:嘉峪检测网


