您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-10-09 08:19
一、背景
2024年9月19日,韩国大化制药公司开发的紫杉醇口服溶液(产品代号:DHP107;研发代号:RMX3001) 获得国家药品监督管理局(NMPA)批准在中国上市,用于一线含氟尿嘧啶类方案治疗期间或治疗后出现疾病进展的晚期胃癌患者的治疗。该紫杉醇口服溶液作为全球首款成功开发并批准上市的口服紫杉醇产品,具有里程碑意义。
长久以来,紫杉醇口服给药备受胃肠道吸收不佳的困扰。这是由于多种因素造成的,其最主要的原因包括药物被细胞色素P450(CYP)酶系代谢,以及肠道上皮细胞和肝脏中存在的外排系统,如P-糖蛋白(P-glycoproteins)的作用,这些机制共同降低了紫杉醇在口服后的生物利用度。
在紫杉醇口服溶液上市之前,市场上紫杉醇制剂仅以注射剂形式存在,需在医院内通过配制后,以静脉滴注的方式给药,这要求患者频繁就诊,并可能伴随注射部位的不良反应。鉴于这些不便,开发紫杉醇的口服制剂一直是制药行业研究的重点方向。大化制药凭借其创新的脂质自乳化药物递送技术,成功研制出了紫杉醇口服制剂,并于2016年9月9日顺利获得韩国食品药品安全管理部(Ministry of Food and Drug Safety,MFDS)的上市许可(产品处方组成如表1所示)。
表1 DHP107紫杉醇口服溶液处方组成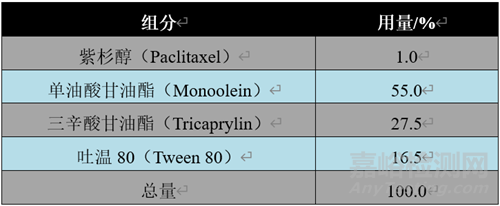
二、制剂开发
大化制药紫杉醇口服制剂开发的思路来源于一个偶然的发现。2005年,S. J. Lee等人发现含单油酸甘油酯的紫杉醇脂质制剂(单油酸甘油酯/三辛酸甘油酯/吐温80)在膀胱癌的膀胱内给药治疗中对药物的吸收效果有积极的影响,单油酸甘油酯能显著增强紫杉醇与膀胱粘膜的生物粘附性,从而增加紫杉醇在膀胱组织中的滞留和渗透。另外有研究表明单油酸甘油酯在口服给药中能够增强小分子甚至蛋白质通过上皮细胞的吸收。但其具体的吸收增强机制尚不完全清楚,目前已有包括纳米孔诱导或膜扰动以及肠道中形成的中间相等多个假说。也有体外研究表明,单油酸甘油酯可以通过抑制P-糖蛋白来增强药物的细胞吸收。
在S. J. Lee等人研究的基础上,研究团队进一步开发了含单油酸甘油酯、饱和甘油三酯和乳化剂的紫杉醇口服脂质制剂。选择单油酸甘油酯作为主要成分是因为其具有高生物粘附性以及潜在的口服吸收促进作用,加入甘油三酯则是因为它们对紫杉醇有很好的溶解度。
研究者选择了三乙酸甘油酯、三丁酸甘油酯、三己酸甘油酯、三辛酸甘油酯、三癸酸甘油酯、三月桂酸甘油酯作为候选的甘油三酯辅料,并考察了使用不同甘油三酯制备的紫杉醇口服制剂在小鼠口服后的药代动力学特性。这些制剂按照紫杉醇:单油酸甘油酯:甘油三酯:Tween 80 = 1.0: 55.0: 27.5: 16.5(重量比)的比例制备,并以50 mg/kg的剂量给予小鼠。结果显示,含有三己酸甘油酯、三辛酸甘油酯和三癸酸甘油酯的配方比其他配方具有更高的暴露量,AUC值分别为12.1± 2.6、8.9±1.8和8.4±2.7 μg·h/mL,且这些值之间在统计学上没有显著差异。相比之下,三乙酸甘油酯、三丁酸甘油酯和三月桂酸甘油酯组的AUC值较低,分别为1.6±0.5、5.4±0.7和4.9±1.6 μg·h/mL,且这些值与三己酸甘油酯组的AUC值有统计学上的显著差异。但是,虽然含三己酸甘油酯的处方在AUC值上表现出色,但基于该辅料安全性信息,三辛酸甘油酯的毒性远低于三己酸甘油酯。因此,出于安全性的考虑,研发团队最后选择了紫杉醇/单油酸甘油酯/三辛酸甘油酯/吐温80的处方配方进行后续实验,因为该配方在提供相似药物暴露量的同时,具有更低的毒性风险。
研发人员还比较了吐温80对紫杉醇口服吸收的影响,当给予不含Tween 80的制剂(紫杉醇:单油酸甘油酯:甘油三酯= 1.0: 66.0: 33.0)时,AUC降低到了6.3 μg·h/mL,仅为含有Tween 80制剂(DHP107)的约56%。这表明,Tween 80的加入能够显著增加紫杉醇口服后的体内暴露量。
研究人员还制备了一系列不同载药量的紫杉醇口服制剂,处方中保持了单油酸甘油酯、三辛酸甘油酯和吐温80的质量比恒定为55.0:27.5:16.5,唯一改变的是紫杉醇的含量,使紫杉醇载药量分别为0.5%、1.0%、1.5%和2.0%。结果表明,当载药量为0.5%时,其绝对生物利用度为13%,当载药量为1.0%时,绝对生物利用度略有上升,达到14%。然而,当紫杉醇浓度进一步增加到1.5%和2.0%时,绝对生物利用度却出现了显著下降,分别降至4%和2%。
三、制剂特点
当温度约在30℃以下时,单油酸甘油酯以层状晶体相存在,它与三辛酸甘油酯不混溶。同样,吐温80在这个温度范围内也与单油酸甘油酯不混溶。因此,在较低温度下,这些成分的物理状态限制了它们的相互溶解。当温度高于30℃时,这三种成分都呈现液态,并且能够均匀混合。即使在0℃以下,也未发现紫杉醇沉淀析出,说明紫杉醇在制剂中不易受温度影响而析出。该制剂可以在-20℃至40℃之间循环加热和冷却,而不会药物的疗效产生影响,表明制剂具有很好的热稳定性,能够在一定温度范围内保持其有效性和稳定性。这些结果对于DHP107紫杉醇口服制剂的存储和给药具有重要意义,因为这意味着该制剂可以在室温下以相分离的形式存储,在存储过程中不需要特殊的温控条件。
四、DHP107口服给药后的吸收机制
研究者通过SAXS(小角X射线散射)和cryo-TEM(冷冻透射电子显微镜)实验发现DHP107在水中会形成了一种海绵相(sponge phase)。海绵相是立方相的一种无序类似物,其粘度低于立方相,但仍保留了立方相约一半的粘膜粘附性。尽管海绵相的粘度较低,但其保留的粘膜粘附性对于DHP107的口服生物利用度有积极影响,可以使DHP107粘附在肠道的粘液层上,这是药物吸收发生的有效部位,提高了DHP107在肠道内的滞留时间和吸收效率。
参考文献
[1] Jang Y, Chung HJ, Hong JW, Yun CW, Chung H. Absorption mechanism of DHP107, an oral paclitaxel formulation that forms a hydrated lipidic sponge phase. Acta Pharmacol Sin. 2017 Jan;38(1):133-145.
[2] Lee, Yong-Kyu Hong, Jung & Jang, Yura & Park, Yeong & Chung, Hesson. (2012). Development, Optimization and Absorption Mechanism of DHP107, Oral Paclitaxel Formulation for Single-Agent Anticancer Therapy.
[3] Kang YK, Ryu MH, Park SH, et al. Efficacy and safety findings from DREAM: a phase III study of DHP107 (oral paclitaxel) versus i.v. paclitaxel in patients with advanced gastric cancer after failure of first-line chemotherapy. Ann Oncol. 2018 May 1;29(5):1220-1226.
[4] Hyeong-Seok Lim, Kyun-Seop Bae, Jin-ah Jung, et al. Predicting the Efficacy of an Oral Paclitaxel Formulation (DHP107) Through Modeling and Simulation,Clinical Therapeutics,Volume 37, Issue 2,2015,Pages 402-417.

来源:药事纵横


