您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-11-07 09:25
美国食品药品监督管理局 (FDA) 已批准 Akura Medical 的研究设备豁免 (IDE) 申请,以启动 QUADRA-PE 研究,以评估 Katana 血栓切除术系统在急性肺栓塞 (PE) 患者中的疗效。
这项关键研究的联合首席研究员是 Sanjum Sethi(美国纽约哥伦比亚大学医学中心)和 Ann Gage(美国纳什维尔 Tristar Centennial Medical Center)。
Akura Medical 总裁兼首席执行官 Murali Srivathsa 表示:“QUADRA-PE 的 IDE 批准标志着该公司为医生提供治疗急性肺栓塞的下一代解决方案之旅中的一个重要里程碑。“我们根据医生的广泛反馈设计了 Katana 系统,这些医生分享了他们对血栓切除术系统的需求,该系统可以最大限度地减少到达凝块的难度,在没有导管堵塞的情况下去除所有类型的凝块,并提供更大的程序反馈。我们期待与我们的临床研究人员合作,以证明我们系统的功效。
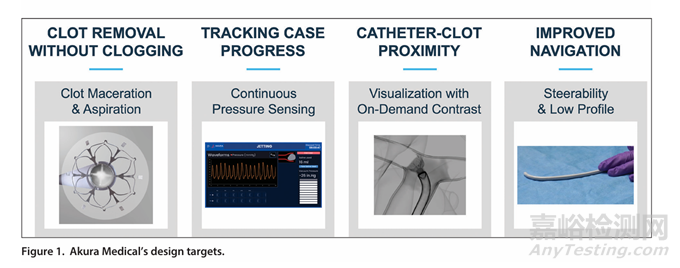
Katana 系统由一个双向、低轮廓的护套组成,旨在促进在复杂脉管系统中更顺畅地导航,并在不需要更换导管的情况下实现造影剂注射。它还具有高速盐水射流,旨在有效分解凝块,不受形态影响,防止导管堵塞以提高手术效率,以及提供实时肺动脉压力数据以提供手术进度见解的传感器。
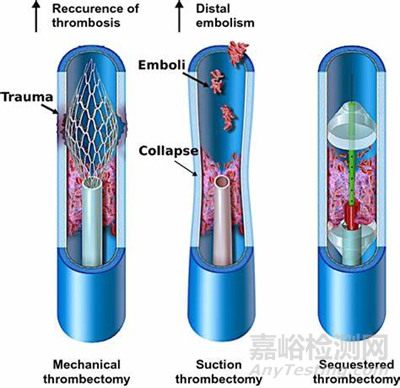
QUADRA-PE 是一项多中心、国际试验,旨在在全球多达 26 个地点招募多达 118 名具有临床意义的急性 PE 患者。主要有效性终点是通过计算机断层扫描 (CT) 血管造影评估的右心室/左心室 (RV/LV) 比值从基线到术后 48 小时降低。主要安全终点是术后 48 小时内主要不良事件 (MAE) 的综合发生率。
关于Akura
Akura Medical是 Shifamed, LLC. 的投资组合公司,Shifamed, LLC. 是一家高度专业化的医疗创新中心,专注于开发先进的解决方案,以更快地进入市场、降低风险、增加影响,并开辟一条通往所有人都能过上更长寿、更健康生活的世界的道路。

来源:CCI心血管医生创新俱乐部


