您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2024-11-13 18:10
刚刚,国家药监局发布《记忆合金肋骨板注册审查指导原则(征求意见稿)》,内容如下:
记忆合金肋骨板注册审查指导原则
(征求意见稿)
本指导原则旨在指导注册申请人对记忆合金肋骨板注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的审评提供参考。
本指导原则是对记忆合金肋骨板注册申报资料的一般要求,注册申请人需依据产品的具体特性确定其中内容是否适用。若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
本指导原则是对注册申请人和技术审评人员使用的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行,需在遵循相关法规和现行有效的国家标准或行业标准的前提下使用本指导原则。如果有能够满足相关法规要求的其他方法,也可以采用,但是需要提供详细的研究资料和验证资料。
本指导原则是在现行法规和标准体系以及当前认知水平下制定的,随着法规和标准的不断更新与完善,以及科学技术的不断发展,相关内容也将适时进行调整。
一、适用范围
本指导原则适用于肋骨骨折内固定的记忆合金肋骨接骨板。通常采用镍钛形状记忆合金材料制成。对于非记忆合金肋骨接骨板和其他记忆合金产品(如胸骨内固定器械),注册申请人可参考本指导原则中适用的内容。
二、注册审查要点
注册申报资料应符合国家药品监督管理局《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》中的要求,同时应符合以下要求:
(一)监管信息
1.产品名称
产品的命名需采用国家标准、行业标准中的通用名称,或以产品结构及组成、临床预期用途、适用部位为依据命名,需符合《医疗器械通用名称命名规则》《无源植入器械通用名称命名指导原则》等相关法规的要求。
2.分类编码
根据《医疗器械分类目录》,分类编码为13-01-03,管理类别为Ⅲ类。
(二)综述资料
详述产品立题依据,描述产品研发的目的、研发的基础和必要性。记忆合金肋骨接骨板产品设计开发应以临床需求为导向,应能保证记忆合金肋骨接骨板产品的输入、输出、评审、验证、确认、转化、更改等各环节的科学性和合理性。重点对产品安全有效性和质量可控性进行确认。产品设计应考虑医疗器械可用性工程的要求。
1.产品描述
需在产品描述中明确产品的通用名称及其确定依据;明确产品的管理类别,包括:所属分类子目录名称、一级产品类别、二级产品类别,管理类别,分类编码;明确产品的适用范围;明确产品的背景信息概述或特别细节,如:申报产品的历史概述、历次提交的信息,与其他经批准上市产品的关系等。如不适用,需说明。
2.器械及操作原理描述
2.1明确记忆合金肋骨接骨板的结构及组成信息,包括选用材料及符合标准、材料牌号信息、表面处理方式、交付状态、灭菌方式、灭菌有效期信息。
2.2提供产品各型号关键部位的结构图。在图示中标识关键尺寸信息及测量位置,例如记忆合金肋骨接骨板长度(L)、高度(H)、厚度(δ)、环抱臂内径(Φ)、板孔直径(R)、环抱臂分布(环抱臂间距L1和数量S1-S4等)、弧度(α)、宽度(W)等。明确产品各型号的关键尺寸及公差。注册申请人可结合申报产品特点选择关键尺寸参数进行规定以充分表征产品结构设计特征。
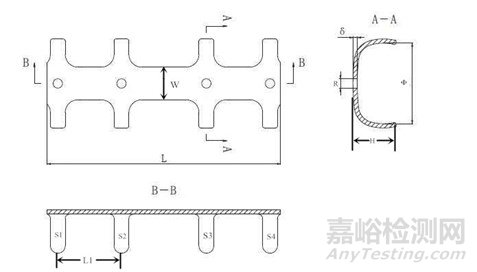
(a)
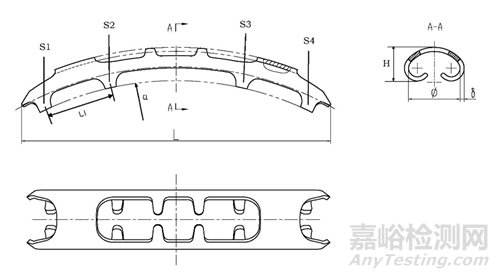
(b)
图 记忆合金肋骨接骨板结构图及其尺寸示例
2.3明确产品各组件的材料牌号及其符合的国家标准、行业标准、国际标准,材料牌号的描述需与其符合的标准一致。
2.4需提交解剖适配图,提供临床使用方法及具体的临床适用情形。
3.型号规格
对于存在多种型号规格的产品,需明确各型号规格的区别,推荐采用对比表及带有说明性文字的图片、图表,如提供各组件组配关系示意图等,对各种型号规格的结构组成、产品特征、技术参数、功能等方面加以描述。
4.包装说明
明确产品所有组成部分的包装形式及初包装(无菌屏障系统)材料信息。建议提供初包装的照片及图示,明确初包装的尺寸信息和材料信息,并以列表形式说明所有包装内容物。
5.与同类和/或前代产品的参考和比较
需阐述申请注册产品的研发背景和目的。如有参考的同类产品或前代产品,需提供同类产品或前代产品的信息,并说明选择其作为研发参考的原因。
需综述同类产品国内外研究、临床使用现状及发展趋势。同时列表比较说明申报产品与参考产品(同类产品或前代产品)在工作原理、原材料、制造工艺、表面处理、结构特征、关键尺寸、适用范围及产品性能指标等方面的异同。
6.适用范围和禁忌证
产品的适用范围、适用人群、禁忌证需与申报产品的性能、功能相符。
6.1适用范围
适用范围的表述需客观、清晰,使用有明确定义或行业公认的术语或名词。例如:适用于肋骨骨折内固定。
6.2预期使用环境
明确预期使用的地点(如医疗机构),说明可能影响其安全性和有效性的环境条件。
6.3适用人群
说明该器械目标患者人群信息,以及使用过程中需要考虑的因素、不适宜应用的某些疾病、情况或特定人群(如适用)。一般记忆合金肋骨接骨板适用于骨骼成熟患者。
6.4禁忌证
如适用,通过风险/受益评估后,针对某些疾病、情况或特定的人群,认为不推荐使用该产品,需明确说明。
7.申报产品上市历史
如适用,提交申报产品在各国家或地区的上市批准时间、销售情况。如有不良事件和召回,分别对申报产品上市后发生的不良事件、召回的发生时间、注册申请人采取的处理和解决方案、相关部门的调查处理情况等进行描述。
(三)非临床研究资料
1.产品风险管理资料
注册申请人需对产品全生命周期实施风险管理,提交风险管理资料(参照GB/T 42062《医疗器械风险管理对医疗器械的应用》),充分识别产品的设计、原材料采购、生产加工过程、表面处理、后处理、产品包装、灭菌、运输、贮存、使用等产品生命周期内各个环节的安全特征,从生物和化学危险、性能有关的危险等方面,对产品进行全面的风险分析,并详述所采取的风险控制措施。
风险管理报告需包括生产和生产后信息(具体内容参考GB/T 42062《医疗器械风险管理对医疗器械的应用》第10章和《医疗器械安全和性能的基本原则》的2.1.2 e)和f)部分)。产品变更注册和已在境外上市产品注册时,申报资料中的风险管理报告需包括上述内容,将风险管理贯穿于产品的全生命周期。
记忆合金肋骨接骨板产品不良事件的类型包括但不限于:患者过敏、固定板断裂、环抱臂断裂、相变温度漂移、与配合用手术工具的不匹配、环抱臂在预弯过程中发生变形、损坏等。
2.医疗器械安全和性能基本原则清单
明确产品符合《医疗器械安全和性能基本原则清单》各适用项要求所采用的方法及证明其符合性的文件。
3.产品技术要求
产品技术要求的制定需符合《医疗器械产品技术要求编写指导原则》的要求,同时结合产品具体适用的指导原则或相关国家标准、行业标准以及产品的特点,选择适用项对各项性能指标和检验方法进行制定,以保证产品安全、有效。
3.1产品型号/规格及其划分说明
列表说明产品的型号、规格,明确产品型号、规格的划分说明。提供各型号产品的结构图并标识关键尺寸。提供产品关键尺寸信息,如记忆合金肋骨接骨板长度、宽度、高度、厚度、弧度、板孔直径、环抱臂分布等。
3.2性能指标
产品技术要求中指标需针对终产品,选取适用的项目制定,且性能指标不低于产品适用的强制性国家标准和/或强制性行业标准。如产品有特定设计,注册申请人还需根据产品设计特征设定相应的性能指标,并将其列入产品技术要求。对于可进行客观判定的成品定性或定量的功能性、安全性指标,需将其列入产品技术要求。
产品技术要求性能指标一般包括:记忆合金肋骨接骨板关键尺寸(如记忆合金肋骨接骨板长度、环抱臂最大内径、厚度、板孔直径等)及公差,硬度,表面质量(外观、表面粗糙度、表面缺陷),形状回复力,形状回复率,相变温度,无菌(如适用),环氧乙烷残留量(如适用)。
3.3检验方法
产品的检验方法需根据技术性能指标设定,检验方法需优先采用国家标准/行业标准中的方法。对于相关国家标准/行业标准中不适用的条款,需说明不适用的原因。所有引用的标准注明其编号和年代号。自建检验方法需提供相应的方法学依据及理论基础,同时保证检验方法具有可操作性和可重现性,必要时可以采用相应图示进行说明,文本较大的可以附录形式提供。
3.4附录
建议注册申请人以附录形式明确产品制造材料信息(如化学成分、冶金结构、机械性能),同时明确材料性能符合的相关标准。如已开展磁共振(MR)环境下的行为属性的相关验证,磁共振兼容性相关信息可在附录中明示。
3.5其他
本部分仅提供了常规产品的基本性能要求,予以参考。如有不适用的项目,需予以说明。对于使用新材料、新技术、新设计或具有新作用机理、新功能的产品,需在产品技术要求中明确产品所具有的其他功能性、安全性指标,性能指标的制定需符合《医疗器械产品技术要求编写指导原则》的要求。
4.产品检验
注册申请人需提供符合医疗器械注册申报法规文件要求的检验报告。记忆合金肋骨接骨板在同一注册单元内所检验的产品需为能够代表本注册单元内其他产品安全性和有效性的典型产品,并提供典型性产品的选择依据。
5.研究资料
注册申请人需说明产品技术要求中性能指标及检验方法的确定依据,需提供采用的原因及理论基础。依据产品性能研究结果,结合临床需求制定性能指标接受标准。必要时,对于自建方法,需提供相应的依据及方法学验证资料。提供涉及的研究性资料、文献资料和/或标准文本。
注册申请人需提供产品材料、产品设计相关静/动态性能等方面的性能研究资料,并提供其可接受的依据,必要时与已上市同类产品相关性能进行对比,以证明其安全有效性。研究资料包括但不限于如下内容:
5.1化学/材料表征研究
针对记忆合金肋骨接骨板使用的记忆合金材料(如镍钛合金),需明确材料符合的标准并提供符合对应标准中的相应规定的研究资料,如化学成分、冶金结构、机械性能等,并提供后续加工过程对材料性能影响的研究资料。必要时,对终产品化学/材料性能进行表征。
5.2物理和机械性能研究
注册申请人需根据产品在临床使用中的受力情况,结合产品的结构设计、尺寸等因素,分别选取最差情况开展性能研究,并提供最差情况的确定依据。必要时,可以通过有限元分析最差情况并提交报告。
5.2.1弯曲性能研究
记忆合金肋骨接骨板在临床实际使用过程中,主要抵抗来自呼吸产生的肌肉牵拉力。为防止弯曲断裂,注册申请人需设计试验模型以评估记忆合金肋骨接骨板在受力时抵抗弯曲的能力,提供记忆合金肋骨接骨板弯曲性能的研究资料。研究需考虑产品的结构设计、尺寸规格、预期适用情形及其受力模式等影响因素,提供试验方法、参数设定(如加载模式、载荷大小、试验配置等)等的确定依据,分析论证试验结果的可接受性。
5.2.2抗滑动性能研究
记忆合金肋骨接骨板在临床实际使用过程中,需要抵抗呼吸产生的往复循环牵拉力。为防止出现轴向滑动,注册申请人需设计试验模型以评估记忆合金肋骨接骨板在受力时抵抗轴向滑动的能力,提供记忆合金肋骨接骨板抵抗轴向滑动性能的研究资料。研究需考虑产品的结构设计、尺寸规格、预期适用情形及其受力模式等影响因素,提供试验方法、参数设定(如加载模式、载荷大小、试验配置、工装设计等)等的确定依据,分析论证试验结果的可接受性。
5.2.3疲劳性能研究
记忆合金肋骨接骨板需要长周期重复承受人体呼吸收缩、扩张肺的收张力和肌肉牵拉力。为避免出现疲劳断裂或松脱,注册申请人需设计试验模型以评估记忆合金肋骨接骨板的疲劳性能。研究需考虑产品的结构设计、尺寸规格、预期适用情形及其受力模式等影响因素,提供试验方法、参数设定(如加载模式、载荷大小、循环次数、试验配置等)等的确定依据,分析论证试验结果的可接受性。
5.2.4相变温度、形状回复力、形状回复率性能研究
记忆合金肋骨接骨板需验证其“形状记忆”功能,注册申请人需设计试验模型以评估记忆合金肋骨接骨板整体及单臂(反复弯折后)的相变温度、形状回复力、形状回复率性能。研究需考虑产品的结构设计、尺寸规格、预期适用情形及其受力模式等影响因素,提供试验方法、参数设定(如原始尺寸、撑开尺寸、恢复后尺寸、撑开和回复次数、试验配置等)等的确定依据,分析论证试验结果的可接受性。
5.3生物学特性研究
产品的生物学评价需涵盖终产品,按照GB/T 16886.1《医疗器械生物学评价第1部分:风险管理过程中的评价与试验》中的系统方法框图及《国家食品药品监督管理局关于印发医疗器械生物学评价和审查指南的通知》中的审查要点进行风险评价,需充分考虑产品疲劳前后镍离子析出(可参考YY/T 1823《心血管植入物镍钛合金镍离子释放试验方法》)的影响。生物学评定终点一般包括细胞毒性、致敏、刺激或皮内反应、材料介导的致热性、急性全身毒性、亚急性毒性、慢性毒性、亚慢性毒性、植入反应、遗传毒性和致癌性,必要时根据GB/T 16886系列标准进行生物学试验。
5.4磁共振兼容性研究
申报产品若预期在磁共振(MR)环境中使用,建议开展MR环境下的行为属性的相关验证,根据YY/T 0987系列标准对产品在MR环境下的磁致位移力、磁致扭矩、射频致热、伪影等项目进行评估。需根据研究报告,列出MR试验设备、磁场强度、比吸收率(SAR)等试验参数及温升、位移力、扭矩及伪影评估结果,研究报告相关信息在说明书中予以明示。
如注册申请人未对申报产品进行MR环境下行为属性的相关验证,需明确该产品尚未在MR环境下对该产品的温升、移位状况及伪影进行测试评估,需在说明书的警示中注明相关内容,提示其存在的风险,由临床医生与医疗机构综合判断临床使用风险的可控性。
5.5清洗和灭菌研究
5.5.1清洗
明确生产工艺中涉及的各种加工助剂(如切削液等)的质量控制标准。明确产品的清洗过程,提供经清洗过程后加工助剂残留控制的验证资料。对生产加工过程使用的所有加工助剂等添加剂均需说明使用剂量、对残留量的控制措施和接受标准以及安全性评价报告。
5.5.2灭菌研究
描述用于保证产品无菌的质量保证体系,明确灭菌工艺(方法和参数)和无菌保证水平(SAL)。产品的无菌保证水平(SAL)需达到10-6。
5.5.2.1生产企业灭菌
对于经辐照灭菌的产品,需明确辐照剂量及相关的验证报告,具体的剂量确定依据可参照GB 18280系列标准。
对于经环氧乙烷灭菌的产品,需提供灭菌结果确认和过程控制报告,具体可参照GB 18279系列标准。
5.5.2.2最终使用者灭菌
对于非灭菌包装的终产品,需明确推荐采用的灭菌方法并提供确定依据,并提供验证资料。采用其他灭菌方法的需提供方法合理性论证和工艺确认及过程控制报告。
5.6动物试验研究
需按照《医疗器械动物试验研究注册审查指导原则第一部分:决策原则》决策是否需开展动物试验研究。如开展动物试验研究,需按照《医疗器械动物试验研究注册审查指导原则第二部分:试验设计、实施质量保证》进行,并遵循3R原则。需关注动物模型建立的科学性和合理性,以及对临床的借鉴意义。一般对于工作机理明确、设计定型,生产工艺成熟,且不改变常规用途的记忆合金肋骨接骨板产品不需要进行动物试验研究。
5.7稳定性研究
申报产品需参照《无源植入性医疗器械稳定性研究指导原则》提供产品稳定性研究资料。稳定性研究一般包含货架有效期、使用稳定性和运输稳定性,其中货架有效期和运输稳定性研究包含器械本身性能稳定性和包装性能稳定性两方面。
5.7.1 货架有效期
医疗器械货架有效期的验证试验通常可分为加速稳定性试验、实时稳定性试验两类。无论加速稳定性试验还是实时稳定性试验,注册申请人均需在试验方案中设定测试项目、测试方法及判定标准。测试项目仅需评估产品随时间老化的相关性能,包括器械自身性能测试和包装系统性能测试两方面。其中器械本身性能稳定性需提供老化前后产品关键性能(如相变温度、形状回复率、形状回复力等)的验证对比资料。包装系统性能测试(如染色液穿透试验、气泡试验、材料密封强度试验等)主要目的是为了验证包装系统对微生物的屏障性能,即无菌状态/微生物限度要求的保持。对于灭菌产品,需要明确灭菌方式与产品的包装材料、包装工艺及方法的适配性。
若注册申请人提供其他医疗器械的货架有效期验证资料,需提供其与本次申报产品在原材料、灭菌方法、灭菌剂量、包装材料、包装工艺、包装方式及其他影响阻菌性能的因素方面具有等同性的证明资料。不同包装、不同灭菌方式的产品需分别提供验证资料。
5.7.2 运输稳定性
提交运输稳定性验证资料,证明规定的运输条件不会对医疗器械的特性和性能造成不利影响。运输稳定性验证应依据适用的国内、国际标准和验证方案进行,如:产品包装的跌落试验、振荡试验等。
(四)临床评价资料
该产品不属于《免于进行临床评价医疗器械目录》中的产品,注册申请人需按照《医疗器械临床评价技术指导原则》的要求选择合适的临床评价路径提交临床评价资料。
1 .同品种医疗器械临床数据
对于选择同品种临床评价路径的产品,可按照《医疗器械临床评价技术指导原则》中将同品种医疗器械的临床数据用于支持申报产品的安全性、临床性能和/或有效性的要求。
2.申报产品临床试验数据
注册申请人如开展临床试验,可参照《决策是否开展医疗器械临床试验技术指导原则》明确需要开展临床试验的主要考虑因素,若开展申报产品临床试验,则需严格按照《医疗器械临床试验质量管理规范》进行临床试验,并提交完整的临床试验资料。临床试验的设计可参考《医疗器械临床试验设计指导原则》。
注册申请人如有境外临床试验数据,可参照《接受医疗器械境外临床试验数据技术指导原则》的要求提交相关资料。
(五)产品说明书和标签样稿
产品说明书、标签和包装标识需符合《医疗器械说明书和标签管理规定》和相关国家标准、行业标准的要求,例如YY/T 0466.1《医疗器械用于医疗器械标签、标记和提供信息的符号第1部分:通用要求》。
说明书需告知使用者所有使用过程中相关的剩余风险。对产品预期使用者的技术知识、经验、教育背景、培训、身体状况(如适用)以及产品使用环境(含工作条件)有要求的,在说明书中需予以明确。
需要明确产品使用方法及适配的手术工具。根据形状回复力、形状回复率的要求,明确手术操作关键步骤。如环抱臂撑开与恢复条件(如温度)、撑开尺寸等要求。
(六)质量管理体系文件
按照《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》提交相关文件。
三、参考文献
[1]中华人民共和国国务院.医疗器械监督管理条例:中华人民共和国国务院令第739号[Z].
[2]国家市场监督管理总局.医疗器械注册与备案管理办法:国家市场监督管理总局令第47号[Z].
[3]国家药品监督管理局.医疗器械注册申报资料要求和批准证明文件格式:关于公布医疗器械注册申报资料要求和批准证明文件格式的公告2021年第121号[Z].
[4]国家食品药品监督管理总局.医疗器械说明书和标签管理规定:国家食品药品监督管理总局令第6号[Z].
[5]国家食品药品监督管理总局.医疗器械分类规则:国家食品药品监督管理总局令第15号[Z].
[6]国家食品药品监督管理总局.医疗器械通用名称命名规则:国家食品药品监督管理总局令第19号[Z].
[7]国家药品监督管理局.无源植入器械通用名称命名指导原则:国家药品监督管理局通告2020年第79号[Z].
[8]国家食品药品监督管理总局.医疗器械注册单元划分指导原则:国家食品药品监督管理总局公告2017年第187号[Z].
[9]国家药品监督管理局.医疗器械安全和性能的基本原则:国家药品监督管理局通告2020年第18号[Z].
[10]国家药品监督管理局.医疗器械产品技术要求编写指导原则:国家药监局关于发布医疗器械产品技术要求编写指导原则的通告2022年第8号[Z].
[11]国家食品药品监督管理局.医疗器械生物学评价和审查指南:关于印发医疗器械生物学评价和审查指南的通知2007年第345号[Z].
[12]国家药品监督管理局.医疗器械动物试验研究注册审查指导原则第一部分:决策原则(2021年修订版): 国家药监局关于发布医疗器械动物试验研究注册审查指导原则第一部分:决策原则(2021年修订版)等2项注册审查指导原则的通告2021年第75号[Z].
[13]国家药品监督管理局.医疗器械动物试验研究注册审查指导原则第二部分:试验设计、实施质量保证: 国家药监局关于发布医疗器械动物试验研究注册审查指导原则第一部分:决策原则(2021年修订版)等2项注册审查指导原则的通告2021年第75号[Z].
[14]国家药监局器审中心.无源植入性医疗器械稳定性研究指导原则(2022年修订版):国家药监局器审中心关于发布无源植入性医疗器械稳定性研究指导原则(2022年修订版)的通告2022年第12号[Z].
[15]国家药品监督管理局.医疗器械临床评价技术指导原则:国家药监局关于发布医疗器械临床评价技术指导原则等5项技术指导原则的通告2021年第73号[Z].
[16]国家药品监督管理局.决策是否开展医疗器械临床试验技术指导原则:国家药监局关于发布医疗器械临床评价技术指导原则等5项技术指导原则的通告2021年第73号[Z].
[17]国家药品监督管理局,国家卫生健康委员会.医疗器械临床试验质量管理规范:国家药品监督管理局,国家卫生健康委员会2022年第28号[Z].
[18]国家食品药品监督管理总局.接受医疗器械境外临床试验数据技术指导原则:食品药品监管总局关于发布接受医疗器械境外临床试验数据技术指导原则的通告2018年第13号[Z].
[19]GB/T 42062-2022,医疗器械风险管理对医疗器械的应用[S].
[20]GB/T 16886,医疗器械生物学评价系列标准[S].
[21]GB 18278.1-2015,医疗保健产品灭菌湿热第1部分:医疗器械灭菌过程的开发、确认和常规控制要求[S].
[22]GB 18279.1-2015,医疗保健产品灭菌环氧乙烷第1部分:医疗器械灭菌过程的开发、确认和常规控制的要求[S].
[23]GB/T 18279.2-2015,医疗保健产品的灭菌环氧乙烷第2部分:GB 18279.1应用指南[S].
[24]GB 18280.1-2015,医疗保健产品灭菌辐射第1部分:医疗器械灭菌过程的开发、确认和常规控制要求[S].
[25]GB 18280.2-2015,医疗保健产品灭菌辐射第2部分:建立灭菌剂量[S].
[26]GB/T 18280.3-2015,医疗保健产品灭菌辐射第3部分:剂量测量指南[S].
[27]YY/T 0987.1-2016,外科植入物磁共振兼容性第1部分:安全标记[S].
[28]YY/T 0987.2-2016,外科植入物磁共振兼容性第2部分磁致位移力试验方法[S].
[29]YY/T 0987.3-2016,外科植入物磁共振兼容性第3部分图像伪影评价方法[S].
[30]YY/T 0987.4-2016,外科植入物磁共振兼容性第4部分射频致热试验方法[S].
[31]YY/T 0987.5-2016,外科植入物磁共振兼容性第5部分:磁致扭矩试验方法[S].
[32]YY/T 0466.1-2016, 医疗器械用于医疗器械标签、标记和提供信息的符号第1部分:通用要求[S].
[33]GB/T 24627-2023,外科植入物用镍-钛形状记忆合金加工材[S].
[34]YY/T 1771-2021,弯曲-自由恢复法测试镍钛形状记忆合金相变温度[S].
[35]YY/T 1823-2022,心血管植入物镍钛合金镍离子释放试验方法[S].

来源:国家药监局


