您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-02-14 08:29
1、概述
药品注册过程中有很多细节不可忽略,笔者以多年工作经验汇总了药品注册过程中那些不可忽略的诸多细节,以期对各位同仁有一定的启示作用。
2、那些不可忽略的细节汇总
药品注册过程中会遇到各种各样的问题,包括工艺信息表核对、质量研究及证明信文件等,下面将逐一进行介绍。
工艺信息表核对时需关注的细节
生产地址需具体到厂房/车间、生产线,同时需确保药品生产许可证包括拟定生产线;如使用到薄膜包衣预混剂,建议在工艺信息表中明确所用薄膜包衣预混剂的组成成份;如存在中间体暂存情况,应提供中间体暂存的具体条件、时限及其支持性研究资料,具体研究应结合剂型特点、工艺特点、暂存时间等选择具有代表性的考察指标。注意考察指标的合理性和全面性。同时在工艺描述中体现中间体暂存条件、暂存时限及拟定包装形式等。
CDE发补的杂质对照品无法获得时,该如何处理?
出于谨慎考虑,部分审评老师可能会参照原研及同品种研究情况,针对某一原料药发补较多杂质。在某些情况下,可能相应的杂质对照品难以获得(难以购买,或购买成本太高,定制成功与否存在风险等),在这种情况下我们该如何应对呢?
首先需分析该杂质产生的可能性,如为工艺杂质,需分析该杂质在什么工艺路线下会产生;如为降解杂质,需分析是否需要极端的降解条件才能产生该杂质等等。或者是采用拟定有关物质分析方法定位目标杂质或目标杂质的主要降解产物(应有相应的质谱离子碎片),用质谱在对应的保留时间全扫样品,证明该杂质未检出,且稳定性研究期间该杂质无增加趋势。
如经过详细分析,证明该杂质产生的风险很小,有可能CDE老师会结合我们提供的分析研究资料认可不对其进行更进一步的要求。
干燥失重
有些产品是否需要进行干燥失重研究,可能无法简单地一概而论。干燥失重是指药品在规定条件下进行干燥,测定药品在干燥过程中失去的吸附水、结晶水和挥发性物质的总量(中国药品检验标准操作规范),常用的干燥失重检测方法包括恒温常压干燥法、恒温减压干燥法及干燥器干燥法等。
某一原料药,含有结晶水,采用费休氏法测定本品水分,其含水量有1个理论值。对其进行干燥失重研究,其研究结果汇总如下表所示:
某原料药干燥失重研究结果
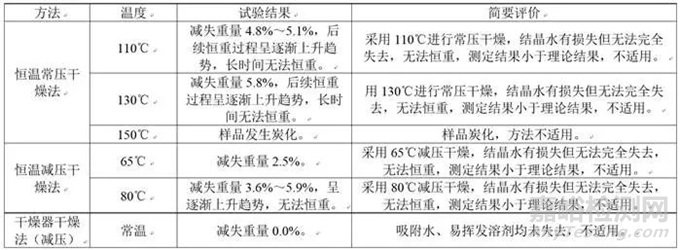
综合以上研究资料,该原料药可不进行干燥失重研究。针对本品的吸附水及结晶水,可参照中国药典2020年版四部通则0832第一法(费休氏法1.容量滴定法)进行试验;挥发性物质主要为溶剂,通过残留溶剂检查项进行控制即可。
炽灼残渣
某一原料药为钠盐形式,可能不需要进行炽灼残渣研究。炽灼残渣主要将有机药物经加热灼烧至完全炭化或无机药物加热分解后,再加适量硫酸湿润,高温炽灼至灰化完全后遗留的无机杂质(多为金属的氧化物或硫酸盐)。该原料药中含大量钠离子(5.3%),会干扰炽灼残渣作为评判无机杂质多少的判断(中国药典一般含无机盐的原料均未制定炽灼残渣检查项),故可不定入质量标准/内控标准。
口崩片崩解时限
对于口崩片,崩解时限是关键质量属性。现版《中国药典》收载了专用于口崩片崩解时限检查的装置,该装置为《中国药典》所特有的。某些口崩片产品收载于USP/BP,其崩解时限均是采用普通崩解时限装置进行研究,如枸橼酸西地那非口崩片。在进行仿制药崩解时限研究时,建议首选《中国药典》口崩片崩解时限专用装置进行仿制药与参比制剂对比研究,应符合《中国药典》附录规定限度。如采用普通崩解时限装置进行崩解时限检查,建议同时采用两种装置进行仿制药与参比制剂对比研究,详细记录崩解时间及现象,说明不采用《中国药典》口崩片专用崩解时限装置的依据,并拟订合理限度。
省所复核意见如何处理
针对某一口服固体片剂,有关物质的省所复核意见如下:
(1)杂质采用加校正因子主成分外标法计算,但对照品溶液为含量测定项下与主成分相同浓度的对照品溶液(0.1mg/ml),与杂质限度浓度相差较大(约1000倍),影响杂质准确定量,建议配制与杂质限度浓度相当的对照品溶液;
(2)多个已知杂质未检出,建议设置灵敏度指标并规定信噪比。
针对以上2个复核意见,我们应尽可能按照省所复核意见进行相关完善,将对照品溶液浓度尽量与杂质限度保持一致;因多个杂质均未检出,需配置灵敏度溶液(单杂限度为0.10%,其灵敏度溶液不得高于0.05%),并拟定合理的信噪比(S/N≥10),以确保杂质能准确检出。
证明性文件
药品生产许可证是比较重要的证明性文件,原料药需包含相应的生产线信息,制剂的药品生产许可证需包括相应的制剂生产线。对于委托生产的产品,药品生产许可证需体现相应的委托生产关系。
3、小结
药品注册过程中会遇到各种各样的问题,笔者以多年工作经验汇总了部分可能会被忽略的“小细节”,包括工艺信息表核对、质量研究及证明性文件等,以期对大家有一定启示作用,助力产品快速获批。

来源:药事纵横


