您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-07-20 09:47
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
百济神州PARP1/2抑制剂拟纳入优先审评。百济神州PARP1/2抑制剂帕米帕利上市申请(NDA)获CDE纳入拟优先审评公示名单,该新药拟用于治疗既往接受过至少两线化疗的BRCA突变的晚期卵巢癌、输卵管癌或原发性腹膜癌患者。NDA的提交是基于一项I/II期临床NCT03333915的积极结果。该试验的II期部分入组了113例既往接受过至少两线标准化疗、携有BRCA1/2突变的高级别上皮性卵巢癌(包括输卵管癌或原发性腹膜癌)或高级别子宫内膜上皮样癌患者,主要终点为经RECIST 1.1评估的客观缓解率。试验结果将于医学会议上公布。
国内药讯
1.京新药业匹伐他汀钙分散片通过一致性评价。京新药业宣布其匹伐他汀钙分散片通过一致性评价。匹伐他汀钙是第三代他汀类药物,是目前国际临床应用中治疗高胆固醇血症、家族性高胆固醇血症效果较好的他汀类药物之一,因其临床有效剂量为1-2mg/天,明显低于其他已上市的他汀类药物,具有糖代谢影响小的特点,具有良好的耐受性。根据IQVIA数据显示,2019年度匹伐他汀钙片国内销售额超过10亿元 。
2.石药美金刚片仿制药即将获批。石药欧意按仿制4类报产的盐酸美金刚片审评状态变更为“在审批”,有望近期获批上市并视同通过一致性评价。盐酸美金刚片是用于治疗中重度阿尔茨海默症的药物,其作用机制为拮抗N-甲酰天冬氨酸受体,延缓兴奋性神经递质谷氨盐酸的释放,改善认知功能,属于2019年版国家医保乙类药物。2019年中国公立医疗机构终端盐酸美金刚片销售额超过5亿元,其中,灵北占据85.53%的市场份额,联邦制药占比14.47%。
3.索元生物抗肿瘤首创新药获FDA快速通道资格。7月17日,索元生物宣布FDA授予其全球首创新药DB102(Enzastaurin)用于一线治疗脑胶质母细胞瘤(GBM)的快速审评通道资格。DB102是从礼来引进的一款丝氨酸/苏氨酸激酶抑制剂,索元生物利用其生物标记物平台技术发现一组全新的生物标记物DGM1,DGM1阳性患者在服用DB102后其生存期有着非常显著的改善。目前评估DB102用于CD20阳性的弥漫性大B细胞淋巴瘤的III期ENGINE研究正在中美两国开展;DB102用于新诊断GBM的国际III期临床也已获FDA及NMPA的批准,预计将于今年启动。
4.金城医药2.4类新药头孢唑林钠获批临床。广东金城金素2.4类改良型新药注射用头孢唑林钠获CDE批准,即将开展用于颌面部间隙感染的临床研究。目前国内外尚无同类产品获批“颌面部间隙感染”的适应症。头孢唑林钠是第一代头孢菌素,抗菌谱广,已获批用于呼吸道感染、尿路感染、皮肤及软组织感染等敏感细菌所致的感染治疗,2019年中国公立医疗机构终端销售额为41.25亿元,华润九新占据80.56%的市场份额。
5.强生新型RSV融合蛋白抑制剂在华申报临床。强生在中国提交的JNJ-53718678口服混悬液的临床试验申请获CDE受理。JNJ-53718678是强生旗下杨森开发的一种新型人呼吸道合胞病毒(RSV)融合蛋白抑制剂,具有治疗呼吸道合胞病毒的潜力。全球范围内,JNJ-53718678处于Ⅱ期临床阶段,本次是该药首次在中国申报临床。目前,杨森正在开展多项关于JNJ-53718678的临床试验:其中一项为用于上呼吸道感染RSV病毒的成人和青少年造血干细胞移植患者的Ⅱ期临床研究。
国际药讯
1.礼来IL-23抑制剂达到Ⅲ期临床终点。礼来IL-23单抗mirikizumab治疗中重度斑块状银屑病的Ⅲ期临床OASIS-2结果积极。与安慰剂相比,mirikizumab治疗组16周后达到sPGA(静态医生总体评估)分数为0或1且评分至少改善2分的患者比例为79.7%,达到银屑病面积和严重程度指数与基线相比改善至少90%(PASI 90)的患者比例为74.4%,均显著优于安慰剂组达主要终点。该研究同时达所有关键次要终点(包括与活性对照相比的所有关键次要终点)。
2.拜耳/默沙东心衰新药获FDA优先审评。FDA受理拜耳与默沙东联合开发的vericiguat的新药申请,用于治疗经历心力衰竭恶化事件后射血分数低于45%的症状性慢性心力衰竭患者。FDA同时授予其优先审评资格,预计2021年1月20日前做出回复。一旦获批,vericiguat有望成为首个治疗这类患者的可溶性sGC激动剂。在一项Ⅲ期临床VICTORIA中,中位随访10.8个月的结果显示,vericiguat治疗组较安慰剂组降低了患者心衰住院和心血管原因死亡风险(35.5%vs38.5%,HR 0.90)。
3.英国地塞米松治疗COVID-19大型临床数据发布。由牛津大学等机构与英国政府合作开展的RECOVERY临床试验结果发表在《新英格兰医学杂志》上。该研究在超过11500例COVID-19住院患者中评估一系列潜在疗法(包括低剂量地塞米松)的疗效,结果显示,地塞米松治疗组患者的28天死亡率为22.9%(482/2104),显著低于常规治疗组(25.7%,p<0.001)。在机械通气、接受输氧但是不需要机械通气和不需要任何呼吸支持各亚组中,三个亚组28天死亡率与对照组相比的数值分别为29.3%vs41.4%、23.3%vs26.2%和17.8%vs14.0%。
4.丙肝药物组合SOF/DCV加快COVID-19患者临床恢复。7月16日,在第23届虚拟国际艾滋病大会上发表了一项最新研究,抗病毒药物组合索非布韦/达克他韦(SOF/DCV)联合标准治疗在中重度COVID-19患者中显示出临床获益。与对照组相比,SOF/DCV治疗组中29例患者在14天或更短时间内达到了临床恢复,达主要终点指标。SOF/DCV组患者的中位住院时间为6天,标准护理组为8天;SOF/DCV组的平均出院时间也较短(6天vs11天)。此外,SOF/DCV组中有3例患者死亡,对照组中有5例死亡。没有严重不良反应的报道。
5.AC Immune SA阿尔茨海默症疫苗启动Ⅰb/Ⅱa期试验。AC Immune SA公司宣布将启动旗下阿尔茨海默症(AD)疫苗ACI-35.030更高剂量组的Ⅰb/Ⅱa期临床试验,评估早期AD患者在接受不同剂量的ACI-35.030后48周治疗期内的安全性、耐受性和免疫原性。试验的其他终点还包括评估临床和认知状况的改善,以及其他免疫原性和安全性数据。ACI-35.030是以脂质体作为疫苗免疫佐剂的抗pTau活性疫苗,能够减少并促进患者体内Tau聚集物的清除,减慢Tau病理学进程,治疗潜在的tau蛋白病。
6.Oncoru与默沙东达成Keytruda临床合作。Oncorus公司宣布与默沙东达成一项临床试验合作,将评估Oncorus开发的病毒免疫疗法ONCR-177与抗PD-1疗法Keytruda联用,治疗晚期/难治性皮肤、皮下或转移性淋巴结实体瘤成人患者的疗效。ONCR-177是一种瘤内给药的溶瘤单纯疱疹病毒(oHSV)病毒免疫疗法,它同时可以表达多达5种调节免疫反应的转基因(表达的蛋白包括IL-12、CCL4、FLT3配体和经临床证实的免疫检查点PD-1和CTLA-4的拮抗剂),可以在裂解癌细胞的同时,改变肿瘤微环境,进一步刺激抗肿瘤免疫反应。
医药热点
1.13部门发文推进互联网医疗。7月15日,国家发改委、中央网信办、国家卫健委、国家医保局等13部门联合发布《关于支持新业态新模式健康发展激活消费市场带动扩大就业的意见》。《意见》明确,积极发展互联网医疗,以互联网优化就医体验,打造健康消费新生态。《意见》强调,规范推广慢性病互联网复诊、远程医疗、互联网健康咨询等模式,支持平台在就医、健康管理、养老养生等领域协同发展,培养健康消费习惯。
2.中疾控专家回应多地冻虾包装箱核酸阳性事件。7月16日,云南省通报排查结果,发现抽查的厄瓜多尔冻南美白虾包装箱检出3份核酸阳性。这是继大连、厦门、江西萍乡、重庆沙坪坝后,又一地从进口虾外包装检出新冠病毒。中国疾控中心全球公共卫生中心主任、传染病预防控制国家重点实验室副主任董小平表示,公众应科学理性看待进口冻虾包装箱核酸阳性,从发现新冠病毒至今,几乎没有真正食用生鲜食品造成感染的案例,同时呼吁,在疫情期间到菜市场购物要做好个人防护。
3.新疆新增新冠肺炎确诊病例13例。据新疆维吾尔自治区卫健委官网消息,7月18日0-24时,新疆(含兵团)报告新型冠状病毒肺炎新增确诊病例13例,新增无症状感染者30例,均在乌鲁木齐市。截至7月18日24时,新疆(含兵团)累计报告新型冠状病毒肺炎确诊病例106例(新疆维吾尔自治区82例,新疆生产建设兵团24例),累计治愈出院病例73例,累计死亡病例3例。现有确诊病例30例,无症状感染者41例,正在接受医学观察2705人。
股市资讯
【安图生物】1)公司获得河南省药监局颁发的关于反三碘甲状腺原氨酸检测试剂盒和真菌(1-3)-β-D-葡聚糖质控品的《医疗器械注册证》;2)持股超过50%股东安图实业以集中竞价交易、大宗交易、可交换债券持有人换股等方式合计减持公司股份661.05万股,占公司总股本的1.54%。
【华海药业】公司预计2020年半年度归母净利润5.52-6.2亿元,同比增长约65%-85%,扣非净利润5.02-5.70亿元,同比增长约90%-115%。
【京新药业】公司获得国家药监局核准签发的化学药品“匹伐他汀钙分散片”的《药品补充申请批准通知书》,该药品通过仿制药一致性评价。
审评动向
1. CDE最新受理情况(07月19日)
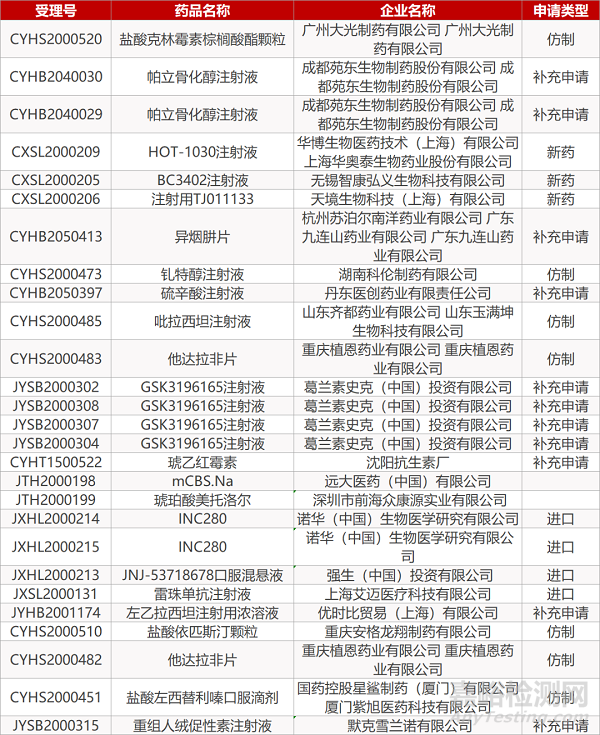
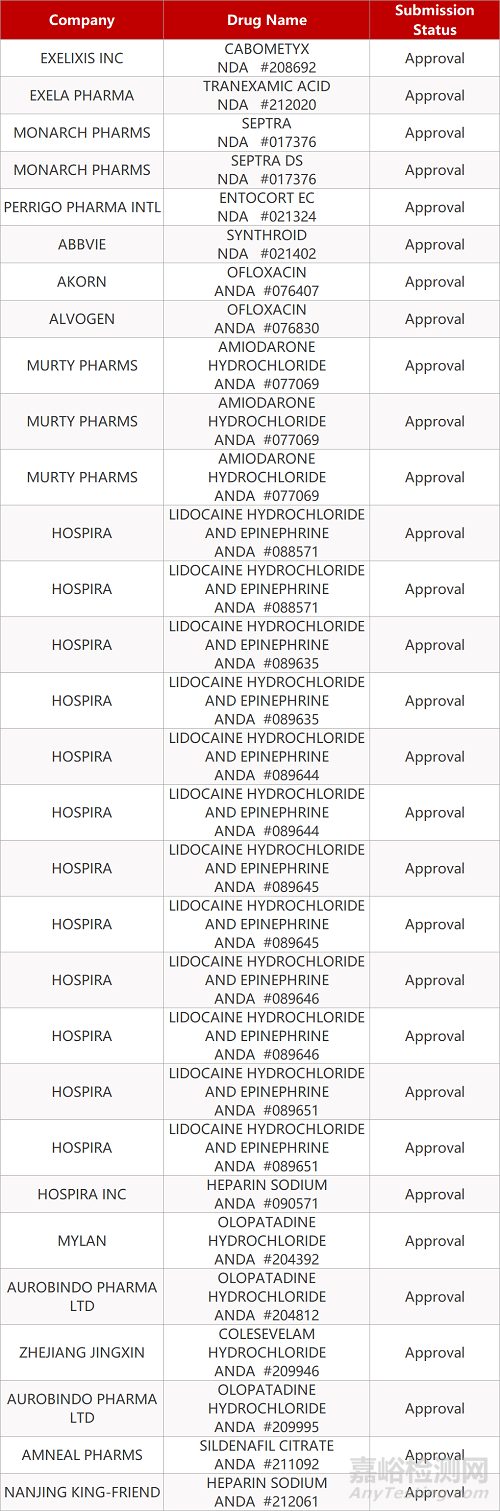
- The End -

来源:药研发


