您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-12-08 16:54
变异毒株奥密克戎(B.1.1.529)的出现再次将人们的视线拉回全球新冠疫情。该变异株包含大量突变,比现在的主流病毒德尔塔传播性更高,且很有可能令现在大部分疫苗效力降低,导致人体再次感染病毒的风险增加。据世界卫生组织(WHO)统计,截至2021年12月3日,全球COVID-19确诊2.63亿人,523.2万人死亡。截至2021年12月2日,全球已接种78.64亿剂疫苗。当前,全球各国正大力推动新冠疫苗的开发。整体疫苗研制进展如何?下面我们一看究竟。
1中国、美国、欧盟均有3-4款疫苗批准上市
截至2021年11月30日,中国、美国以及欧盟地区上市疫苗达到11款,其中中国药监局(NMPA)附条件批准上市4款,美国药监局(FDA)授权紧急使用3款(Authorized for Emergency Use, EUA),欧盟药监局(EMA)授权使用(Authorised for use)4款。中国疫苗为灭活疫苗和腺病毒载体疫苗,以灭活疫苗为主;美国疫苗为mRNA疫苗和腺病毒载体疫苗,以mRNA疫苗为主;欧盟批准了美国疫苗在欧洲地区的应用之外,还批准了阿斯利康(AstraZeneca)的腺病毒载体疫苗。
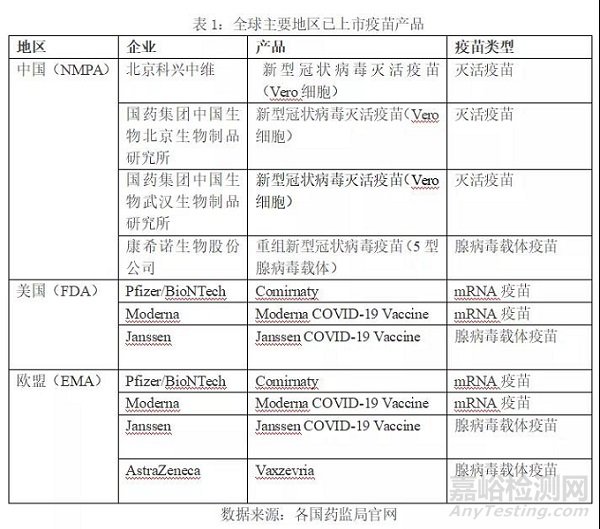
2全球新冠疫苗研发管线近330款,130余款进入临床阶段
据WHO统计,截至2021年11月26日,全球共开展326款新冠疫苗研发,其中132款已经进入临床阶段。进入临床阶段的产品主要集中在phase1、phase1/2等临床早期阶段,占比达到56%;处于phase3阶段的产品28个,有望在未来1-2年内上市。
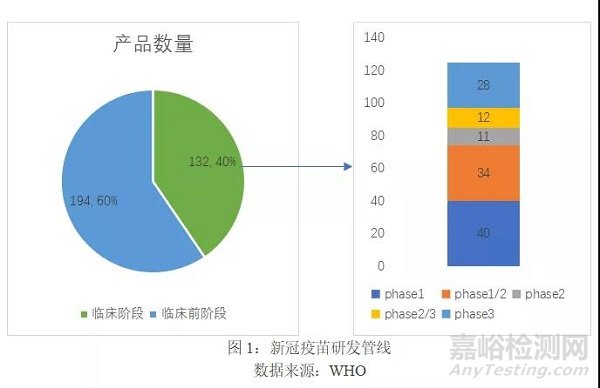
3临床阶段管线以蛋白亚单位疫苗居多,核酸疫苗、病毒载体疫苗以及灭活疫苗也有较多布局
进入临床阶段的候选疫苗类型主要是蛋白亚单位疫苗(Protein subunit),有47款之多;mRNA疫苗、病毒载体疫苗、灭活疫苗、DNA疫苗也有较多布局,处于临床阶段数量分别为21、19、17和15。从临床阶段产品类型来看,未来新冠疫苗的研发焦点集中在蛋白亚单位疫苗和核酸疫苗(包括mRNA疫苗和DNA疫苗)。
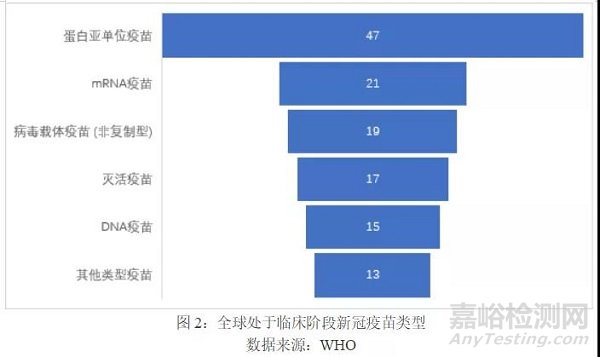
4接种程序以两剂次为主,间隔时间多选择三周或四周
进入临床阶段的候选疫苗接种程序以两剂次为主,共82款候选疫苗,占比62%;一剂次候选疫苗20款,占比15%;三剂次仅有1款疫苗。另外,有29款疫苗目前尚未确定接种程序。二剂次候选疫苗中,时间间隔常设为14天、21天和28天,数量占比分别为9%、40%和51%。
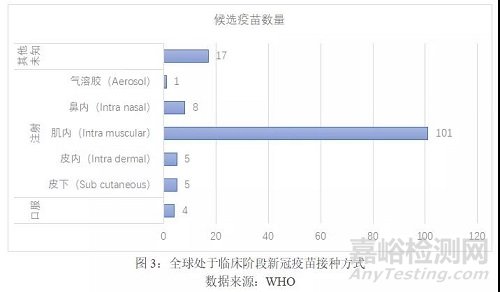
5接种方式以肌肉注射为主,探索鼻内、口服等新型给药方式
进入临床阶段的候选疫苗接种方式以注射为主,共111产品,占比84%;4款创新型口服疫苗,占比3%;另外有17款疫苗尚未确定接种方式。在注射疫苗中,肌肉注射方式的疫苗类型最多,共101款,占注射类疫苗的比重为90%;鼻内有8款;皮内注射和皮下注射疫苗各有5款;气溶胶疫苗1款。
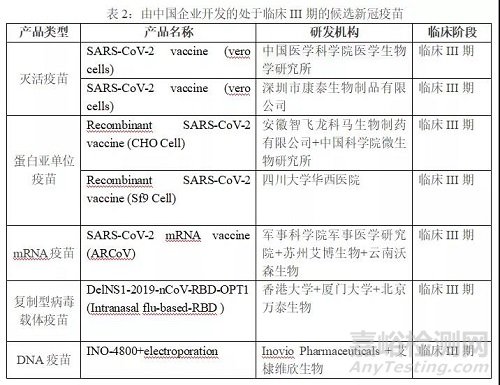
6多款处于III期临床的候选新冠疫苗来自中国机构
当前,处于临床III期阶段的新冠疫苗共28款,以以蛋白亚单位、灭活和核酸疫苗为主,分别有13款、6款和5款,三者合计占比85%。其中,由中国企业申报的产品达到7款,占比25%,涉及多条技术路线的产品。
在灭活疫苗方面,中国医学科学院医学生物学研究所、康泰生物分别将各自研发的产品推进到临床III期阶段。
在蛋白亚单位疫苗方面,四川大学华西医院研制出Recombinant SARS-CoV-2 vaccine (Sf9 Cell),该疫苗利用昆虫细胞在培养液中大量繁殖,将新冠病毒的基因引入昆虫细胞,该细胞作为工厂生产出高质量的重组疫苗蛋白,并进行精致纯化,该技术易于大规模生产投入市场;安徽智飞龙科马生物制药有限公司和中国科学院微生物研究所联合研制的Recombinant SARS-CoV-2 vaccine (CHO Cell),该疫苗以新冠病毒S蛋白的受体结合域(RBD)为靶点,通过重组表达RBD蛋白,诱导人体产生中和抗体,从而阻断新冠病毒与宿主细胞表面受体ACE2结合,达到预防感染的目的。
在核酸疫苗方面,中国人民解放军军事科学院军事医学研究院、苏州艾博生物科技有限公司与云南沃森生物技术股份有限公司共同研制出新型冠状病毒mRNA疫苗(ARCoVax),与BNT162b2(德国BioNTech公司与辉瑞合作研发)和mRNA-1273(美国Moderna公司研发)苛刻的储运温度相比(BNT162b2需要摄氏零下-70度,mRNA-1273需要摄氏零下-20度),ARCoV疫苗可在2-8摄氏度环境下保存。美国生物制药上市公司Inovio Pharmaceuticals和中国苏州创新药研发企业艾棣维欣生物制药(Advaccine Biopharmaceuticals)联合开发的DNA疫苗INO-4800+electroporation 已经进入临床III期, INO-4800已有的研究结果显示,所有受试年龄组志愿者均对疫苗呈现出良好的耐受性和免疫原性,并产生平衡的中和抗体和良好的T细胞反应(包括CD8和CD4),INO-4800对已测试的新冠病毒突变株也有广泛的交叉免疫反,INO-4800无需冷链或超冷链运输,可以在室温下储存一年以上。
在病毒载体疫苗方面,厦门大学、香港大学、北京万泰共同研制的鼻喷流感病毒载体新冠肺炎疫苗DelNS1-2019-nCoV-RBD-OPT1,已经进入临床III期,该疫苗是在双重减毒的普通季节性流感病毒载体内插入新冠病毒刺突蛋白基因片段研制而成的活病毒载体疫苗,通过模拟呼吸道病毒天然感染途径激活局部免疫应答和全身性免疫应答而发挥保护作用。
7结语
全球新型冠状病毒的大流行激发各国开展“疫苗军备竞赛”,330多个研发管线不断向前推进。中国处于新冠疫苗研发的第一梯队,在核酸疫苗、病毒载体疫苗、蛋白亚单位疫苗、灭活疫苗等多个技术平台进行科研攻关,不断将各类疫苗推进到防疫第一线。全球应该加强防疫合作,在疫情监测、技术攻关、临床试验和疫苗分发使用上一致行动,为最终战胜疫情贡献合力。

来源:艾美达行业研究


