您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-08-24 11:06
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
信立泰ARNi类新药上高血压III期临床。信立泰自主研发的ARNi类小分子化药S086片在用于治疗轻、中度原发性高血压患者的III期临床完成所有患者入组。ARNi类药物是血管紧张素受体-脑啡肽酶双重抑制剂,能同时阻断肾素-血管紧张素系统中的血管紧张素受体和脑啡肽酶,从而发挥舒张血管、抑制交感神经等作用。S086目标适应症为高血压和慢性心衰,目前这两种适应症均处于III期临床开发阶段。
国内药讯
1.上海医药FIC单抗获批乳腺癌II期临床。上海医药旗下上海交联申报的B013注射剂获CDE临床试验默示许可,拟开展II期临床用于一线治疗局部晚期或转移性三阴性乳腺癌患者。B013注射剂是Oncternal公司开发的一款治疗用重组单抗1类新药,上海医药拥有该新药在大中华区域的独家开发和商业化授权。据悉,全球范围内尚无同靶点的单抗药物进入临床阶段。
2.齐鲁第四代EGFR抑制剂获批临床。齐鲁制药第四代EGFR抑制剂QLH11811获CDE临床许可,适应症为具有EGFR等驱动基因异常的晚期非小细胞肺癌。公布于2022ACCR年会上的临床前结果显示,QLH11811在野生型EGFR、激活突变ex19del以及多种组合型耐药突变中的活性均优于第三代抑制剂osimertinib,并且针对L858R/C797S组合突变活性最高。目前全球共9款靶向C797S突变的EGFR抑制剂进入临床阶段。
3.康方PD-1/LAG-3双抗报IND。康方生物治疗用生物制品1类新药AK129注射液的临床试验申请获CDE受理。AK129是一款PD-1/LAG-3双抗药物,可阻断PD-1与其配体PD-L1和PD-L2的结合,以及阻断LAG-3与其配体MHCII等的结合,解除肿瘤微环境中的免疫抑制。公布在AACR 2022年会上的临床前研究结果显示,AK129可有效抑制肿瘤生长,较其他LAG-3抑制剂显示出更好的抗肿瘤活性。
4.优卡迪CAR-T报淋巴瘤IND。上海优卡迪生物开发的CAR-T产品“U16注射液”临床试验申请获CDE受理(受理号:CXSL2200375)。U16是一款针对非霍奇金淋巴瘤开发的CAR-T产品,相关靶点尚未透露。优卡迪专注于CAR-T等细胞/基因治疗技术和产品的创新,目前已成功推出多款创新型CAR-T产品。今年7月,该公司CD19靶向ssCART-19细胞注射液获得FDA授予孤儿药资格,用于治疗急性B淋巴细胞白血病(B-ALL)。
5.宜明昂科CD47/PD-L1双抗报IND。宜明昂科IMM2520注射液的临床试验申请获CDE受理。IMM2520是一款CD47/PD-L1双抗,通过阻断SIRPα/CD47和PD1/PD-L1的信号通路,从而解除肿瘤细胞对巨噬细胞和T细胞的免疫抑制,并通过基因工程改造的Fc片段结合Fcγ受体诱导抗体依赖的细胞介导的细胞毒作用(ADCC)和抗体依赖的细胞介导的吞噬作用(ADCP)。在临床前研究中,IMM2520在过表达CD47和PD-L1 CT26小鼠肿瘤模型中显示出抗肿瘤活性。
6.翰森引进新冠口服小分子全球开发权利。翰森制药发布公告,旗下公司翰森(上海)与北京华益健康药物研究中心(又名为全球健康药物研发中心,GHDDI)签署独家许可与合作开发协议,获得后者新冠口服小分子候选药物3CL蛋白酶抑制剂GDI4405在全球开发、生产及商业化的独家权利。根据协议,GHDDI将获得1200万元首付款及最多人民币16.8亿元的开发、注册及基于销售的商业化里程碑潜在付款,以及产品的销售分成。
国际药讯
1.辉瑞/BioNTech二价新冠疫苗在美报EUA。辉瑞与BioNTech联合开发的Omicron BA.4/BA.5二价新冠mRNA疫苗已向FDA提交紧急使用授权(EUA)申请,用于12岁及以上人群预防接种。目前,Omicron BA.4/BA.5是美国流行的主要变异株。这款二价疫苗包含编码原始新型冠状病毒刺突蛋白的mRNA,以及编码Omicron BA.4/BA.5变异株刺突蛋白的mRNA。研究表明,二价疫苗对原始野生株、Omicron BA.1、BA.2和BA.4/BA.5变异株均能产生强烈的中和抗体反应。
2.抗真菌新药雷扎芬净在欧盟报产。欧洲药品管理局受理Mundipharma与Cidara公司开发的新型棘白菌素雷扎芬净(rezafungin)的营销授权申请(MAA),用于治疗成年侵袭性念珠菌病患者。rezafungin具有较长的半衰期,可每周给药1次。在Ⅲ期临床ReSTORE中,rezafungin治疗组在系统治愈率方面非劣效于卡泊芬净组。该新药已于上月在美国递交新药申请(NDA)。
3.诺和诺德双机制降糖复方Ⅱ期临床积极。诺和诺德双重机制复方CagriSema用于治疗2型糖尿病的Ⅱ期临床结果积极。CagriSema由长效胰淀素类似物cagrilintide和GLP-1受体激动剂司美格鲁肽组成。该项试验32周治疗数据显示,CagriSema、司美格鲁肽与cagrilintide三个治疗组患者HbA1c数值分别下降2.18、1.79与0.93个百分点,患者体重分别下降15.6%、5.1%与8.1%。CagriSema的安全性与耐受性良好。诺和诺德计划明年启动Ⅲ期临床。
4.CD30-CAR-T联合PD-1抗体上Ⅰb期临床。Tessa公司自体CD30-CAR-T疗法TT11联合PD-1抗体nivolumab用于二线治疗复发/难治性CD30阳性经典霍奇金淋巴瘤(cHL)的Ⅰb期开放标签试验完成首例患者的给药。正在进行的Ⅱ期CHARIOT试验结果显示,TT11在14例可评估的复发或难治性cHL的患者中达到57.1%的完全缓解(CR)率和71.4%的总缓解率(ORR)。此外药物的总体安全性良好。
5.ANGPTL3靶向单碱基编辑疗法临床前研究积极。Verve公司基于脂质纳米颗粒(LNP)的单碱基编辑疗法VERVE-201临床前研究结果积极。VERVE-201旨在通过对ANGPTL3基因进行编辑以永久性关闭ANGPTL3(肝脏中胆固醇和甘油三酯代谢的关键调节因子)的表达,拟开发用于治疗家族性高胆固醇血症或粥样动脉硬化患者。在非人灵长类临床前动物实验中,VERVE-201能够将血液中的ANGPTL3蛋白水平降低超过90%并且维持2年。该公司预计2024年将这款疗法推进至临床开发。
6.GnRH拮抗剂撤回美国NDA。由于无法在PDUFA日期(2022年9月13日)前解决FDA针对GnRH拮抗剂linzagolix上市申请(NDA)提出的问题,ObsEva公司日前撤回了linzagolix的NDA申请,并终止与Kissei公司关于linzagolix的许可协议,将该药物的相关权益退回给Kissei公司。linzagolix是一款口服小分子新药,今年6月已获欧盟批准上市,用于子宫肌瘤相关的严重月经出血。葆正医药拥有linzagolix的中国权益。该新药目前正在日本和中国进行治疗子宫内膜异位症相关疼痛的III期临床。
医药热点
1.儿童脑科学与脑健康促进专委会成立。中国妇幼保健协会儿童脑科学与脑健康促进专业委员会8月20日正式成立,北京大学公共卫生学院教授王晓莉担任首届专委会主任委员。儿童脑科学与脑健康促进专委会将作为构建妇幼保健系统儿童脑科学与脑健康专业人才交流的平台,促进儿童脑科学与脑健康人才队伍发展、科研教学水平以及诊疗服务技术的持续性提升,推动妇幼保健系统儿童脑疾病与脑健康专科建设,在全面促进儿康行业发展上发挥重要作用。
2.欧盟同意猴痘疫苗“一拆五”注射法。欧盟监管机构欧洲药品管理局19日宣布,鉴于丹麦巴伐利亚北欧公司生产的猴痘疫苗供应量有限,欧洲国家可以考虑减小疫苗单次接种剂量以扩大接种范围,减量接种对预防感染同样有效。欧洲药管局建议采用“一拆五”注射法,即个体接受两次猴痘疫苗皮内注射,接种间隔约4周,单次接种剂量为原剂量的五分之一。
3.福奇宣布卸任NIAID主任。8月22日,Anthony S. Fauci, MD(福奇博士)宣布将于12月从美国国家过敏症和传染病研究所(NIAID)主任职位卸任,但依然是NIAID的PI。NIAID是美国国立卫生研究院(NIH)下属的27个研究所/中心之一。福奇博士从1984年当NIAID主任开始,已给7届总统做过医学顾问;尤其是在80年代末90年代初HIV流行的时候,他是HIV防治领域最有名的公众人物,还获得了美国公民最高奖总统自由勋章。
评审动态
1. CDE新药受理情况(08月23日)
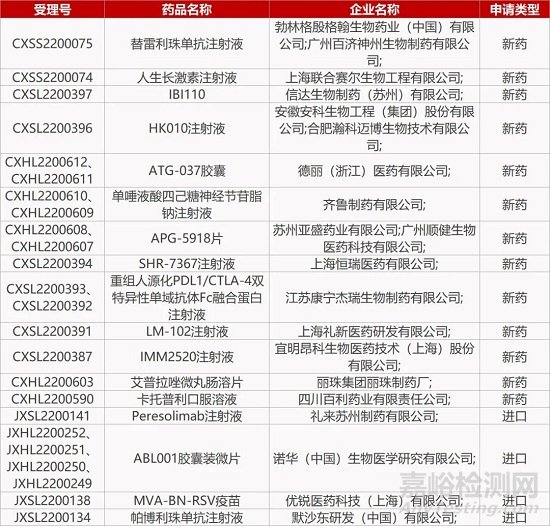


来源:药研发


