今日头条
深圳赛岚肿瘤表观遗传疗法获批临床。赛岚医药宣布其基于新一代表观遗传机理研发的潜在“first-in-class”抗肿瘤候选药物CTS2190胶囊获FDA临床试验许可,即将开展Ⅰ期临床评估用于晚期实体瘤患者的安全性与初步疗效。在临床前研究中,CTS2190已显示出对多种实体瘤和血液瘤的细胞、CDX、PDO和PDX模型的有效抑制效果,而且具有良好的药代动力学和安全性,有望为肿瘤治疗提供有力的创新手段。
国内药讯
1.武汉滨会溶瘤病毒拟纳入突破性治疗品种。滨会生物1类生物制品重组人GM-CSF溶瘤II型单纯疱疹病毒(OH2)注射液(Vero细胞)获CDE拟纳入突破性治疗品种,针对适应症为:经至少二线以上标准治疗失败的不能手术切除或转移性的黑色素瘤患者。该产品可选择性感染肿瘤细胞并在其中复制,最终裂解、杀死肿瘤细胞,并释放出抗原物质诱导特异性抗肿瘤免疫反应。在美国,FDA已授予该新药孤儿药资格,用于治疗IIb期至IV期黑色素瘤。
2.卫材&渤健Aβ单抗拟纳入优先审评。卫材与渤健联合开发的1类新药仑卡奈单抗注射液的上市申请获国家药监局拟纳入优先审评,拟用于治疗早期阿尔茨海默病(AD)。仑卡奈单抗(lecanemab,BAN2401)是一款抗淀粉样蛋白(Aβ)原纤维抗体,已在今年1月获FDA批准用于治疗AD。两项Ⅲ期临床(EMERGE和ENGAGE)扩展研究显示,aducanumab治疗两年后能持续降低患者大脑中的Aβ水平和血浆中的p-tau181水平。
3.歌礼PD-L1单抗慢性乙肝II期临床积极。歌礼制药皮下注射PD-L1抗体恩沃利单抗(ASC22)治疗慢性乙型肝炎的最新临床数据公布于亚太肝脏研究协会2023年年会上。24周治疗数据显示,在基线HBsAg≤100 IU/mL的患者亚组中,42.9% (3/7)的患者在治疗期间实现了HBsAg清除(HBsAg低于检测下限,即LLOQ<0.05 IU/mL),并在24周或41周随访结束时保持HBsAg清除,显示ASC22具有慢乙肝功能性治愈潜力。ASC22总体耐受性良好。
4.尚健CLDN18.2/CD47双抗获批临床。尚健生物自研创新CLDN18.2/CD47双抗SG1906注射液获国家药监局批准临床,拟开发用于CLDN18.2阳性晚期恶性实体肿瘤。SG1906能同时特异性结合CLDN18.2和CD47分子,介导ADCC、ADCP以及通过阻断CD47和SIRPα相互作用,具有协同抗肿瘤效应。在CLDN18.2中低表达的PDX肿瘤模型中,SG1906显示出积极的抑瘤效果,未见明显的靶点相关不良反应。2022年10月,FDA已批准该新药在美国开展临床试验。
5.博奥明赛IgG1单抗报乙肝IND。博奥明赛1类生物制品BM012注射液的临床试验申请获得CDE受理。BM012是一种具有多重机制抗乙肝病毒(HBV)的IgG1全人源单克隆抗体药物,已在临床前研究显示出比同类产品 (Vir3434) 更好的抑制S抗原的活性以及抗病毒药效,并在GLP毒理研究中展示出良好的安全性。BM012注射液的首个适应症为慢性乙型肝炎病毒感染。
国际药讯
1.首个IgA肾病非免疫抑制疗法获批上市。Travere公司内皮素/血管紧张素受体拮抗剂(DEARA)Filspari(sparsentan)获FDA加速批准上市,用于在有高风险出现疾病进展的IgA肾病患者中降低蛋白尿。在一项Ⅲ期PROTECT研究中,sparsentan治疗组36周后患者蛋白尿较基线平均减少49.8%,活性对照组平均减少15.1%(p<0.0001)。Filspari也是FDA批准针对IgA肾病的首个非免疫抑制疗法。
2.首款AM酶替代疗法获批上市。Chiesi Global Rare Diseases公司重组人α-甘露糖苷酶Lamzede(velmanase alfa-tycv)获FDA批准上市,用于治疗α-甘露糖苷贮积症(AM)的非中枢神经系统表现。Lamzede也是FDA批准针对该疾病的首款酶替代疗法,旨在提供或补充天然α-甘露糖苷酶,以降解富含甘露糖的寡糖并防止其在体内各种组织中蓄积。2018年3月,欧盟委员会已批准Lamzede用于治疗轻中度AM患者的非神经系统表现。
3.眼科双环肽疗法获批治疗GA。Apellis公司靶向补体C3的聚乙二醇化双环肽疗法Syfovre(pegcetacoplan)获FDA批准,用于治疗由年龄相关性黄斑变性(AMD)引起的地图样萎缩(GA)。来自III期DERBY和OAKS研究的24个月疗效数据显示,每个月或每两个月一次的pegcetacoplan治疗,皆具一致性的疗效与安全性。2021年5月,pegcetacoplan已获得FDA批准上市,用于治疗阵发性睡眠性血红蛋白尿症(PNH)。
4.K药联合化疗治疗胃癌III期临床积极。默沙东PD-1抑制剂Keytruda联合PF(5-氟尿嘧啶+顺铂)或CAPOX(卡培他滨+奥利沙铂)一线治疗HER2阴性晚期胃癌或胃食管交界处 (GEJ) 腺癌的III期KEYNOTE-859结果积极。中位随访为31.0个月时,Keytruda组患者的OS较安慰剂组显著延长(12.9vs11.5个月),死亡风险降低22%(HR=0.78;95% CI, 0.70-0.87;P<0.0001);两组患者PFS(6.9vs5.6个月)和DOR(8.0vs5.7个月)显著延长,疾病进展或死亡风险降低24%;两组3-5级治疗相关不良事件(TRAEs)发生率亦相似。
5.Moderna公布四价流感疫苗III期数据。Moderna公司公布季节性流感mRNA疫苗mRNA-1010在成年人中开展的关键III期临床中期结果。与传统疫苗相比,mRNA-1010在甲型H1N1和甲型H3N2的血清转化率上取得优效结果,在H3N2的几何平均滴度比上也具有优效性,在H1N1的几何平均滴度比上具有非劣效性。但在乙型Victoria和乙型Yamagata的血清转化率和抗体滴度方面则均未达到非劣效性。mRNA-1010与传统疫苗的不良反应发生率分别为70%和48%。
6.OSE公司癌症疫苗获批注册性III期临床。OSE公司宣布癌症疫苗Tedopi同时获得FDA和EMA同意开展关键性III期临床,用于二线治疗HLA-A2阳性晚期非小细胞肺癌(NSCLC)。此前,Tedopi已在三线治疗NSCLC患者的III期临床中获得积极结果。结果显示,与标准治疗(SOC)相比,Tedopi组患者的1年OS率更高(44.4%vs27.5%);3-5级治疗期间不良事件(TEAE)发生率更低(11%vs35%)。
医药热点
1.广东乡村医生每人每年补贴2万元。近日,广东高度重视基层医疗卫生服务能力建设,陆续出台政策、加大投入。广东省卫健委已推动下发4.8亿多资金,用于2023年在岗、离岗村医的补助。无论是持有执业(助理)医师证书,还是乡村医生执业证书,只要在村卫生站工作,均可领取补贴,补贴标准为乡村医生每人每年2万元。
2.广州构建居家腹膜透析治疗体系。近日,由广东省广州市卫健委主办、南方医科大学南方医院承办的广州市居家腹膜透析治疗示范体系建设项目在南方医院举行试点单位授牌活动。该项目为卫生健康领域重点发展的“院士工程”,安排专门资金推动,旨在探索社区肾脏替代治疗广覆盖。该项目吸纳了21家医疗卫生机构参与,包括1个项目示范中心(南方医院),3个分中心(中山大学孙逸仙纪念医院、广州医科大学附属第一医院、广州市第一人民医院),以及17家基层医疗卫生机构。
3.吉林打造四级临床重点专科。近日,吉林省卫健委出台《吉林省临床重点专科建设“十四五”规划》,提出到2025年,力争建设国家临床重点专科50个、省级临床重点专科50个、市级临床重点专科110个、县级临床重点专科210个,形成资源均衡、分工协作、纵向贯通、横向联通的临床专科服务体系。
评审动态
1. CDE新药受理情况(02月18日)
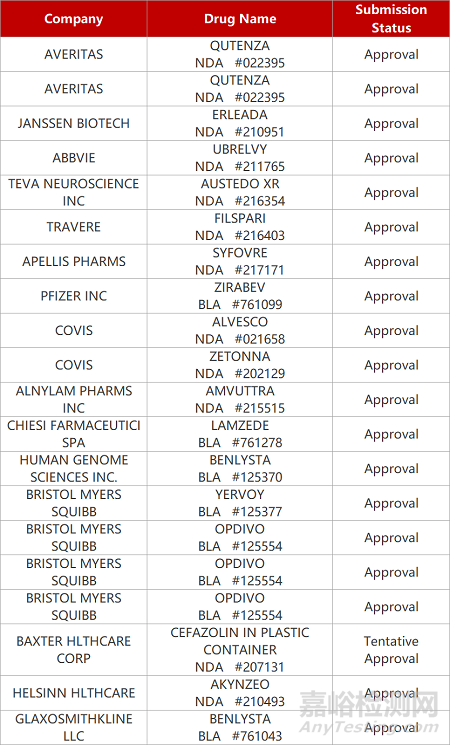
2. FDA新药获批情况(北美02月17日)
 ..
..


 ..
..


