今日头条
恒瑞FIC支气管扩张症新药获批临床。恒瑞医药子公司瑞石生物开发的1类化药RSS0343片获国家药监局临床默示许可,拟开发用于治疗非囊性纤维化支气管扩张症患者。RSS0343是一款口服共价可逆小分子抑制剂,具有很强的抑制炎症和防止相关组织损伤的作用,有望为多种慢性自身免疫或炎症性疾病的患者提供具有新治疗机理的口服疗法。目前,国内外尚无同类药物获批上市。
国内药讯
1.传奇/杨森CAR-T疗法Ⅲ期临床积极。杨森与传奇生物联合开发的BCMA靶向CAR-T疗法Carvykti在治疗复发/难治性多发性骨髓瘤(RRMM)的Ⅲ期临床CARTITUDE-4最新数据积极。在中位随访为16个月时,Carvykti与标准治疗相比,降低疾病进展风险74%;Carvykti组的中位PFS尚未达到,标准治疗组的中位PFS为12个月。安全性方面,97%接受Carvykti治疗的患者报告出现严重不良事件,包括94%的患者出现血细胞计数降低,76%的患者出现免疫相关毒性。
2.GSK启动ASO疗法慢性乙肝中国Ⅲ期临床。葛兰素史克反义寡核苷酸(ASO)疗法GSK3228836(bepirovirsen)在中国登记启动一项国际Ⅲ期临床,拟评估Bepirovirsen用于治疗核苷(酸)类似物经治的HBeAg阴性慢性乙型肝炎病毒感染受试者的有效性和安全性。该项研究的中国部分将由南方医科大学南方医院侯金林主任医师牵头并担任主要研究者。此前,GSK3228836已被CDE纳入用于治疗慢性乙肝的突破性治疗品种。
3.泽璟LAG-3/TIGIT双抗获批临床。泽璟制药1类生物制品注射用ZGGS15获国家药监局临床试验默示许可,拟用于晚期实体肿瘤的治疗。ZGGS15是一款LAG-3/TIGIT双特异性抗体,已在临床前动物模型中显示出单药治疗的抗肿瘤增殖作用,且ZGGS15和PD-1抗体联合具有比LAG-3单抗或TIGIT单抗与PD-1抗体联合更好的协同增强抗肿瘤增殖的作用。在非人灵长类动物中,ZGGS15也显示出良好的药代动力学特征及安全性特征。
4.百利天恒CD33靶向ADC获批临床。百利天恒宣布其自研1类生物制品注射用BL-M11D1(CD33-ADC)获国家药监局临床默示许可,即将开展用于复发或难治性急性髓系白血病患者的I期临床试验。该公司同时宣布,EGFR/HER3双抗ADC创新药BL-B01D1的联合用药临床研究也获得国家药监局批准,即将开展联合甲磺酸奥希替尼片治疗EGFR突变的局部晚期或转移性非小细胞肺癌患者的临床试验。
5.安斯泰来CLDN18.2/CD3双抗中国报IND。安斯泰来与Xencor联合开发的CLDN18.2/CD3双抗ASP2138的临床试验申请获CDE受理。ASP2138旨在通过与CLDN18.2和CD3的选择性结合导致的T细胞激活,对表达CLDN18.2的肿瘤细胞产生细胞毒性从而达到治疗作用。在临床前研究中,ASP2138已在NOG小鼠模型中显示出对表达CLDN18.2的胃癌的抗肿瘤作用。该新药拟开发用于治疗CLDN18.2阳性的胃或胃食管交界处腺癌、胰腺癌。
国际药讯
1.美敦力胰岛素皮下泵获批上市。美敦力(Medtronic)模拟胰腺生理性分泌胰岛素的胰岛素皮下输注装置MiniMed 780G系统获FDA批准上市,用于7岁以上的1型糖尿病患者每5分钟自动调整和纠正血糖水平,为患者提高满足需求的胰岛素(包括基础状态及餐时血糖)。该系统结合新的Guardian 4传感器和灵敏监测(SmartGuard)技术,并使用有助于减少胰岛素防腐剂损失的创新材料,可使用长达7天,降低输液器闭塞的风险。
2.舒巴坦/度洛巴坦复方获FDA推荐批准。FDA抗菌药物咨询委员会(AMDAC)推荐批准Entasis公司(已被Innoviva收购)复方抗生素舒巴坦钠-度洛巴坦钠(SUL-DUR)上市,用于治疗由鲍曼不动杆菌-醋酸钙复合体(不动杆菌)的敏感菌株引起的成人医院获得性细菌性肺炎和呼吸机相关性细菌性肺炎。在III期ATTACK研究中,与多黏菌素相比,SUL-DUR治疗使碳青霉烯耐药ABC感染患者的28天全因死亡率更低(19%vs32.3%)。再鼎医药拥有该新药在大中华区的独家授权。
3.Incyte公司CD19抗体长期疗效积极。MorphoSys和Incyte联合开发CD19抗体tafasitamab在AACR2023年会上公布其联合来那度胺用于治疗复发/难治性弥漫性大B细胞淋巴瘤(R/R DLBCL)的Ⅱ期研究L-MIND五年随访结果。数据分析显示,联合治疗达到57.5%的总缓解率(ORR);中位随访44个月,中位持续缓解时间(DOR)尚未达到;中位总生存期为33.5个月,中位无进展生存期为11.6个月;研究期间没有发现新的安全事件。
4.诺华前列腺癌放射配体疗法扩产。FDA批准诺华位于新泽西州米尔本的工厂生产放射性配体疗法Pluvicto,供美国商业使用,用于PSMA阳性转移性去势抵抗性前列腺癌三线治疗。Pluvicto是全球首款靶向PSMA的放射性配体疗法,上市9个月的营收达到2.71亿美元。此前,诺华一直从意大利的一家工厂供应这种放射疗法。诺华的目标是到2024年及以后每年至少供应25万剂的Pluvicto。
5.新型AAV基因疗法CD早期临床积极。Myrtelle公司靶向大脑中少突胶质细胞的基因疗法rAAV-Olig001-ASPA在治疗儿童致命遗传性脑疾病Canavan disease(CD)的Ⅰ/Ⅱ期临床结果积极。rAAV-Olig001-ASPA旨在通过重组腺相关病毒(rAAV)载体将治疗性ASPA基因直接传递给少突胶质细胞,以恢复少突胶质细胞产生髓磷脂的功能。数据显示,8例CD患者在接受治疗后6个月获得积极的初步疗效和良好的安全性。
6.补体创新药物公司Complement完成A轮融资。Complement公司宣布完成由Gimv和Forbion共同领投的7200万欧元的A轮融资,以用于推进其用于治疗由于干性年龄相关性黄斑变性(AMD)引起黄斑地图样萎缩(GA)的创新AAV基因疗法CTx001的开发,并完成Ⅰb期临床试验。此轮融资还将用于评估该公司非眼科适应症管线的产品、并进一步开发新型补体精准医学(CPM)平台。
医药热点
1.新版国家儿童肿瘤监测年报发布。4月22日,国家儿童肿瘤监测中心编制的《国家儿童肿瘤监测年报(2022)》发布。《年报》显示,2019—2020年全国新发肿瘤患儿中,排名前三位的癌种分别为白血病(32.89%)、中枢神经系统肿瘤(15.18%)和淋巴瘤(9.71%);在新发肿瘤患儿各年龄组占比中,最高的是1~4岁组(30.59%)。
2.医学毕业生可免试注册乡村医生。4月21日,国家卫健委等五部门联合发布关于实施大学生乡村医生专项计划的通知,由各省专项招聘医学专业高校毕业生免试注册为乡村医生到村卫生室服务,并加大激励和保障力度,引导大学生乡村医生服务农村、扎根农村。从2020年起,国家卫健委在部分省份实施医学专业高校毕业生免试申请乡村医生执业注册政策,目前已累计有4300名大学生乡村医生进入村卫生室服务。
3.北京推动“城区医院进农村”。近日,北京市政府印发《关于做好2023年全面推进乡村振兴重点工作的实施方案》,其中要求提升基本公共服务能力,建立“城区医院进农村”专项帮扶机制,组织城市大医院对口支援农村基层医疗卫生机构。优化乡村医疗卫生机构布局,按照“村用、乡镇管、区统筹”原则推进乡村两级医疗卫生机构一体化管理,加强村卫生室运行保障和乡村医疗卫生队伍建设。
评审动态
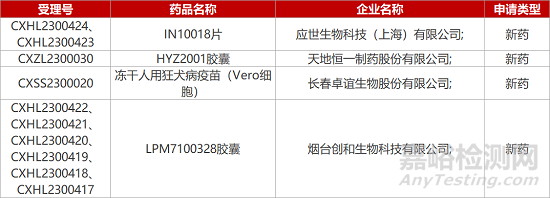
1. CDE新药受理情况(04月24日)
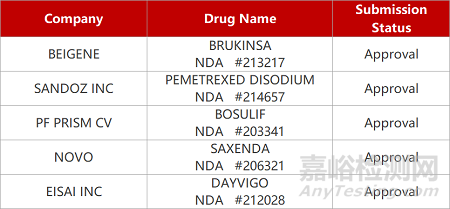
2. FDA新药获批情况(北美04月21日)