2023年8月10日,全球牙科和脊柱市场的领导企业 ZimVie Inc.(纳斯达克股票代码:ZIMV)宣布,美国食品和药品管理局(FDA)已批准其高度较小的 Mobi-C® 颈椎间盘假体。
4.5 毫米高的Mobi-C®获批FDA
ZimVie 的这款高度较小的 Mobi-C® 颈椎间盘可在七个特定位置与周围骨骼接触,既增强了稳定性,也将更好地适应美国患者群体的解剖结构。2004年,Mobi-C在法国完成首次植入,自此已有超过25个国家的患者选择该产品进行治疗。2013年,Mobi-C 成为首个获批FDA的颈椎间盘,用于治疗超过一个节段的颈椎疾病。
密歇根骨科解决方案诊所(PLLC)的脊柱外科医生 Jad G. Khalil 博士表示,这款最新获批的 4.5 毫米高的颈椎间盘植入物是对 Mobi-C 系列产品的重要补充。有了它,外科医生在应对严重塌陷的椎间盘时也能使用 Mobi-C 假体,并能够避免小关节过度牵拉。这将扩大颈椎间盘置换术的适应症,让更多的患者可以受益于这款临床表现优秀的 Mobi-C 颈椎间盘。
▲图片源自公司官网(下同)
加州大学戴维斯分校脊柱神经外科教授兼主任 Kee D. Kim 博士强调了此次获批的临床重要性。他表示,人工椎间盘尺寸不当可能会导致假体移位、下沉和节段性后凸等问题。生物力学研究数据表明,人工椎间盘高度哪怕只增加 1 毫米,其水平的运动范围都会减少约 50%。即使是 5 毫米高的人工椎间盘,对于某些患者来说也可能太紧。因此,FDA 此次批准了 4.5 毫米高的 Mobi-C 椎间盘对于患者来说是一个非常好的消息,也可以让外科医生更灵活地选择最合适的人工椎间盘。
ZimVie Spine 全球总裁 Rebecca Whitney 表示,4.5 毫米高度的 Mobi-C 获得FDA批准对于外科医生及其患者来说是一次胜利,也是对公司全球监管事务团队深思熟虑策略的验证。他们利用从欧盟研究中获得的真实世界临床证据,来展示产品长期效果的安全性和有效性,并确保 FDA 能够批准这款高度较低的椎间盘。公司很高兴能够为外科医生提供市场上最广泛的人工颈椎间盘(多种接触面积和高度选项),为患者保留运动功能。这款产品将于今年秋天在美国正式商业化推出。
关于 Mobi-C 颈椎间盘
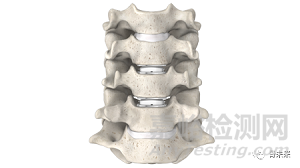
Mobi-C 是 FDA 批准的首个用于在单节段和双节段(C3-C7)重建颈椎间盘的颈椎间盘假体。Mobi-C 是一种钴铬合金和聚乙烯可旋转衬垫假体,可一步插入颈椎,无需凿骨或其他椎骨锚固,如使用螺钉或龙骨。
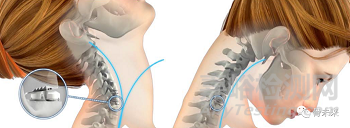
Mobi-C 颈椎间盘假体适用于骨骼成熟的患者,用于重建C3-C7节段椎间盘,一般在单节段或两个连续节段的椎间盘切除术后使用,治疗伴有或不伴有颈部疼痛或脊髓病的顽固性神经根病(手臂疼痛和/或神经功能缺损)。Mobi-C 颈椎间盘假体采用前路植入术式。
Mobi-C 颈椎间盘优势:
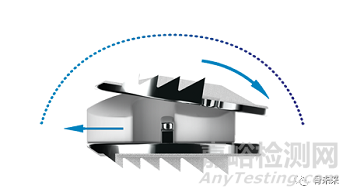
(一)采用可旋转衬垫
可旋转衬垫让颈椎间盘假体具有可控移动性,能够恢复颈椎的自然运动。获得专利的可旋转核心是Mobi-C灵活移动的基础。随着椎骨和颈部肌肉的运动,Mobi-C 植入物可以自由地左右扭转、滑动以及旋转。
▲图片源自公司官网(下同)
(二)实现骨保留
Mobi-C 的可旋转核心设计,在植入物与骨界面处产生的应力较低。Mobi-C的植入无需侵入性龙骨或螺钉,也不需要为准备龙骨而进行凿骨,省略了手术切割步骤。
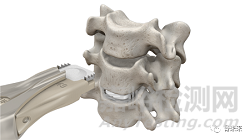
(三)易于插入颈椎
Mobi-C可实现一步插入。在插入Mobi-C颈椎间盘时,螺钉或龙骨置入避免了额外的暴露以及繁琐的手术步骤,无需钻孔或凿孔。
(四)可自我调整
Mobi-C颈椎间盘假体每一层的旋转中心都是可变的,并且会不断变化。该假体旨在通过其自动调节的可旋转核心来适应瞬时旋转轴。可旋转核心允许椎间盘上方和下方的椎骨移动,以保持正常的颈部运动。
关于 ZimVie
2022年3月,捷迈邦美(Zimmer Biomet)宣布将其牙科和脊柱业务剥离为ZimVie,作为独立上市子公司,并以股票代码为“ZIMV”在纳斯达克开始常规方式交易,其脊柱和牙科业务在全球拥有超过200亿美元的市场规模。
ZimVie专注于牙科和脊柱以及骨修复领域,包括种植牙、手术工具、骨移植替代品、脊柱融合植入物、非融合替代品和数字护理管理解决方案。
ZimVie公司2022年全年第三方净销售额为9.095亿美元,与2021年全年相比,按报告计算减少了9.8%,按固定汇率计算减少了6.8%。第三方牙科部门净销售额为4.597亿美元,减少了880万美元。第三方脊柱分部净销售额为4.498亿美元,减少了9050万美元。
2022年全年净亏损为6390万美元,与2021年全年净亏损(9533美元)相比减少了3140万美元,占第三方净销售额的7.0%。2022年全年调整后净收入为4790万美元,比上年增加 1080万美元。