一、前言导读
1、结构性心脏病概览
结构性心脏病是近年心血管疾病领域提出的一个新概念,2005年由德国法兰克福的Horst Sievert医生首先提出,泛指一大类先天性或获得性的以心脏和大血管结构异常为主要表现的心血管疾病,如传统定义的先天性心脏病、心脏瓣膜疾病和心肌病等。
广义的结构性心脏病是指除原发心电疾患(因某些电生理异常而发生的VT/VF)和循环疾病(部分高血压、稳定性心绞痛、ACS)以外,任何心脏结构的异常,任何与心脏和大血管结构有关的疾病。而狭义的结构性心脏病是指解剖异常引起的心脏结构改变所造成的心脏的病理生理变化。包括:(1)先天性心脏病:室间隔缺损(VSD)、房间隔缺损(ASD)、动脉导管未闭(PDA)等;(2)瓣膜病:二尖瓣、三尖瓣、主动脉瓣、肺动脉瓣等;(3)心肌病:肥厚性心肌病、扩张型心肌病、致心律失常型右室心肌病等;(4)心肌梗塞后室间隔穿孔、室壁瘤、疤痕心肌等。
在过去十年中,结构性心脏病的诊断及治疗取得了飞速发展,成为了当今心血管疾病领域的一大亮点,其未来发展引人瞩目。
根据弗若斯特沙利文的资料显示,被广泛视为针对瓣膜性心脏病高度有效疗法的介入式瓣膜手术在中国仍然供不应求,用于该等手术的经导管心脏瓣膜器械亦然。此问题影响了大量未能得到妥善治疗的病患,也为合格并致力于改变现状的医疗器械从业者带来了可观的商业机遇。
瓣膜性心脏病的特点为四个心脏瓣膜(即主动脉瓣、二尖瓣、三尖瓣及肺动脉瓣)中一个或多个瓣膜出现损伤或缺陷。在这几个瓣膜中,主动脉瓣控制心脏和主动脉之间的血液流动,从而控制通往身体其他部位的血管;二尖瓣和三尖瓣控制心房和心室之间的血液流动;而肺动脉瓣控制从心脏到肺的血液流动。正常运作的瓣膜可确保适当的血液流动,但瓣膜性心脏病会导致瓣膜变得太窄及硬化(狭窄)而无法完全开启,或无法完全闭合(反流)。下图显示了不同类型的瓣膜性心脏病。
在治疗方案选择方面,对于轻度和中度患者,一般疾病早期通过药物治疗延缓疾病的进展。对于重度患者则需要通过手术干预,因为瓣膜性心脏病是一个机械性病症,相当于心脏这个“泵”的“阀门”坏了,仅通过药物治疗效果有限。
2、主动脉瓣疾病介绍、治疗方法及市场规模
主动脉瓣疾病
1)主动脉瓣狭窄(AS):AS是主动脉瓣狭窄阻碍血流从左心室到主动脉,是一种进展性心血管疾病。一旦出现症状,需要进行外科换瓣术或介入换瓣术。
2)主动脉瓣反流(AR):AR是主动脉瓣闭合不完全导致心脏舒张时血液从主动脉倒流入左心室。AS患者也经常伴随AR症状,单纯性AR患者较少。
瓣膜置换术
1)经导管主动脉瓣膜置换术(TAVR /TAVI):是针对主动脉瓣膜疾病(尤其是AS)患者外科手术不耐受情况下的主要治疗方法;TAVR作为一种介入治疗技术,其最大特点是无需开胸、主要通过经股入路完成主动脉瓣膜置换术。
2)TAVR定义及手术过程:传统开胸手术需要在全身麻醉和体外循环支持下开胸换瓣,30%-50%的主动脉瓣膜病患者身体无法耐受。TAVR是指通过血管/心尖作为入路,将组装完备的人工主动脉瓣经导管置入到病变的主动脉瓣处,在功能上完成主动脉瓣的置换。TAVR作为一种微创介入治疗手段,具有手术风险低、高危患者耐受性强的优势,目前已成为未来心脏瓣膜治疗方法的发展趋势。
TAVR示意图
市场规模
根据弗若斯特沙利文的统计,中国2020年主动脉瓣狭窄和主动脉瓣反流的患者数分别为440万人和390万人,预计到2030年上述两类疾病的患病人数将分别达到520万人和460万人,2020年至2025年的复合增长率分别为2.2%、2.4%。
2、二尖瓣疾病介绍、治疗方法及市场规模
二尖瓣反流
二尖瓣常见疾病为二尖瓣反流(MR)及二尖瓣狭窄(MS), 其中二尖瓣反流是一种可由多种病因导致、以收缩期血流由左心室反流至心房为特征的瓣膜性心脏病。MR患者占所有二尖瓣反流疾病患者65%,约占所有心脏瓣膜疾病的50%,未经治疗的MR患者1年和5年死亡率分别为20%和50%。
二尖瓣反流主要包括 DMR(原发性二尖瓣反流)和 FMR(功能性二尖瓣反流):其中FMR占MR总数的3/4。在临床诊疗指南中依据 Carpentier分型,根据二尖瓣活动度将MR分为TypeI(正常)、TypeII(过度)和TypeIII(受限)。
经导管二尖瓣修复及置换
1.经导管二尖瓣修复术(TMVr)
根据技术原理可以分为以下几类:
1)经导管缘对缘二尖瓣修复术(TEER),代表产品包括MitraClip和PASCAL系统;
2)经导管间接二尖瓣环成形术(Carillon系统);
3)经导管二尖瓣人工腱索的置入(NeoChord);
4)经导管直接瓣环成形术(Cardioband系统和Mitralign)。
2.经导管二尖瓣置换术(TMVR)
类似TAVR,经外周血管或者经心尖途径,将人工瓣膜锚定在二尖瓣的病变位置。
纵览全球二尖瓣修复/置换治疗领域,TEER是最早实现广泛商业化植入的技术。
经导管二尖瓣治疗技术汇总如下图所示:
市场规模
中国中度至重度二尖瓣反流患病数由2016年的980人增加至2020年的1080万人,2016年至2020年的复合年增长率为2.5%。该数字预计将于2025年达到1210万人 ,2020年至2025年的复合年增长率为2.3%。
3、三尖瓣疾病介绍、治疗方法及市场规模
三尖瓣反流(TR)
三尖瓣反流是指右心室收缩期间血液从右心室回流到右心房。复旦大学附属中山医院14万例超声数据研究显示,我国中度和重度的TR检出率分别为2.22%和1.39%;重度TR患者1年死亡率36%,5年死亡率约接近50%。
经导管三尖瓣置换/修复术(TTVR/r)
原理类似TMVR,经导管三尖瓣介入治疗主要分为置换和修复两大类。
三尖瓣介入修复与介入置换
市场规模
中国的三尖瓣反流患病数于2020年达到920万人,预计将在2025年达到90万人,2020年至2025年的复合年增长率为1.5%。
4、肺动脉瓣疾病介绍及治疗方法
肺动脉瓣狭窄
肺动脉瓣发育异常而引起的肺动脉瓣开放受限,可单独存在,常是复杂心血管畸形的组成部分。肺动脉狭窄开放受限后,从肺动脉瓣流向肺动脉的血流减少从而引起机体缺氧。过多的血流淤积于右室,造成右心前负荷增加,右房、右室增大从而引起右心功能不全。
介入治疗
1.经皮球囊肺动脉瓣成形术(把狭窄的瓣膜口用球囊扩开):单纯性肺动脉瓣中度至重度狭窄首选治疗方法。
2.经皮肺动脉瓣植入术(置入一个新的肺动脉瓣瓣膜):适用于法洛四联症术后肺动脉瓣反流需再次干预,进行性或严重右室扩大,中重度右心功能不全,三尖瓣重度反流。
关于高分子瓣膜
人工心脏瓣膜是一种用于治疗心脏瓣膜疾病或缺损心脏的植介入医疗器械,通过置换人体心脏内发生病变的瓣膜,可使患者重建血液循环动力功能,在心血管治疗领域具有重要作用。高分子瓣膜是一种由高分子材料制成、能够更好治疗心脏瓣膜病的创新器械。其中,高分子材料是一种由大量重复单元组成的大分子化合物,具有较高的强度和耐用性。
瓣膜发展趋势来看,从最早的机械瓣(A-C:包括双叶瓣、斜碟瓣 、球笼瓣),到生物瓣(D-F)再到最新的介入瓣(G、H),心脏瓣膜经历了三代技术革新。置入机械瓣后需终生进行抗凝治疗,且有血栓及出血风险;生物瓣膜其有较好的生物相容性,只需短期抗凝,血流动力学性能更为优良,但容易出现钙化、破损以及撕裂等问题。评价生物瓣膜最重要的两个指标:良好的耐久性和优异的血流动力学表现。
传统瓣膜对比
随着研究不断深入,高分子材料瓣膜出现在临床上。基于高分子材料的瓣膜集机械瓣和生物瓣二者的优势于一身,既具备优异的耐疲劳特性,又有极好的血液相容性。与传统机械瓣和生物瓣相比,高分子心脏瓣膜的使用寿命长,可以达到25年左右,而且与生物心包瓣膜一样,高分子瓣膜无需终生抗凝,也不会产生机械瓣膜的噪音,具有零钙化、低凝血、高生物相容性的优点。
高分子瓣膜脉动流影像
伴随材料科学在该应用领域的突破,高分子(Polymer)瓣膜材料的自动化生产不仅弥补了动物心包瓣膜能效的不足,并能走出手工缝合时代,极大降低材料及制造成本,提到产品质量的一致性。同时在体外模拟实验中,结果显示高分子(Polymer)瓣膜使用寿命比传统牛心包瓣膜更长久(达20~25年)。认为未来三到五年,具备高分子瓣膜制备能力的TAVR公司会成为行业翘楚。
近十年来开发的用于外科开胸手术的聚合瓣膜(SVR)和用于经导管瓣膜置换术的聚合瓣膜(TVR)
高分子多聚合物瓣膜的研发难度很高。经过全球科学家、临床医生和材料学家数十年探究和反复验证,直到近几年才取得突破并制作出达到临床要求的高分子多聚合物瓣膜。目前全球范围内来说,仅有少数企业掌握高分子瓣膜技术,并且暂无上市的产品。据不完全统计,国内正在进行高分子瓣膜研发的企业有:以心医疗、心通医疗、先健科技、启明医疗、心锐医疗、沛嘉医疗、心岭迈德等。
二、医疗器械产品解析
1 、LifePolymer
Foldax公司
Tria采用Foldax开发的革命性的聚合物材料----LifePolymer制成,是目前高分子心脏瓣膜进展最快的高分子瓣膜产品。Tria由聚合物瓣叶、聚醚醚酮(PEEK)支架和聚四氟乙烯(PTFE)缝合环构成,是一个真正意义上100%由合成聚合物制作而成的人工心脏瓣膜。离体测试结果显示,Tria外科瓣可使用约35年,优于如今生物瓣的平均使用寿命。
该瓣膜有一个带瓣膜的自扩张镍钛合金框架和一个10毫米的密封套。尺寸为27毫米的经导管Tria瓣膜已通过台架测试,并在加速疲劳测试中显示出1亿次循环。平均梯度为3.6 mmHg,EOA为2.9 cm2。
Tria产品图
Tria TVR瓣膜也已经在体内进行了研究。该装置通过 CPB 植入主动脉位置。通过升主动脉输送瓣膜,并对其进行定位以评估瓣膜在体内的有效性。结果显示了可输送性,良好的血液动力学,30天后没有表面纤维蛋白、血栓或纤维化,袖口愈合良好,90天后瓣叶干净。目前,Tria正在进行更大规模的临床研究。此外,Foldax公司的二尖瓣手术瓣膜和经导管主动脉瓣置换术(TAVR)也将陆续进入临床阶段。
将LifePolymer与专利设计相结合,开发出无需应用动物组织的长效心脏瓣膜;可用于经导管置换或外科手术替代病变的心脏瓣膜;旨在减少或消除终身抗凝药物的需求并优化血流动力学和有效的开口面积。LifePolymer材料具有较强的耐久性,无动物组织潜在的疯牛病传染问题,部分性能优于生物瓣膜,如优异组织相容性、优异机械性能、长期使用寿命。
同时Tria将对瓣膜加工方式带来革命性改变,是第一个并且唯一一个机器人生产制造的心脏瓣膜。因此其聚合物瓣叶可以始终如一地以精确的厚度制造,并且旨在实现具有可预测性能的瓣膜,并与患者共度一生,其将为数以百万计的主动脉瓣、二尖瓣和三尖瓣疾病患者带来更为经济、安全、有效的治疗。
2 、Polymer Valve
Strait Access Technologies(SAT)公司
SAT研发了一款新型球扩式主动脉瓣聚合物瓣膜Polymer Valve——适用于风湿性和退行性疾病患者。它是由荷兰帝斯曼(DSM)研发的CarboSil热塑性有机硅-聚碳酸酯-聚氨酯(TSPCU)的聚合物材料制成。
SAT Polymer Valve中空球囊放置瓣膜假体,允许血液自由血流,无需快速起搏,可通过触觉反馈确认手术过程中定位是否理想,并且允许批量化、自动化生产。入路方式为经心尖和经股动脉;有三种尺寸类型。该产品已受到世界心脏联合会的支持,将在监管部门批准后启动临床试验。
安装在心脏支架和球囊扩张导管上的新型聚氨酯心脏瓣膜
3 、STEALTH聚合物经导管主动脉瓣、MASA瓣膜
PECA Labs公司
STEALTH聚合物经导管主动脉瓣
宾夕法尼亚州的 PECA Labs公司研发的STEALTH聚合物经导管主动脉瓣,超薄输送系统——全聚合物小叶使输送系统更纤薄,以减少血管损伤的机会;经过临床验证的聚合物材料,提供了卓越的性能和耐用性。
STEALTH聚合物经导管主动脉瓣
(a)在CAVD主动脉瓣模型中部署的测试瓣膜,侧面和顶部视图
(b)在复制器中安装在匹配CAVD主动脉上的部署瓣膜,使用x线血管造影可视化
MASA瓣膜
除STEALTH聚合物TAVR瓣膜外,PECA Labs公司还设计并完成制造了一款聚合物肺动脉瓣——MASA瓣膜。MASA专为儿科设计,是一种用于肺动脉瓣重建的聚合物瓣膜导管,该瓣膜具有专利双叶片结构,旨在随着患者身体的发育同步扩展,从而避免重复手术。
MASA 瓣膜是用于肺动脉瓣重建的双叶聚合物脉瓣导管。该瓣膜有一个 ePTFE(聚四氟乙烯)导管和用聚丙烯缝合线固定在导管上的 ePTFE 瓣膜叶片。这一装置的外导管表面采用弹性印刷设计,可指示瓣膜位置和血液流动方向。MASA利用ePTFE 的材料特性和 RVOT专用阀门设计来缓解当前肺动脉瓣问题。
MASA独特的ePTFE 材料制备有助于避免人体免疫反应和瓣膜钙化,这是生物瓣膜最为常见问题,也是瓣膜失效的主要原因。MASA采用PECA Labs专有导管和瓣膜小叶制成,可生产多种尺寸,以确保与每位患者独特的解剖结构相匹配。
MASA瓣膜被设计用于重建右心室流出道(RVOT)并提供功能性肺动脉瓣。植入后,MASA 瓣膜为血液从右心室(RV)到肺动脉(PA)提供了一条通道,而集成瓣膜有助于防止回流到右心室。这款瓣膜肺动脉瓣导管适用于22岁以下患有下列先天性心脏畸形的患者,可用于右心室流出道的矫正或重建:
肺动脉狭窄;
法洛四联症;
动脉干幼稚症;
大血管转位;
肺动脉闭锁。
目前,MASA聚合物肺动脉瓣已完成首例人体植入,患者为21个月大的婴儿。
4 、FibraValve
哈佛大学
哈佛大学的研究人员通过创新的3D打印技术开发出一种名为FibraValve的儿童心脏瓣膜,以解决儿童风湿热所导致的心脏瓣膜损伤问题。这项突破性研究能够在短短10分钟内通过聚己内酯(PCL)和聚乳酸(PLA)等材料的组合,利用聚焦旋转喷射纺丝(FRJS)的新方法进行3D打印,让瓣膜与患儿一起生长,从而消除了额外的手术需求,最大限度地减少了手术并发症和痛苦。
FibraValve是由长纤维聚合物纤维组成的,它复制了人类心脏瓣膜的物理特性,并且具有足够的多孔性,允许细胞渗透并用活组织代替支架
资料来源:哈佛大学威斯研究所
FibraValves是一款由可吸收材料---PLCL制造的可吸收可再生的高分子瓣膜。PLCL聚合物材料不仅可以改善FibraValve植入体内后活细胞的渗透性,而且还能进行生物降解。相比之前的其他组织工程瓣膜,FibraValve更具弹性,并且能够使细胞在整个支架上更均匀地分布。团队还对瓣膜内部“瓣叶”的形状进行了优化,以减少血液通过瓣膜返流的量。通过所有这些改进,FibraValve能够实现自我重塑,对于仍处于生长阶段的儿童心脏瓣膜疾病患者非常有用。
FibraValve采用了创新的瓣膜框架设计,通过FRJS技术结合空气喷射流的引入,可以充满液体聚合物,从而轻松调整最终形状,并提高纤维在心轴上的沉积速率。最终得到的合成3D打印结构具有网状纳米纤维网络,可以促进细胞的渗透和生长。FRJS制备技术有点类似全自动棉花糖售卖机,通过空气射流将PLCL丝引导到心脏瓣膜上支架上,形成一个具有网状纳米纤维网络的可吸收人工瓣膜。FRJS制备的FibraValve复制了人类瓣膜的物理特性,并且具有足够的多孔性,可以让细胞渗透并用活组织替换支架。FibraValve最终生物可吸收PLCL材料将逐渐被细胞取代,最终形成再生的心脏瓣膜。
聚合物和聚焦的气流被强制通过纺丝装置,聚合物的纤维聚集在阀形芯棒上形成纤维阀
资料来源:哈佛大学威斯研究所
根据哈佛大学研究团队介绍FRJS制备一个人工瓣膜只需要几分钟,效率非常。如此高效的技术一旦临床证实安全有效,将有望使瓣膜价格大幅下降,将真正帮助那些需要瓣膜置换的患者,并为日后开发更多定制化的植入式医疗设备提供了新思路。该研究结果为再生医学领域的进一步发展铺平了道路。
5、Triflo valve
Novostia公司
创新公司Novostia推出一款无需终身抗凝的机械瓣---Triflo valve。Triflo valve是一款突破性的机械瓣,由高性能生物相容材料制成,具有出色的耐磨性和抗疲劳性,能够承受高心动周期。解决机械瓣最大问题血栓,同时延续机械瓣最大优点终身有效的使用寿命。Triflo valve特别适合用于儿童和年轻患者,改善他们的生活质量,为他们提供一种独特、耐用、无抗凝、无噪音的心脏瓣膜。
Triflo valve由法国心血管外科医生Didier Lapeyre和达索航空公司阵风飞机的联合设计师Philippe Perrier共同设计开发,是拥有航空发动机基因的人工瓣膜。
Triflo valve具备以下优势:
低血栓形成
由于其采用独特的仿生理结构设计,Triflo valve能够防止传统机械阀上观察到的导致血栓栓塞的血液流动诱导机制。已经在几十头动物实验中被证实,植入1.5年动物们都无需服用抗凝剂,没有发生阻塞性血栓形成。这归功于Triflo valve的优异生物相容性材料和类似于天然的人类心脏瓣膜结构设计。类人体瓣膜设计,使Triflo valve不会产生高速回流射流,不会引发止血反应。
经久耐用
Triflo valve由高性能生物相容性材料制成,具有出色的耐磨性和抗疲劳性,能够承受高心脏周期。与耐用性有限的生物瓣不同,尤其是对于年轻患者而言,瓣膜的结构设计可让任何年龄的患者终生使用,从而避免二次手术的风险。
安静
由于特殊的设计,Triflo valve的功能类似于人体自身瓣膜,能够平稳而安静地关闭,消除了一些使用传统前机械阀门的患者感知到的“咔哒”声。Triflo valve采用由一种新的高性能聚合物制成,可替代传统的金属、陶瓷等材料并减少声学传播的声波。
出色的血流动力学
Triflo valve凭借其三叶设计,展示了卓越的血流动力学性能,包括小尺寸。
其独特的设计允许无阻碍的小叶开放和最佳的血液流动,具有低剪切应力和通过枢轴区域的湍流
适用于任何年龄的主动脉瓣和二尖瓣患者
Triflo valve拥有多种尺寸:
主动脉瓣:从15毫米到27毫米
二尖瓣:从25毫米到33毫米
6、SIKELIA® Polymer TAVR
以心医疗
SIKELIA® Polymer TAVR是上海以心医疗自主研发的全球首款高分子材料瓣叶的经导管主动脉瓣置换产品,是由自膨胀镍钛合金支架和由以心医疗自主研发的BioDura®高分子复合材料瓣叶组成的一体式结构。
(A至D)产品形态及与周围组织的关系
Polymer TAVR具有一系列显著特点,主要涵盖了以下八个方面:
1. 零钙化:零钙化是一种重要的技术创新,目的是解决传统TAVR产品在使用过程中可能出现的瓣膜钙化问题。传统TAVR产品主要采用动物心包或瓣膜组织制作瓣叶材料,然而这类组织瓣膜在长时间使用后容易出现人工瓣膜退行性变,导致钙化和瓣膜功能衰败。这种状况不仅影响患者的生活质量,还可能增加手术风险和治疗成本。早期的聚合物瓣膜工程虽然试图解决这一问题,但由于材料本身容易钙化,进展相对缓慢。随着材料科学的发展,以心医疗公司推出了一种采用改进后的聚合物复合材料制成的Polymer TAVR系统,从而有效避免了瓣膜钙化的问题。
2. 低凝血:Polymer TAVR系统采用了一种具有创新性的表面涂层技术,该技术涉及在瓣叶材料表面涂覆一种特殊材料。这种材料具有降低凝血和抗血栓形成的特性。研究表明,表面修饰已经显示出增强材料表面对内皮细胞的亲和性,从而保护人工瓣膜免受免疫系统的异物反应。
3. 高生物相容性:Polymer TAVR(经导管主动脉瓣置换)系统的瓣叶材料在人体内能够较好地适应和融合,不易产生排斥或不良反应。这种特性对于人工瓣膜的长期稳定性和成功率至关重要。Polymer TAVR系统的瓣叶材料采用高分子聚合物,这些聚合物及其表面被特别设计和优化以提高生物相容性。当Polymer TAVR人工瓣膜植入患者体内,能够更好地与周围组织融合,减少刺激和排斥反应。优异的生物相容性使得人工瓣膜在患者体内更加稳定,有助于延长瓣膜寿命并降低并发症风险,增加人工瓣膜的耐久性。
4. 大网格设计:Polymer TAVR系统的支架设计采用大网格设计,可以增加瓣膜支架的柔韧性和适应性,大网孔设计使支架能更有效地适应不同解剖结构和病变严重程度的主动脉瓣,确保安全贴合并降低瓣周漏等并发症的风险,可提高手术成功率。大网孔的设计还可以降低冠状动脉阻塞的风险,并有助于再次PCI时的冠脉通路。瓣膜支架设计中的较大网孔还有助于促进人工瓣膜的最佳血流,降低支架血栓形成的风险并提高整体瓣膜性能。较大的网孔设计可能使介入医生在术中更易于回收和如有必要时重定位人工瓣膜(如有必要)。
5. 记忆合金丝铆接结构:Polymer TAVR系统的支架采用具有形状记忆和超弹性特性的记忆合金丝铆接结构,可以适应不同的主动脉瓣解剖形态,并保持铆接连接的完整性及其功能,提高手术成功率。
6. 连合对齐:Polymer TAVR系统的独特设计使其易于与原生瓣叶连合对齐(commissural alignment),将原生主动脉瓣瓣叶连合(即交界)与Polymer TAVR人工瓣膜交界进行对齐,并远离冠状动脉开口,有助于TAVR后PCI的冠脉通路等。
7. 预装、完全可回收:Polymer TAVR系统的人工瓣膜具有预装载、完全可回收的特性,可以大大减少手术时间和手术风险。
8. 良好耐久性:Polymer TAVR系统的瓣膜使用寿命可达20-25年,是传统TAVR产品使用寿命的两倍以上,耐久性良好。
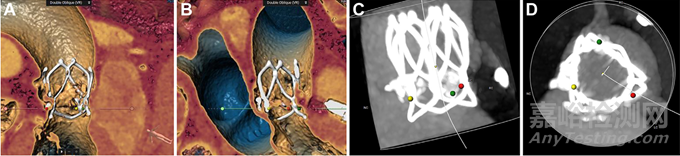
(A)活体透视显示主动脉根部。(B)钙化主动脉瓣处球囊膨胀。(C)传递系统。(D)将参考点与正位环空对齐后,逐渐展开瓣膜。(E)确认瓣膜位置和冠状动脉血流量。(F)完成阀门部署。(G)即刻血管造影显示中度瓣膜周围渗漏。(H) 15分钟后瓣周渗漏减少至轻度。
SIKELIA® Polymer TAVR产品植入后理论寿命能达到20-25年,因此适合更年轻的病人,大大扩展了同类产品的适用人群范围。同时从生产工艺上,可实现全自动化工业生产,显著降低了原材料和制造成本,提高了产品质量的一致性。随着Polymer TAVR系统在临床应用的不断推广,有望改善更多患者的生活质量,为全球瓣膜领域开创新篇章。
7、TaurusApex
沛嘉医疗
TaurusApex是沛嘉医疗独立研发的第四代介入瓣膜产品,使用自研的高分子纤维编织物作为瓣叶材料。通过模仿自体瓣叶结构(5层疏水结构)设计了多层复合材料,采用超细高强高分子纤维编织纤维层,兼具优异的机械性能和类似天然瓣叶的各向异性。与传统的牛心包材料相比,TaurusApex的厚度可减少80%,耐久性显著提升,在2亿次疲劳测试后各血液动力学参数基本保持不变,瓣叶并无明显使用痕迹。
根据沛嘉在研发公开日介绍, TaurusApex主要致力于解决生物瓣的不足(例如寿命短):
整个工艺过程解决了动物源材料人工筛选的不确定性,减少了缝制过程的手工操作。TaurusApex的生产工艺特点,使建立批量化生产能力、降低生产成本成为可能,与动物源材料相比具有性能上的高度一致性,并在关键性能上实现按需调整,将带领介入瓣膜产品走出“手工缝瓣”的历史阶段。TaurusApex瓣叶厚度比传统牛心包瓣叶的厚度大幅降低,更符合经血管人工瓣膜产品的要求,有望获得更为优异的临床结果和术者使用体验。
TaurusApex仿生复合编织结构
人体自体主动脉瓣叶由5层疏水组织构成(包括表层、纤维层、海绵层、心室层、表层 ),而生物瓣采用动物心包,由纤维层和外膜层构成。TaurusApex设计模仿人体自体瓣叶结构设计,采用多层复合材料。这与国外标杆企业Foldax产品TRIA的瓣叶不同,TRIA的瓣叶只有单层聚氨酯材料,通过反复浸涂成型。
TaurusApex采用多层仿生复合编织结构,更接近人体自体瓣叶性能,在耐久性能和抗撕裂,抗磨损等方面表现更优。为此沛嘉开发了一系列的技术和评价方法以达成这些设计目标。
纤维各层间结合强度评价
根据TaurusApex实验数据表明,与传统牛心包材料相比,高分子瓣叶材料断裂力提高至少2-5倍,可以大大提高耐久性能;缝合断裂力提高约70%,可提高耐久性能。除了革命性的高分子瓣的研发外,在生物材料上,公司还有非醛交联技术加持,聚焦耐久性的提升。
8、PoliaValve
心岭迈德
心岭迈德的高分子主动脉外科瓣膜(PoliaValve)目前已在国内率先完成首例国产高分子外科瓣膜的正式动物实验,占据了领先优势。实验结果显示:PoliaValve植入后,瓣膜有效开口面积(EOA)、跨瓣压差等指标均不逊色于传统生物瓣膜。
经过多轮设计迭代和充分设计验证,心岭迈德的高分子外科瓣膜具有不亚于生物瓣膜的流体力学性能、耐疲劳性能,以及远远领先于生物瓣膜的抗钙化性能。例如,在90天小鼠皮下钙化实验中,其高分子主动脉外科瓣膜钙化结晶数量是常见生物瓣膜的1/3。
心岭迈德还是国内首家采用机器人自动化生产高分子瓣膜的企业。其中,瓣膜材料浸沾成型、烘干和测厚均由机器人完成。相比于人工操作,机器人可实现智能化、高精度、高质量、大规模应用,降低成本,消除手工生产的不可控性。
在结构性心脏病领域,目前国内生物瓣组织抗钙化技术仍需追赶海外领先技术,心岭迈德应用自主研发的创新型高分子材料带来的技术突破,有望实现我国在该领域的跨越式极速发展。心岭迈德的高分子外科瓣膜是材料合成和加工技术的验证平台。充分验证后,高分子主动脉介入瓣膜也会进入开发设计阶段。
9、PoliaValve
心锐医疗
苏州心锐医疗科技有限公司是国内从事高分子瓣膜研发的企业,坚持从源头创新,聚合物瓣膜从材料合成到构型设计均为自主研发,该公司自主研发的聚合物瓣膜在血流动力学(如EOA、渗漏性能等)、耐疲劳特性等方面均优于传统主流瓣膜产品。
心锐医疗的聚合物瓣膜的材料经第三方检测,关键性能与全球领先的高分子瓣膜企业Foldax公司基本一致,完全能够满足心脏瓣膜的使用需求。同时,心锐医疗在瓣叶结构上创新,使其在瓣膜有效开口面积、渗漏性能等血流动力学方面优于传统主流瓣膜产品。
从高分子瓣膜的核心要素看,心锐医疗在高分子材料、瓣叶结构设计等方面均处于全球领先水平。基于心锐医疗的软硬件优势,已布局的高分子外科主动脉瓣、二尖瓣以及介入主动脉瓣。预计今年年底或明年年初将进入临床。
参考资料: 医林研究院、《高分子瓣膜研究报告》、医心、MEDTF、以心医疗、智慧医械、我爱瓣膜、动脉网、美国心脏病学会杂志、医械知识产权等。