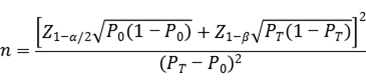刚刚,器审中心发布《个体化用药基因检测试剂临床评价指导原则(征求意见稿)》,内容如下:
个体化用药基因检测试剂临床评价指导原则(征求意见稿)
本指导原则旨在指导注册申请人对个体化用药基因检测试剂临床评价资料的准备及撰写,同时也为技术审评部门提供参考。
本指导原则是对个体化用药基因检测试剂临床评价的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
本指导原则是供注册申请人和技术审查人员的指导性文件,但不包括审评审批所涉及的行政事项,亦不作为法规强制执行,应在遵循相关法规的前提下使用本指导原则。如果有能够满足相关法规要求的其他方法,也可以采用,但需要提供详细的研究资料和验证资料。
本指导原则是在现行法规和标准体系以及当前认知水平下制定的,随着法规和标准的不断完善,以及科学技术的不断发展,相关内容也将适时进行调整。
一、 适用范围
近年来,药物基因组学得到了迅猛发展,越来越多的药物基因组生物标记物相继涌现,比较典型的标志物如:药物代谢酶、和药物作用靶点的基因变异。
药物代谢酶和药物作用靶点的基因变异可通过影响药物的体内浓度和靶组织对药物的敏感性,导致药物反应(如药物疗效和药品不良反应)的个体差异。药物基因组生物标志物的检测,即个体化用药基因检测,是临床实施个体化药物治疗的前提。
个体化用药基因检测目的主要有以下两方面:
1. 根据个体遗传信息预测药物疗效,从而调整用药剂量或更换用药种类,以改善药物疗效。
2. 根据个体遗传信息预测药物不良反应,从而调整用药剂量或更换用药种类,以避免或减少药品不良反应。
本指导原则所述个体化用药基因检测试剂即指药物代谢酶和药物作用靶点基因变异检测试剂,适用于采用基因检测方法检测人体样本中基因组特定变异,从而指导特定药物使用的检测试剂。
本指导原则不适用于伴随诊断试剂。
本指导原则适用于进行体外诊断试剂产品注册申请和变更注册申请的产品,重点针对个体化用药基因检测试剂临床评价资料的准备及撰写明确要求。
二、注册审查要点
(一) 个体化用药基因检测试剂基因变异及配对药物的选择
个体化用药基因检测试剂在产品设计中最关键的问题在于特定基因变异及其指导的特定药物的选择。
在该类试剂的设计开发过程中,申请人应充分考虑备选基因变异和药物的临床需求和临床认可度、以及备选基因变异各基因型在中国人群的发生频率等,充分调研国内外药品说明书、权威数据库(如:PharmGKB数据库、CPIC数据库和DPWG数据库)和相关指南,选择适当的基因变异和药物组合。
应特别提醒的是:
1. 申请人应特别关注针对中国人群的研究数据,基因变异和药物组合应适合中国人群的特点,满足中国人群的临床使用需要。
2. 针对与药品不良反应相关的个体化基因检测试剂,其临床意义的确认,主要依赖诊疗指南、权威数据库、药品说明书或临床研究证据等。在开发该类试剂时,建议申请人进行充分调研后,选择基因变异与药品不良反应关系明确的基因和药物组合进行产品研发。
3. 针对个体化多基因联合检测试剂,在产品设计开发时,应充分考虑多基因联检时,所指导的单个或多重用药仅在具有适用人群时,方可考虑联检组合。
(二)个体化用药基因检测试剂临床评价要求
1. 临床评价内容
该类试剂的临床评价包括如下两大部分内容:
1.1产品临床意义的确认,即基因变异与药物反应的确认,可通过诊疗指南、权威数据库、药品说明书或高水平临床研究证据等提供临床证据。产品临床意义确认的证据,可为多种证据类型的组合。
1.2产品临床检测性能的确认,应通过临床试验提供临床证据。
1.3 如通过临床试验提供临床证据,应注意:
1.3.1境内临床试验应符合《体外诊断试剂注册与备案管理办法》、《医疗器械临床试验质量管理规范》及《体外诊断试剂临床试验技术指导原则》等现行法规的要求。
1.3.2如为境外临床试验数据,还应评估境内外人种差异对临床试验结果的影响,如有必要,应根据《使用体外诊断试剂境外临床试验数据的注册审查指导原则》补充相关临床证据。
2. 针对产品临床检测性能进行的临床试验
下面仅说明该类试剂临床试验中应关注的重点问题。
2.1 临床试验机构
临床试验应在不少于3家(含3家)、具备相应条件且按规定备案的医疗器械临床试验机构开展。
2.2 对比方法
对于中国境内已有同类产品上市的试剂,可选择中国境内已上市的、具有可比性的同类产品作为对方法,或采用具有可比性的临床参考方法(如:一代测序等)作为对比方法进行比对研究对于已在中国有同类产品上市的试剂,建议优选选择同类产品作为对比方法。
对于中国境内尚无同类产品上市的试剂,采用申报产品与具有可比性的临床参考方法(如:一代测序等)作为对比方法。
对比方法的可比性应关注:适用样本类型的可行性、预期用途(适用人群、所检基因变异及指导药物)的可比性以及产品性能指标的可比性等。
2.3 受试者选择
临床试验的入组人群应来自申报产品的预期适用人群,应为所指导药物的预期使用人群,并根据申报产品的预期用途,纳入相关人群进行临床试验。临床试验方案应明确受试者入排标准,并说明依据。入组受试者应能够代表产品适用人群的各种情形,例如:应包括不同年龄、性别受试者;如涉及多个适应证,每种适应证患者均应纳入一定数量。
2.4样本量
临床试验样本量应采用适当的统计学方法进行估算,并详细描述所使用统计方法及各参数的确定依据。此部分临床试验目的为评估两种检测方法之间的一致性,建议采用单组目标值法进行最低样本量的估算。通过阳性符合率和阴性符合率来分别计算所需阳性样本和阴性样本的例数,应针对各基因每个变异位点分别进行样本量的估算。
针对每个变异位点,阴、阳性符合率的临床可接受标准(P0)一般不低于95%。当评价指标PT接近100%时,该样本量估算方法可能不适用,应考虑选择更加适宜的方法进行样本量估算和统计学分析,如精确概率法等。
公式中,n为样本量;Z1-α/2、Z1-β为显著性水平和把握度的标准正态分布的分数位,P0为评价指标的临床可接受标准,PT为申报产品评价指标预期值。
针对每个变异位点,所估算的阳性样本量应为纯合突变型和杂合型的总和,要求纯合突变型和杂合型均应具有一定的例数。如纯合突变型或杂合型样本由于临床发生频率低较难获得,可回顾性临床原始样本进行富集。对于具有明确临床意义的变异位点,如确属罕见突变型(应提供证据),在该变异位点总体阳性样本量满足要求的前提下,可酌情减少纯合突变型或杂合型的例数。对于临床意义尚未明确的新的变异位点,可采用回顾性临床原始样本进行临床研究,保证纯合突变型或杂合突变型评价的充分性。
临床试验总样本量确定时应在上述阴、阳性样本最低样本量估算的基础上,同时考虑其他可能造成受试者脱落的情况,根据实际情况适当增加入组样本量。
2.5 统计分析
应对所入组人群进行人口学分析,包括性别、年龄、疾病类型和基因型例数总结等。
针对每个变异位点,一般以3x3格表分别总结申报产品与对比方法的定性检测结果,计算两种方法的阳性符合率(包括纯合突变型和杂合型总体)、阴性符合率(野生型)、纯合突变型的符合率、杂合型符合率、野生型符合率、总和符合率及相应的95%置信区间。
针对不一致样本,应采用合理的方法进行确认,对不一致的原因综合进行分析。
3. 针对产品临床意义(临床有效性)确认的临床证据
3.1 已有同类产品上市的申报产品
对于在中国已有同类产品上市的申报产品,可认为其临床意义已得到认可,无需再进行临床有效性的确认。
3.2无同类产品上市的申报产品
3.2.1 如新变异位点与药物反应的关系已在国内相关诊疗指南、或国内药品说明书中被明确说明,并且具有较高的证据级别(如涉及证据级别),可认为其临床意义已得到认可,无需再进行临床有效性的确认。
3.2.2 如新变异位点与药物反应的关系已在国外相关指南、权威数据库或国外药物说明书中被明确说明,具有较高的证据级别(如涉及证据级别),且包含充分的中国人群的临床数据,可认为其临床意义已得到认可,无需再进行临床有效性的确认。
3.2.3 如新变异位点与药物反应的关系已在国外相关指南、权威数据库或国外药物说明书被明确,并且具有较高的证据级别(如涉及证据级别),但上述认可并未包含中国人群的临床数据,申请人应充分评价国内外人种的差异对变异位点与药物反应关系的影响,如有必要,应提交基于中国人群的临床证据。
3.2.4如新变异位点与药物反应的关系尚未在境内外诊疗指南、药品说明书和权威数据库等方面获得认可,申请人可通过以下方式证明变异位点与药物的关系。
3.2.4.1 通过国内循证医学证据。申请人应采用系统评价的方法,确定合理的临床问题,并制定科学的检索路径和关键词、进行有效的文献筛选和数据处理等,对高水平临床研究数据进行完整的系统评价,并提供系统评价报告。应提醒注意的是,该部分结论的获得应是基于高水平研究数据获得得。
3.2.4.2 通过国内临床试验
3.2.4.2.1 临床试验机构
临床试验应在不少于2家、具备相应条件且按照规定备案的医疗器械临床试验机构开展
3.2.4.2.2 临床试验设计
应采用临床原始样本进行申报产品的检测,并前瞻性或回顾性收集临床病例使用配对药物的临床结局(如:疗效或不良反应等),分析特定变异位点不同基因型与临床结局的关系,最终给出特定变异位点不同基因型可指导药物使用的结论。如采用回顾性方式,应连续纳入一段时间内的相关患者,不得进行病例挑选。
临床结局表征指标的设定应有充分的依据,应在临床试验资料中明确设定的依据,并提供充分的支持资料。与药品不良反应相关的产品,临床结局表征指标可以为是否发生某种不良反应,或能够代表病例是否发生不良反应的检测指标。与药物疗效相关的产品,临床结局表征指标可以为是否有效,或能够代表病例是否有效的检测指标。
该部分临床试验申报产品的检测结果,可采用申报产品临床检测性能确认时的检测结果。
3.2.4.2.3 受试者选择
临床试验的入组人群应来自申报产品的预期适用人群,应为所指导药物的预期使用人群,应为药物说明书“适应证”部分描述患者。临床试验方案应明确受试者入组标准,并说明依据。入组受试者应能够代表产品适用人群的各种情形,例如:应包括不同年龄、性别受试者;如涉及多个适应证,每种适应证的患者均应纳入一定数量。
3.2.4.2.4样本量
临床试验样本量应采用适当的统计学方法进行估算,并详细描述所使用统计方法及各参数的确定依据。此部分临床试验目的为评估变异位点与配对药物的相关性,因此,针对每一变异位点,不同基因型的病例(纯合突变型、杂合型和野生型)应均有一定的数量,以便进行有效的统计学分析。
3.2.4.2.5 统计分析
应对所入组人群进行人口学分析,包括性别、年龄、疾病类型和基因型例数总结等,同一变异位点不同基因型的人群应具有相同的人口基线。
针对每个变异位点,应分别分析不同基因型(纯合突变型、杂合型和野生型)与配对药物的相关性,并进行统计学分析,最终结论应能支持变异位点可有效指导特定药物的使用。
3.2.5 对于新变异位点临床意义的确认,可为上述多种证据的组合。
4. 涉及临床试验时的临床试验方案、小结和报告
各临床试验机构应采用同一临床试验方案,并在整个临床试验过程中严格执行,不可随意改动。方案应对试验设计类型、对比方法选择、受试者选择、评价指标、统计分析方法、样本量估算和质量控制要求等做出明确的规定,并根据各临床试验机构情况合理确定样本量分配计划。
各临床试验机构应对临床试验数据和实施情况进行总结,出具临床试验小结。
临床试验报告应对整体临床试验实施过程、结果分析、试验结论等进行条理分明的描述,并应包括必要的数据和统计分析方法,最后得出临床试验结论。临床试验报告的撰写参考《体外诊断试剂临床试验技术指导原则》的相关要求。
数据汇总表中应提供唯一可溯源的受试者编号、样本编号、基本人口学信息(性别、年龄等)、临床诊断背景信息、疾病类型、申报产品及对比方法的检测结果等信息。
如涉及委托第三方机构进行参考方法检测的,应提供临床试验机构与第三方机构签订的委托协议。同时应提供参考方法的详细资料,如:方法原理、所需试剂及仪器、参考方法的性能验证、参考方法质控、典型的试验图谱及数据等。上述资料应由临床试验机构签章确认。