近年来中药创新利好政策不断颁布,药品监管部门坚持守正创新,不断完善中药注册批准法规制度体系,鼓励中药新药研发,中药新药研发和上市速度明显加快,中药传承创新发展驶入“快车道”。本文汇总了23年中药品种的申请和审批情况,并对申报数量大幅增加的经典名方做出简要分析,供大家参考。
23年批准上市中药新药7个,与22年批准上市数量相同。批准品种中1.1类创新药4个(含1个进口中药)、1.2类创新药1个、2.2类改良型新药1个、3.1类经典名方1个。
23年申请上市中药品种共计24个,其中1类新药7个、2类改良型新药3个、3.1类经典名方13个、4类同名同方药1个。申请量较22年12个有较大增幅,特别是申请上市的经典名方从2个增加到13个。
23年申请临床试验中药共计67个,其中1类创新药47个、2类改良型创新药20个,较22年(54个)有一定增加。
经审评,23年明确不批准上市(或撤回)品种5个,其中2个品种为22年受理品种,申请临床试验未许可的品种有11个。
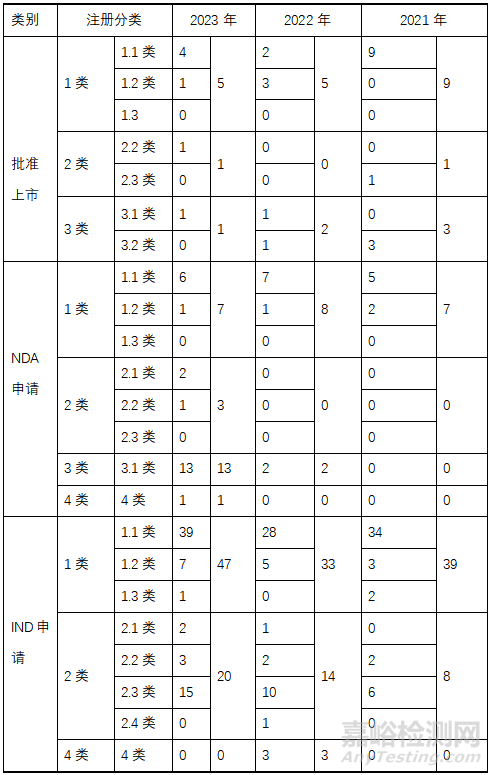
近3年注册申请和批注上市的中药品种,详见表1
▲表1-近3年注册申请和批准情况
注:1.2类新药,提取物和制剂按照1个品种统计。
一、 批准上市的中药
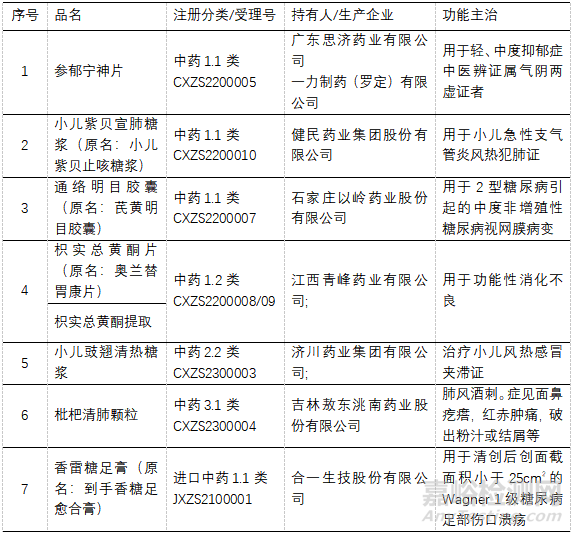
23年批准上市中药品种7个(批准文号8个),1.1类5个(含进口1.1类1款)、1.2类1个、2.2类(改变剂型)1个、3.1类(经典名方)1个,进口1.1类“香雷糖足膏”为附条件批准。见表2。
▲表2-2023年批准上市的中药
二、 申请上市的中药(NDA)
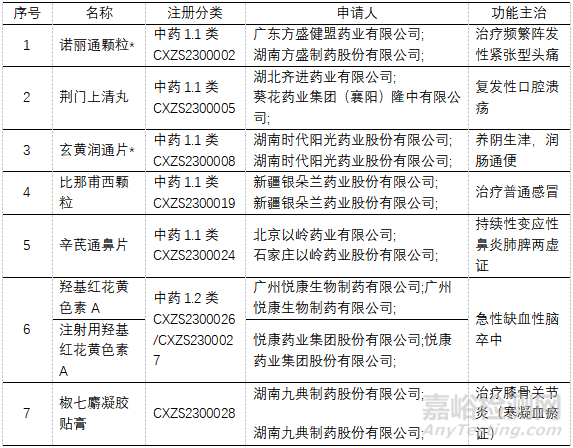
共受理申请上市的1类中药新药7个,其中1.1类6个、1.2类1个;改良型新药3个,其中2个改变给药途径的2.1类,1个改变剂型的2.2类品种;经典名方共计13个品种,同名同方药1个。详见表3~表6
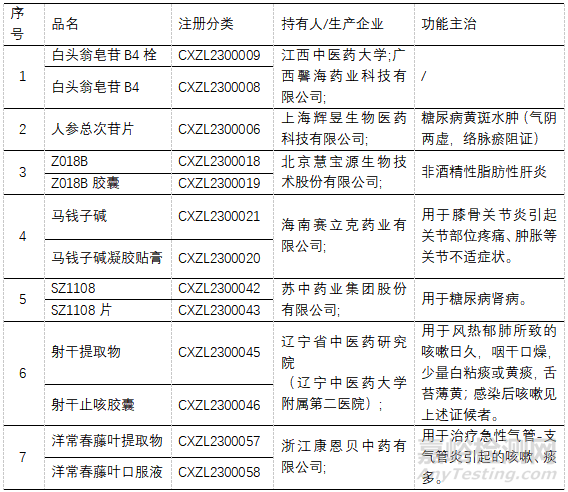
▲表3-NDA申请的1类中药新药 *未被批准
▲表4-NDA申请的改良型中药 *已批准上市
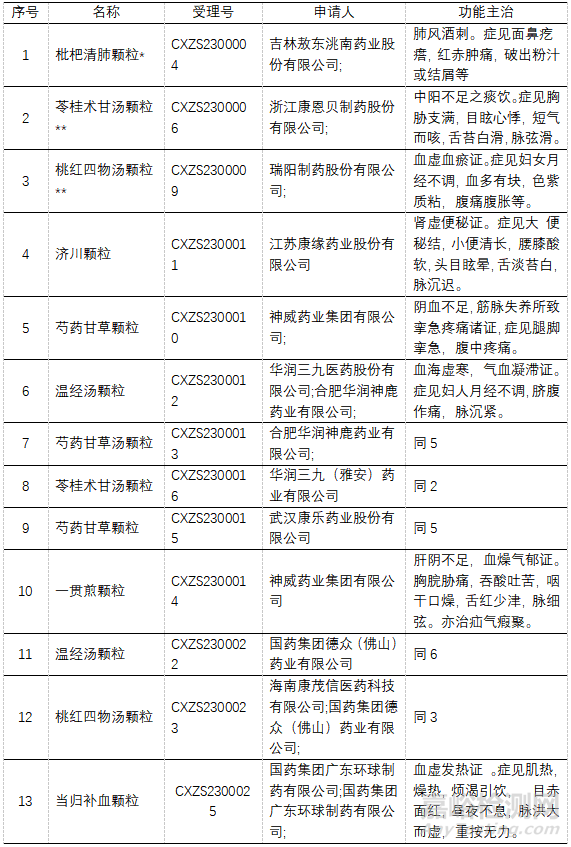
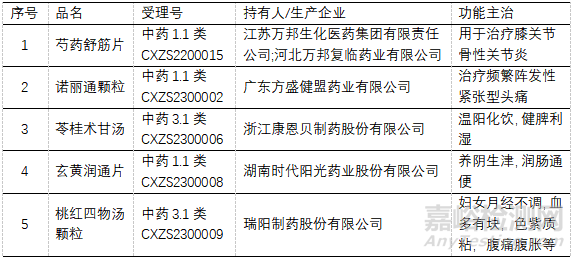
▲表5-经典名方(3.1类) *已批准上市 **未批准上市
▲表6-同名同方药
三、 未批准上市(含撤回)的中药
23年共计3个品种未批准,2个1.1类、2个3.1类;1个1.1类撤回。详见表7
▲表7-2023年未批准上市的中药
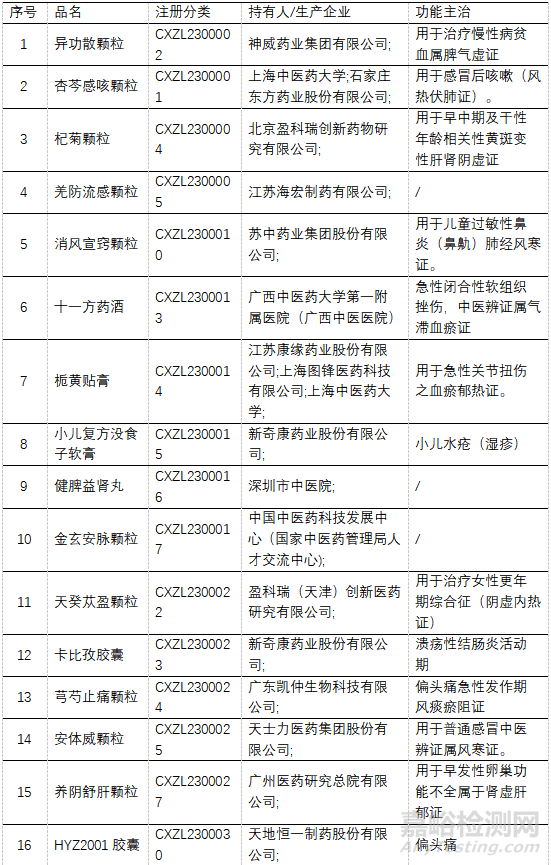
四、 申请临床研究的中药(IND)
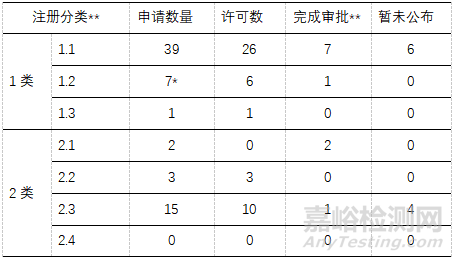
IND申请共计67个。其中1.1类39个品种,1.2类7个品种(提取物和制剂以1个品种计),1.3类1个;改良型新药共计20个,其中2.1类2个、2.2类2个、2.3类15个、2.2类/2.3类同报1个。见表8
▲表8-中药IND申请数量及许可结果
*提取物与制剂同时申请按照一个品种计算
**完成技术审评(临床试验可能未被许可)
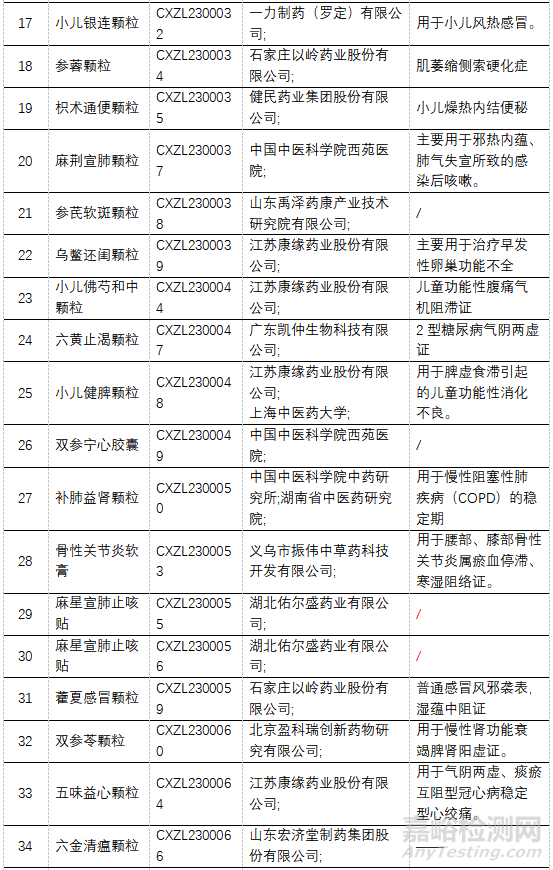
1.1类中药IND申请中,适应症最多的是呼吸系统感冒相关8个、消化系统 6个,儿科用药有 5个。药品名称及许可情况详见表9~表13。
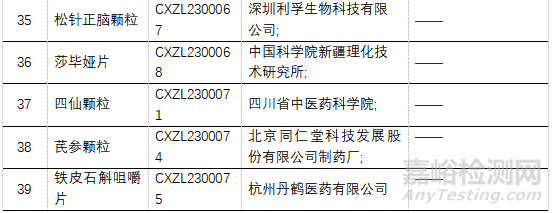
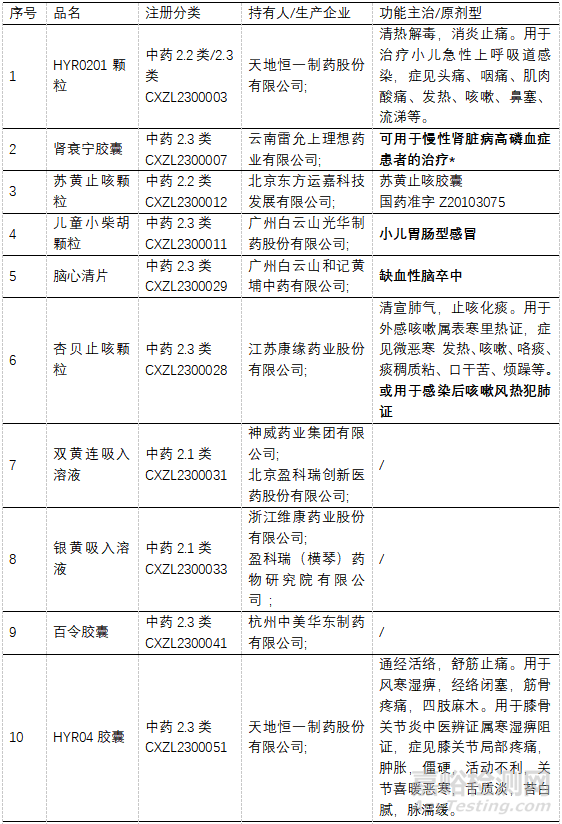
▲表9-申请IND的1.1类新药
注:“/”完成审批;“——”暂未公布。下同
▲表10-申请IND的1.2类新药
▲表11-申请IND的1.3类新药
▲表12-申请IND的改良型中药
* 加粗部分为增加的功能主治
五、 经典名方的申请和批准情况分析
到目前为止,NMPA共公布3批39首方关键信息。3.1类经典名方共受理14个,22年受理2个、23年受理13个,批准2个(1个23年)、未批准3个(2个23个)。申请涉及8个品种,10家申请人。合肥华润神鹿药业有限公司申请3个品种。
申请厂家最多的是:苓桂术甘汤,受理3家(批准1家、未批准1家、正在审评的1家);芍药甘草汤,受理3家,均为在审状态;桃红四物汤颗粒,受理3家,未批准2家、在审1家;温经汤颗粒受理2家,均为在审状态;温经汤颗粒,受理2家,均为在身状态;一贯煎颗粒、济川颗粒和当归补血颗粒均为1家受理,为在审状态。