您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-11-15 08:22
Humacyte公布一项关于可再生人工血管ATEV的临床研究(V007 3),研究显示出可再生人工血管ATEV更优的功能和通畅性,相比于自体瘘(AVF)。

V007 3是一项前瞻性、多中心、随机临床研究,在美国招募了242名血液透析患者。研究中的患者被随机分配接受ATEV或自体瘘进行血液透析,并随访长达24个月。
具体研究数据
术后6个月,试验组和对照组的功能通畅率分别为:81.3%和66.4%;
术后12个月,试验组和对照组的次级通畅率分别为:68.3%和62.2%。
两个治疗组的感染率都很低,试验组和对照组相关感染的患者比例为9.1%对9.9%(总事件数为12和14);
治疗中出现的不良事件发生率,试验组和对照组分别为98.3%对96.7%(总事件1211和828);
不良事件的最大差异在于血栓形成,试验组和对照组分别为52.1%和9.1%(126例和12例总事件;
大多数(94%)患有血栓形成的ATEV患者得到了成功治疗。
本项研究还进行三个亚组分析:
女性患者(n=70)
术后6个月和12个月,通畅率显著更高(P<.0001);
试验组前12个月的血液透析持续时间明显更长,(试验组8.3个月,对照组5个月;P=0.0011)。
肥胖患者(体重指数≥30;n=93)
术后6个月和12个月,通畅率显著更高(P=0.0001);
试验组前12个月的血液透析持续时间明显更长,(试验组7.7个月,对照组4.5个月;P=0.002)。
糖尿病患者(n=165)
术后6个月和12个月,通畅率显著更高(P=0.0024);
试验组前12个月的血液透析持续时间明显更长,(试验组7.4个月,对照组5.5个月;P=0.0155)。
PI评价
“这些结果表明,ATEV(一种生型人工血管)的可用性可能会改变许多血液透析患者的动静脉通路。我特别高兴地看到,在女性、肥胖和糖尿病患者中取得了积极的结果,这些患者通常在自体瘘管手术和历史上有限的血液透析治疗选择方面效果不佳。这些服务不足的患者在1年以上的持续时间明显更长,可以大大减少对动静脉通路导管的依赖。”
---Mohamad A.Hussain Brigham and Women’s Hospital
Humacyte公布优异临床数据(尤其是对比金标准AVF,显示出压倒性优势),让尿毒症患者看到新希望。在临床上,当尿毒症患者需要进行血透时,医生首选都是采用自体瘘,直到无法再从患者身上找到合适血管创建自体瘘时,才会考虑用人工血管。之所以医生这么选择,主要因为传统聚合物人工血管与自体血管差距太大。不仅AVG寿命低,而且容易发生感染,这导致AVG成为患者和医生最后无奈选择。
不过随着可再生生物学人工血管出血,有可能改变AVF和AVG选择。让AVG成为透析患者首选,这次V007 3临床研究给予患者和医生信息。不过目前研究只公布一年随访时间,需要更长期限随访数据来证实可再生血管的长期安全性和有效性。
当然除了需要Humacyte努力外,还需要国内再生血管参与一起努力。目前国内已经有两家生物可再生人工血管企业进入临床研究。期待他们临床研究数据能够取得ATEV一样临床效果,从而推进国内人工血管发展,造福国内患者。
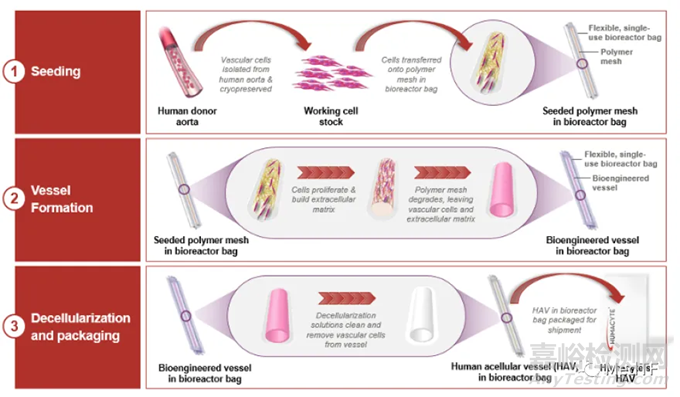
ATEV
ATEV是无细胞组织工程血管(acellular tissue engineered vessel)简称,其不仅保留血管生物力学特征,同时剔除可导致免疫排斥反应的成分。
ATEV的制造过程可分为:
先从人类供体获得血管细胞,然后对其进行组织培养,并且把细胞放在一个血管状的可降解支架上。细胞组织浸浴在营养液中生长,并不断延展从而获得真正的血管所具有的物理特性。
数周后,细胞生长并产生新组织,形成管状血管结构,而聚合物支架完全降解。
再将生物工程血管去细胞化以产生ATEV:一种细胞外基质,保留了血管的生物力学特征,但清除了可能诱导免疫反应的细胞成分。
Humacyte
Humacyte是由耶鲁大学Laura E. Niklason院士于2004年创立的创新医疗器械公司,其正在开发一个颠覆性的生物技术平台,以提供可普遍植入的生物工程人体组织和器官,旨在改善患者的生活并改变医学实践。
Humacyte开发和生产脱细胞组织,用于治疗各种疾病、损伤和慢性病。 Humacyte是人类无细胞血管(HAV)组合,目前正处于针对多种血管应用的后期临床试验,包括血管创伤修复、血液透析的动静脉通路和外周动脉疾病。冠状动脉旁路移植术、小儿心脏手术、1 型糖尿病治疗以及多种新型细胞和组织应用的临床前开发也在进行中。

来源:MedTF


