您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-03-03 10:27
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:14条资讯,阅读时长约:3分钟 」
恒瑞PD-1肝癌项目研究结果发表。近日由中国解放军东部战区总医院全军肿瘤中心秦叔逵教授和复旦大学附属中山医院任正刚教授共同牵头开展的恒瑞卡瑞利珠单抗在既往经过治疗的晚期肝细胞癌患者中的Ⅱ期临床结果于国际顶级期刊《柳叶刀·肿瘤学》正式发表。患者接受卡瑞利珠单抗 3 mg/kg q2w(n=109例)或 q3w(n=108例)的治疗,中位12.5个月随访时,在可评估患者中,客观缓解率为14.7%;2周用药一次的患者的客观缓解率为11.9%,三周一次的缓解率为17.6%;据BICR评估的所有患者疾病控制率为44.2%。
1.信立泰盐酸莫西沙星片获批上市。信立泰盐酸莫西沙星片(信达敏)获国家药监局核发的《药品注册批件》。盐酸莫西沙星为第四代新型喹诺酮类抗菌药,主要用于治疗成人(≥18 岁)敏感细菌所引起的感染,包括急性细菌性鼻窦炎、慢性支气管炎急性发作、社区获得性肺炎、复杂性皮肤和皮肤组织感染、复杂性腹腔内感染等,为《国家基本医疗保险、工伤保险和生育保险药品目录》医保乙类产品。
2.华世通降糖药阿格列汀即将获批。据NMPA官网信息,华世通生物4类仿制药苯甲酸阿格列汀片的批件已于2月21日核发。如若顺利获批,华世通生物将有望成为继亚宝药业之后,第二家拿下西格列汀仿制药的企业。阿格列汀(Alogliptin,尼欣那)是武田研发的一种二肽基肽酶4(DPP-4)抑制剂,于2010年在日本获批用于治疗2型糖尿病。该药2013年1月已获批进口中国,2017年全球销售额达537亿日元(约为5亿美元)。目前,国内共有5款原研DPP-4抑制剂获批,其中,沙格列汀、维格列汀和阿格列汀均有仿制药获批。
3.诺华曲美替尼+达拉非尼新适应症即将获批。诺华曲美替尼/达拉非尼组合疗法第2个适应症的上市申请已变更为"在审批",预计近期将获批上市。此次获批适应症预测是非小细胞肺癌,去年12月,该组合疗法已在国内获批黑色素瘤。截至目前,该组合疗法已获FDA批准的适应症包括:黑色素瘤、小细胞肺癌和甲状腺癌。据米内网数据,曲美替尼/达拉替尼联合疗法2019年的销售额达13.38亿美元,同比增长15.8%。
4.万隆制药盐酸非索非那定片一致性评价申请获受理。万隆制药盐酸非索非那定片一致性评价补充申请获CDE受理。盐酸非索非那定属于第二代H1受体拮抗剂,适用于季节性过敏性鼻炎、慢性特发性荨麻疹等病症的治疗。该药原研药(赛诺菲)的上市申请已于2019年5月获CDE受理。目前国内市场有6家国内企业、1家跨国企业拥有该产品生产批文。万隆制药为该产品首家申报一致性评价企业。
5.和铂医药抗CTLA-4抗体在美获批临床。和铂医药新一代抗CTLA-4抗体HBM4003获FDA批准新药临床试验许可。该试验将评估HBM4003作为单一药物在晚期实体瘤患者中的安全性、耐受性、药代动力学和抗肿瘤活性。HBM4003是一种全人源的抗CTLA-4重链抗体,产生自和铂医药特有的 Harbour Mice®平台。和铂医药已于2019年在澳大利亚开展HBM4003的Ⅰ期临床试验,目前正在顺利进行中。
1.FDA批准Daraprim首个仿制药。FDA批准首个Daraprim(达拉敏,乙胺嘧啶)片剂的仿制药,与用于治疗细菌感染的磺胺类药物共同使用,用于治疗弓形虫病。据了解,此次获批的Daraprim片剂仿制药来自美国Cerovene公司。Daraprim是美国药房零售价最贵的药物之一,每片750美元,每月(60片)的零售定价为45000美元。目前该药在其他国家已有仿制药获批上市,每片价格低至0.05美元—0.10美元。
2.武田抗体药物Entyvio SC获CHMP推荐批准。武田皮下注射(SC)剂型的肠道选择性抗体药物Entyvio(vedolizumab)获欧洲药管局人用医药产品委员会(CHMP)推荐批准,用于中重度溃疡性结肠炎(UC)或克罗恩病(CD)成人患者的维持治疗。该产品包括预充式注射器和预充式注射笔。如果获批,Entyvio将成为针对UC和CD治疗可同时提供SC和IV的唯一一种维持疗法。一项III期VISIBLE-1研究结果显示,与安慰剂组相比,Entyvio SC治疗组有统计学上显著更高比例的患者达到临床缓解(46.2%vs14.3%,p<0.001),而且Entyvio IV对照组观察到了相似的临床缓解率(42.6%)。
3.艾伯维Venclexta+阿糖胞苷一线治疗III期研究失败。艾伯维(AbbVie)公司公布靶向抗癌药Venclexta/Venclyxto(venetoclax)联合低剂量阿糖胞苷(LDAC)一线治疗急性髓性白血病(AML)III期VIALE-C(M16-043)研究的更新结果。结果显示,研究没有达到显著改善OS的主要终点:与安慰剂+LDAC治疗组相比,venetoclax+LDAC治疗组死亡风险降低25%(HR=0.75[95%CI:0.52-1.07],p=0.11)。在中位随访12个月时,venetoclax+LDAC治疗组中位OS为7.2个月,安慰剂+LDAC治疗组中位OS为4.1个月。额外随访6个月后的事后分析显示,venetoclax+LDAC治疗组中位OS为8.4个月,安慰剂+LDAC治疗组中位OS为4.1个月(HR=0.70[95%CI:0.50-0.99])。venetoclax是一种B细胞淋巴瘤因子-2(BCL-2)抑制剂。
4.Debiopharm创新疗法获FDA突破性疗法认定。Debiopharm公司“first-in-class”口服IAP拮抗剂获FDA授予突破性疗法认定,用于和标准治疗方案联用,一线治疗无法切除的局部晚期头颈部鳞状细胞癌。目前的标准治疗方法为基于顺铂的化疗与标准化学放射疗法(CRT)同时进行。在一项Ⅱ期临床试验中,与对照组相比,治疗组患者在接受CRT治疗18个月后局部控制率改善21%。在接受治疗2年后,患者的疾病进展和死亡风险下降63%(p=0.007)。
5.大麻素新型抗癫痫药Epidiolex在美申请新适应症。大麻素处方药制药公司GW Pharma及其子公司Greenwich Biosciences宣布,已向FDA提交了大麻素药物Epidiolex(cannabidiol,大麻二醇,CBD)口服液体制剂的一份补充新药申请,用于治疗由结节性硬化症(TSC)引发的癫痫。一项III期临床研究显示,与安慰剂相比,Epidiolex能够显著降低患者TSC相关癫痫发作频率:Epidiolex 25mg/kg/天治疗组、50mg/kg/天治疗组相对基线分别降低49%、48%,安慰剂组降低29%(p=0.0009,p=0.00118)。Epidiolex此前在美国已获批用于治疗与Lennox-Gastaut综合征(LGS)和Dravet综合征相关的癫痫发作。
1.我国口罩日产能产量双双突破1亿只。国家发改委2日宣布,按照党中央、国务院部署,我国口罩日产能产量快速增长,双双突破1亿只。据调度,2月29日,包括普通口罩、医用口罩、医用N95口罩在内,全国口罩日产能达到1.1亿只,日产量达到1.16亿只,分别是2月1日的5.2倍、12倍。其中,医用N95口罩日产能产量分别达到196万只、166万只,有效解决了一线医护人员的防护需要。
2.美国公布该国首例新冠肺炎死亡病例。2月29日,美国华盛顿州公布一名新冠病毒感染病例死亡。华盛顿州当天宣布进入“紧急状态”,并称将动用一切必要资源应对疫情。目前,尚不清楚这一病例是如何感染新冠病毒的。另据报道,美国白宫2月29日表示,因新冠肺炎疫情蔓延,美国将对伊朗实施旅行限制措施,并建议公民不要前往意大利和韩国疫情严重的地区。
3.百济神州PD-1定价和慈善援助方案出炉。百济神州PD-1抗体药物替雷利珠单抗注射液(百泽安)的定价和慈善援助方案正式公布。援助方案为:首次申请买2援2,而后患者可灵活选择买2援2一年内循环,或买3援助至一年(最多不超过11个疗程),直到疾病进展或项目结束(以较早者为准)。据悉,百泽安建议售价为10,688元/支(100mg)。这也意味着长期使用百泽安进行治疗的患者只需支付5个疗程的费用即可获得一整年的药物治疗,年治疗费用最低约为10.69万元。援助项目将于3月6日正式启动。
股市资讯
【佐力药业】2019年度实现营业收入9.11亿元(+24.77%);归母净利润0.29亿元(+40.86%)。
【太安堂】公司将其持有的控股子公司康爱多0.5%的股权转让给白云投资,转让金额为1,250.00万元。
【东诚药业】截至2020年2月27日,公司股东鲁鼎思诚累计减持公司股份748.87万股(公司总股本的0.93%),本次计划实施期限已届满。
1. CDE最新受理情况(3月2日)
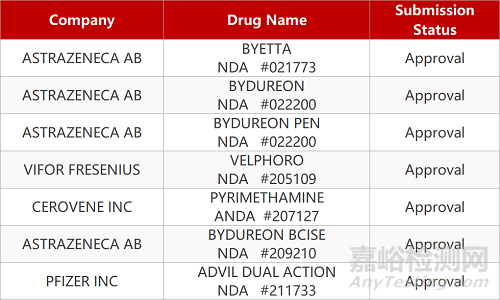
2. FDA最新获批情况(北美2月28日)
- The End -

来源:药研发


