您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-09-30 09:32
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「 本文共:16条资讯,阅读时长约:3分钟 」
今日头条
辉瑞托法替尼在美获批第四项适应症。FDA批准辉瑞(Pfizer)JAK1/JAK3抑制剂托法替尼(XELJANZ®)用于治疗活动性多关节病程的青少年特发性关节炎(pcJIA)2岁及以上儿童和青少年患者。此次批准了两种配方(片剂和口服溶液)。在一项Ⅲ期研究A3921104中,使用托法替尼治疗第18周时,患者达到JIA美国风湿病学会(ACR)30应答(改善超过30%);在44周时,托法替尼治疗组患者的疾病发作率为31%,显著低于安慰剂组(55%)。此前该新药在美国已获批三种适应症。
国内药讯
1.正大天晴卡格列净片获批上市。正大天晴4类仿制药卡格列净片获NMPA批准上市,成为继豪森药业之后该品种国内第2家获批的仿制药。卡格列净是强生开发的一种SGLT-2抑制剂,用于II型糖尿病患者的治疗。2019年,强生卡格列净销售额为7.35亿美元。除豪森药业卡格列净获批之外,同属于SGLT-2抑制剂的恩格列净已经有豪森药业和科伦药业2家仿制药获批。
2.仁合益康药业苯磺酸左氨氯地平片即将获批。河北仁合益康药业4类仿制药苯磺酸左氨氯地平片上市申请进入行政审批阶段,预计即将获批,有望成为该品种首家通过一致性评价的产品。苯磺酸左旋氨氯地平是一种钙离子拮抗剂(CCB)类的降压药,为苯磺酸氨氯地平的左旋体。国内有11家企业拥有该产品的生产批文,2019年中国公立医疗机构及城市零售药店终端合计销售额超过50亿元,目前尚无企业通过一致性评价。
3.君实PD-1联合化疗一线治疗鼻咽癌达Ⅲ期终点。君实生物PD-1特瑞普利单抗(拓益)联合化疗治疗复发/转移性鼻咽癌患者的Ⅲ期临床JUPITER-02结果积极。期中分析结果显示,经IDMC评估,与安慰剂联合吉西他滨/顺铂方案相比,特瑞普利单抗联合吉西他滨/顺铂一线治疗可显著延长患者的无进展生存期。君实生物计划于近期向NMPA及相关国家的药监部门递交其上市申请。就在本月早些时候,特瑞普利单抗用于治疗鼻咽癌获得FDA授予的突破性疗法认定。
4.拜耳sGC激动剂vericiguat拟纳入优先审评。拜耳和默沙东联合开发的sGC激动剂vericiguat片的三个上市申请获国家药监局纳入拟优先审评公示名单,申请的适应症为慢性心力衰竭成人患者(射血分数<45%且发生过心力衰竭加重)。vericiguat早前已在美国、欧洲、日本等多国递交了上市申请;今年7月,FDA已授予其优先审评资格,用于治疗经历心力衰竭恶化事件后射血分数低于45%的症状性慢性心力衰竭患者。本次在中国纳入拟优先审评意味着该药有望加速在华获批上市,有望实现中美欧日同步上市
5.豪森引进的CD19单抗获批临床。由Viela Bio开发的CD19靶向单抗Inebilizumab获国家药监局临床试验默示许可,用于治疗重症肌无力。2019年5月,豪森已以超过2.2亿美元的首付款+里程碑付款获得了该新药在中国的开发和商业化权益。在美国,Inebilizumab已于今年6月获FDA批准上市,用于治疗视神经脊髓炎谱系疾病患者,商品名为Uplizna。截至目前,全球范围内仅有Inebilizumab和Tafasitamab两款CD19 单抗获批上市。
6.香雪制药TCR-T疗法在美国获批临床。香雪精准医疗的合作伙伴Athenex公司细胞疗法TCRT-ESO-A2的新药临床试验申请获得FDA批准,拟开发用于治疗组织基因型为HLA-A*02:01,肿瘤抗原NY-ESO-1表达为阳性的实体瘤。香雪精准医疗已于2018年7月与Athenex公司和Axis公司(为香雪精准与Athenex合资成立)签署协议。香雪精准医疗及其关联方将拥有的针对NY-ESO-1阳性表达的TCR-T细胞治疗技术授予Axis公司在中国大陆地区以外的国家和地区以独占许可的方式使用知识产权,以开发和商业化许可产品和技术。
7.康泰生物新冠灭活疫苗(Vero细胞)获批临床。康泰生物新冠病毒灭活疫苗(Vero细胞)获国家药监局应急批准开展临床试验,拟用于预防由SARS-CoV-2感染引起的新冠病毒肺炎(COVID-19)。临床前研究显示该疫苗在小鼠、大鼠、食蟹猴体内能诱导产生高水平的中和抗体,其食蟹猴攻毒实验表明,接种该疫苗的动物可耐受高滴度新冠病毒攻击,显示出良好的保护效果。目前,该公司的新冠灭活疫苗车间已完成建设,将开始调试、试生产及认证工作。
国际药讯
1.遗传性血管水肿新药Haegarda获FDA扩大适应症。杰特贝林(CSL Behring)C1酯酶抑制剂Haegarda(C1-INH)获FDA批准扩大适应症,用于6岁及以上患者预防遗传性血管水肿(HAE)发作。此次批准,使该药成为用于6岁及以上患者预防HAE发作的唯一一个皮下治疗方案。除了扩大儿科适应症外,更新的标签还包括了孕妇使用Haegarda的临床安全数据。在COMPACT关键研究中,60 IU/kg Haegarda与安慰剂相比将HAE发作次数减少了95%(中位减少)、将急救药物的使用减少了99%以上(中位减少)。
2.盐野义铁载体头孢菌素Fetroja获FDA批准新适应症。FDA批准日本盐野义制药新型抗菌药Fetroja(cefiderocol,头孢地尔)的一份补充新药申请,用于18岁及以上成人患者治疗由易感革兰氏阴性菌引起的医院获得性细菌性肺炎和呼吸机相关细菌性肺炎。Fetroja是首个获得监管批准的具有铁载体功能的抗生素,能够克服革兰氏阴性菌针对抗生素的多种耐药机制。在一项III期APEKS-NP研究中,cefiderocol治疗组与大剂量美罗培兰治疗组在全因死亡率(ACM)方面具有非劣效性(12.4%vs11.6%)。
3.基因泰克口服SMA疗法长期疗效积极。罗氏旗下基因泰克公司口服SMN2基因剪接调节剂Evrysdi(risdiplam)治疗症状性1型脊髓性肌萎缩症(SMA)婴儿患者(年龄为2-7个月)的FIREFISH研究获积极结果。经risdiplam治疗两年后,有88%的婴儿活着,并且不需要接受永久通气;有59%(10/17)的婴儿能够在没有支撑的情况下坐起来至少5秒钟,与治疗1年后(7/17)相比这一比例有所提高;有71%婴儿的CHOP-INTEND运动能力评分达到40分或更高,所有婴儿在24个月的评分优于12个月;在2岁时仍然生存的14例婴儿中,100%能保持吞咽能力。
4.Sarepta基因疗法SRP-9001最新临床数据公布。Sarepta Therapeutics公司拟用于治疗杜氏肌营养不良症(DMD)的基因疗法SRP-9001获阳性临床结果。低剂量SRP-9003组18个月时所有3例患者在所有功能性测量中都继续显示出较基线水平的改善(包括肌营养不良评估(NSAD)、起身时间等指标);6个月时患者NSAD的平均改善为3.0,18个月时为5.7。高剂量组6个月时所有3例患者在所有功能指标上都显示出改善;与基线相比,NSAD平均改善3.7。SRP-9001总体安全可控。
5.第一三共HER3靶向ADC治疗肺癌最新进展。第一三共制药HER3靶向抗体偶联药物patritumab deruxtecan(U3-1402),在经标准疗法(包括一种EGFR TKI)治疗后病情进展的转移性或不可切除性EGFR突变非小细胞肺癌(NSCLC)患者中的I期临床获积极结果。在研究的剂量递增和剂量扩展部分,通过盲法独立中心审查评估,该新药在可评估患者中的客观缓解率为25%,疾病控制率为70%,中位缓解期为6.9个月;45%的患者疾病稳定;patritumab deruxtecan的总体安全性和耐受性与剂量递增阶段一致。
医药热点
1.广州白云区开百万年薪招公立医院院长。9月25日,全国事业单位招聘网发布的《广州市白云区百万年薪保底+高质发展平台公开选聘区属公立医院院长公告》显示,白云区将面向全国选聘广州市白云区妇幼保健院、广州市白云区第三人民医院和广州市白云区石井人民医院院长各1名,报名时间截至2020年10月31日。院长实行年薪制,其年薪与医院发展经营状况、考核结果挂钩,考核结果为合格及以上的,年薪将保持在100万元以上。
2.院士呼吁实施主诊医生负责制。在第十四届中国医院院长年会上,中国医学科学院北京协和医学院院校长王辰再次呼吁三级查房制度转型,实施主诊医生负责制。王辰院士特别强调,主诊医生负责制,“有利于年轻医生成长发展,高年资医生业务提升”。同时,由于其“医疗效率高,医疗责任明确”,患者也能获得高效、优质、连续的医疗照护。此外,主诊医师负责制可以“显著减少住培、专培基地医院的自有医生”,基层将“获得大批规培后的优质医生”。
3.所有医药代表信息或开始上传。上周五中国药学会发布的《关于开展医药代表备案平台使用工作的通知》显示,国家药监局拟于近期将正式发布《医药代表备案管理办法(试行)》,中国药学会受国家药监局委托,承担医药代表备案平台的建设和维护工作。从目前的信息看,医药代表备案平台的建设工作已经完成,现在处于医药代表备案平台试用阶段,药品上市许可持有人使用账号可以登录进入操作界面。
股市资讯
【正海生物】公司于近日取得国家药监局下发的医疗器械注册许可事项变更的《受理通知书》,产品为生物膜,适用于硬脑(脊)膜缺损的修复。
【利德曼】公司于近日取得由北京市药品监督管理局颁发的体外诊断试剂《医疗器械注册证》,产品为心型脂肪酸结合蛋白(H-FABP)测定试剂盒(磁微粒 化学发光法),H-FABP对于诊断急性冠状动脉综合征中不同形式的心肌缺血损伤具有高度敏感性和特异性,且在其他组织损伤时也具有较高的应用价值。
【华海药业】2020年前三季度实现归属于公司股东的净利润预计在8.2亿至8.7亿之间,同期增长约60%到70%,归属于公司股东的扣非净利润预计在7.45亿至8.2亿之间,同期增长约100%到120%。
审评动向
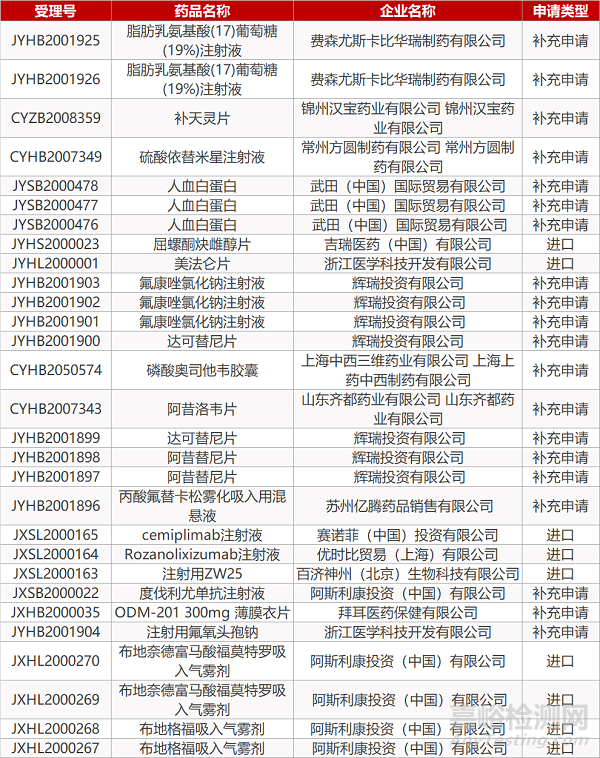
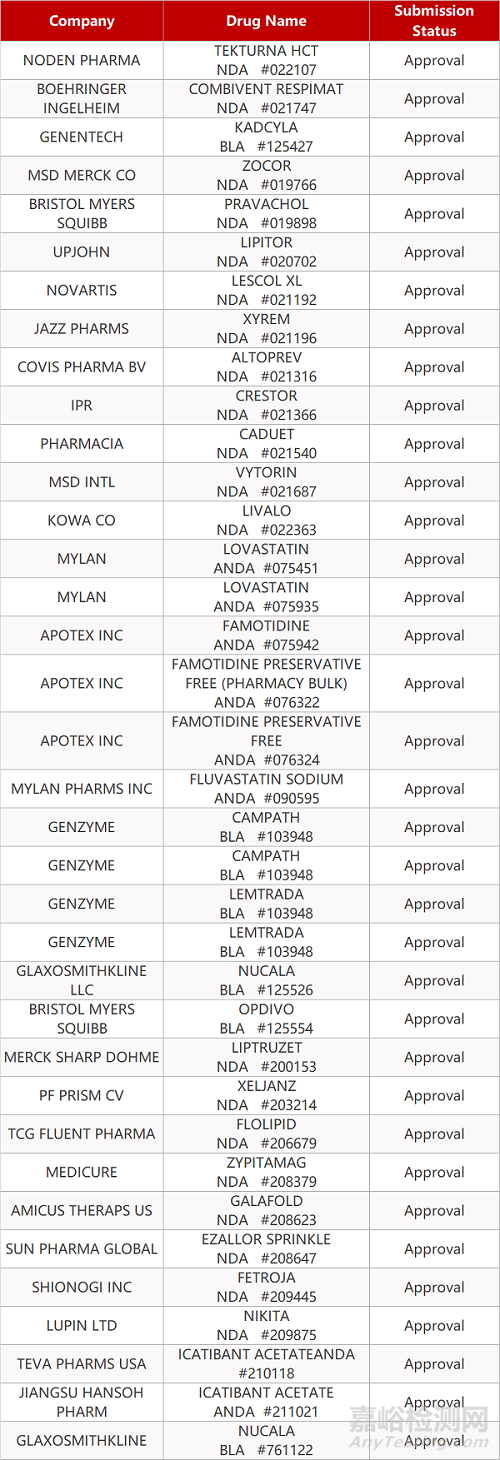
- The End -

来源:药研发


