您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-09-01 12:24
喷雾干燥是一种通过机械设备将液体物料转变成粉状或固体颗粒的一种技术。由于该技术具有耗时短、适用于热敏性物料、干燥产品性质稳定、重现性好、连续、可扩展等突出优势,被广泛应用于各个研究领域[1] [2]。在制剂领域,喷雾干燥不仅可以发挥其传统的干燥脱水作用,还能用于制备和生产各种包载药物的新型药物递送系统如微粒、纳米粒等,通过控制工艺条件可有效地控制药物或载药颗粒的粒径、形态、孔隙率、形态等理化性质,从而改变药物的体内释放、吸收、清除行为,具有很大的应用前景[3]。本文介绍了喷雾干燥的原理、特点、影响因素以及简要总结了其在干粉吸入剂中的应用。
1 原理和特点
喷雾干燥是通过雾化器将料液雾化成直径微小的雾滴,并在干燥塔中与热介质(通常为空气,氮气或二氧化碳)直接接触,然后通过传热和传质过程,迅速将液滴中的水分或溶剂蒸干,最终形成固态粉末或颗粒,随后通过分离装置如旋风分离器来实现气固分离,即可收集干燥产品 (Fig.1)[4]。其中,原料液可以是溶液、混悬液或乳液、也可以是熔融液或膏糊液。所获得的固体颗粒在亚微米到微米级呈现相对窄的粒径分布。与液体制剂相比,加工所得固体产品具有更高的化学和物理稳定性。此外,它们还可以用于生产其他合适剂型(例如胶囊或片剂)的前体[5]。喷雾干燥具有很多优点:(1)干燥效率高,干燥所需时间短;(2)适用于多种物料,包括热敏型材料,且干燥产品特性恒定;(3)操作条件可控,从而调节或控制产品的特性和质量指标;(4)重现性好,适用于工业化大规模生产[3]。
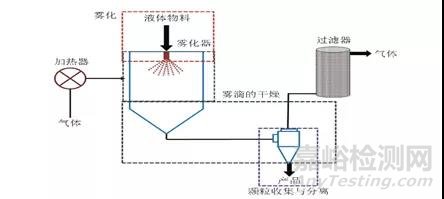
Fig1.喷雾干燥装置及流程
2 影响喷雾干燥的因素
虽然喷雾干燥具有众多优势,但其效率和干燥产品质量受到很多因素的影响,例如雾化器和喷嘴的类型、热介质的种类及温度、流速、分离装置等工艺过程以及料液的流变学性质、浓度、所用辅料等,实际应用时要根据需要加以考察[6]。
2.1干燥系统的类型和工艺参数
2.1.1系统组成
首先是雾化器的类型。常用的雾化器包括气流式、压力式和旋转式三种。旋转式是通过离心作用将液体甩出,在旋转盘边缘破碎成小颗粒,所得液滴粒径分布范围窄,而压力式喷雾器是加压液体通过小孔或涡流室发生雾化,简单但液滴分布宽且易堵塞。雾化器的喷嘴也会影响产品的粒度,大喷嘴直径有利于形成大粒径的产物[7]。其次,料液和气体介质的相对流向,有并流、逆流和混合流。在并流情况下,最终产物存在于最低温度区域,使其成为干燥热敏性物质的首选;而逆流条件下,干燥的产品会接触最热的气体介质,从而具有更高的热效率。此外,分离器的类型也会影响产品的分离和收集效率[3]。
2.1.2干燥介质及其流速
干燥介质是传热和传质的载体,它的流速、比热和与液滴之间的温度差决定了干燥过程中能量交换的效率。常用的雾化干燥介质包括空气、N2和 CO2[8]。质轻的介质可以在雾化过程中获得较小的液滴尺寸和较快的运动速度。干燥气体还有一定的增塑作用,这取决于气体在聚合物中的溶解度,与空气和 CO2相比,使用 N2时乳糖的结晶度最高且形态有差异[8]。降低干燥气体流速会使得颗粒在干燥室内停留时间更长,从而减少了溶剂残留,而较高的流速则可能获得更小的颗粒粒径[9]。
2.1.3干燥温度
入口干燥温度直接影响液滴的传热和传质过程,从而影响液滴形貌和表面特性和内部的水分分布。较高的入口温度会导致粒径增大有利于物料干燥完全,但会破坏热敏性物质的活性。相反,温度较低,物料干燥不完全,容易结块,降低产率[10]。
2.2物料性质
流体进料特性(如浓度、粘度、密度表面张力和溶剂沸点)也会显著影响最终产品的特性。例如,高浓度料液有利于形成较大的颗粒,低表面张力的流体则产生较小的颗粒尺寸,低沸点的流体通常会产生具有多孔表面的颗粒,疏水性辅料的应用会提高粉末的流动性和分散性[11]。
3 在干粉吸入剂中的应用
肺部给药是借助呼吸气流将药物递送至肺部,从而发挥肺局部作用或吸收入血发挥全身疗效。因其吸收面积大、气血屏障薄、酶活性低、无首过效应等优势,被广泛研究用于治疗哮喘、COPD等肺局部疾病及糖尿病等全身性疾病[12]。肺部给药主要有三种方式:气雾剂、喷雾剂和干粉吸入剂。喷雾干燥技术已被广泛研究应用于制备干粉吸入剂[5]。但干粉吸入制剂的研发还存在一些挑战,首先,气道逐级分叉的结构会影响药物的沉积。通常,只有空气动力学直径(MMAD)在1-5μm之间的粒子能够沉积于肺深部。但同时,几何粒径介于1-5μm 的微粉化药物具有粘附性,易聚集,流动性较差,会极大降低药物的肺部沉积率。其次,肺泡区域的巨噬细胞会吞噬和清除粒径1-3μm的外来异物[13]。通过调整喷雾干燥工艺参数和制剂处方组成,可改善微粉化药物流动性和分散性,制备多孔微粒、纳米粒聚集体等新型肺部递送系统,从而有效提高肺部递送效率和避免清除[14]。
3.1 纯药物或药物与载体混合物
目前,已上市的干粉吸入剂大多都是纯微粉化药物或者药物与辅料的混合物。可通过将药物或与载体混合物(干粉吸入剂中最常见载体为乳糖、甘氨酸等)溶于溶剂中,采用喷雾干燥技术制得适合粒径和较窄粒径分布的干粉颗粒。从吸入装置中的射出剂量(ED)和可吸入粒子百分比(FPF)或FPD是关键的质量评价指标,ED>75%和FPF>40% 才满足干粉吸入剂的评估标准[14]。通常,粒径越大,粉体流动性越好,ED 越大,但 FPF随之降低,会导致肺部沉积率和药效降低,因此,需要在此之间找到平衡。
Silvia Belotti等以阿米卡星为模型药物,PEG-32硬脂酸脂为表面活性赋形剂,用含乙醇的水溶液溶解后经喷雾干燥制成干粉,作者应用了质量源于设计(QbD)理念,研究了5个关键因素:(A)干燥温度(B)进料速度(C)乙醇浓度(D)赋形剂浓度(E)药物浓度对最终产品质量的影响[15],实验方案如Table 1所示。
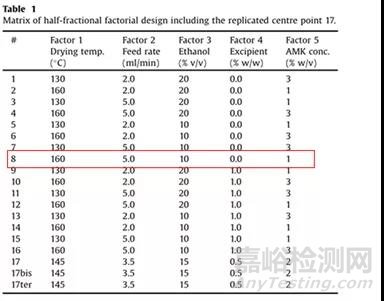
结果表明,该19次实验所得粒子的粒径(D50)均在2-3um之间,扫描电镜下粒子形态如Fig.2所示,含赋形剂的喷雾干燥颗粒中,小粒子数目高于不含赋形剂的粒子,推测粒子间相互作用力会增大,易聚集,会导致FPD和ED降低。Fig.3(A, B)结果证实了这一点,含赋形剂的实验组的FPD和ED值普遍低于不含赋形剂组。且从图中可以看出,在实验序号为8的条件下,粒子聚集前后ED值相同且高于80%(药物用量为10mg),同时ED值也接近60%,且Fig.3 (C, D)表明D因素(赋形剂浓度)对FPD和ED 值会产生很大的负面影响,说明PEG-32硬脂酸脂不适合用作该药物的赋形剂。其次药物浓度和乙醇浓度会有一定的影响,而其他因素影响不大。
综上所述,在序号为8的实验条件下,即干燥温度160度,乙醇浓度10%,药物浓度1%时,可保证粉末的吸入性能良好。

Fig.2 喷雾干燥所得粒子的扫描电镜(SEM)图(A) 含赋形剂(B)不含赋形剂
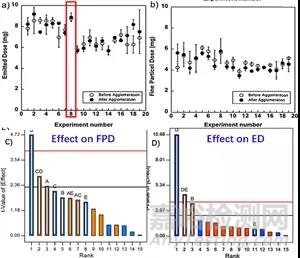
Fig.3 阿米卡星喷雾干燥粉末的(A)ED和(B)FPD的值以及pareto图分析的各因素及其交互作用对(C)FPD和(D)的影响程度排序
3.2 多孔微粒
多孔微粒结构疏松多孔,是通过增加粒子孔隙率、降低颗粒密度以增加粒子的几何直径,从而克服颗粒间的相互作用力,改善粒子的流动性和分散性,可通过调节喷雾干燥的各项参数,使载药多孔微粒的粒径在5μm以上,而由于密度低赋予粒子的空气动力学直径低于5 μm,从而实现较高的肺部沉积效率,以及逃逸肺部网状内皮系统的摄取,延长肺内滞留时间[16]。为通过喷雾干燥技术制备多孔微粒,定义了peclet系数,即溶质从液滴外围扩散到其中心所需的时间与液滴干燥所需的时间(Td)之比。第一个时间取决于液滴半径的平方(R2)与溶质或纳米粒扩散系数(D)之比。这个比值表征了扩散和对流的相对重要性(Eq. 2):
式中,Pe是peclet数,R是液滴半径,D是扩散系数,Td是液滴干燥所需时间[20]。对于吸入制剂,最佳的peclet数应该远大于1,因为这表明分子重新分布到液滴中心的时间更短,从而在空气-水界面处的积聚,产生的颗粒相对疏松。反之,当peclet数小于1时,分子加速向液滴中心扩散,会产生相对致密的干燥颗粒,颗粒小,粒子间粘附力大不利于肺部递送。因为干燥时间长会通过作用力(即范德华力)或在赋形剂基质中固化促进分子凝聚,导致基质在干燥早期阶段形成壳。增加气压可使壳破裂并继续泄漏,最后产生多孔颗粒。PulmoSpheres技术是通过喷雾干燥制备可吸入的多孔微粒,且成功放大生产应用于市场的一个成功案例。该方法是用乳剂作为料液,以可挥发的PFOB作为油相,在喷雾干燥时PFOB挥发过程中可使粒子形成疏松多孔的结构 [18]。
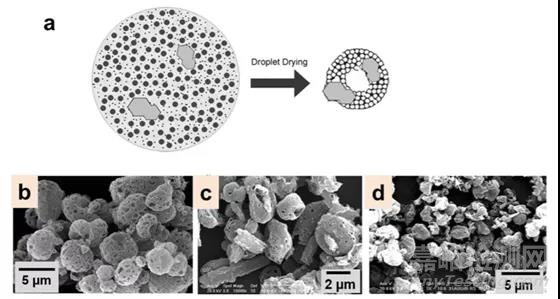
Fig.4 通过喷雾干燥技术制成载药多孔微粒的示例
3.3 纳微颗粒
由于纳米粒粒径太小,易被呼出,研究者提出了一种纳微颗粒,可通过纳米喷雾干燥技术(NSD)使纳米粒聚集成适合吸入的微米级别的粒子,吸入体内后又可解离成纳米粒子来发挥其优势。NSD的原理是在高频振动下,药物溶液透过亚微米孔以细小波长喷射入热气体中,溶剂瞬间蒸发形成纳微颗粒,并且采用超高压静电场来捕集 NSD颗粒[6]。这是由于传统的分离技术已无法回收超细颗粒[19]。
徐恩宇等[20]采用这种纳米喷雾干燥技术,以一水合乳糖(LAC)、可溶性淀粉(STA)、海藻糖(TRE)和-环糊精(CD)为辅料,制备载硫酸沙丁胺醇的NSD颗粒。
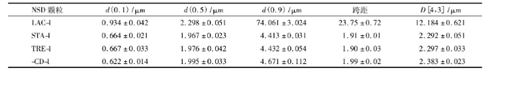
粒径和形貌如Fig.5和Table.2所示,所有粒径的D50值均在2um左右,适合于肺部吸入,但其中LAC-1的D90值为74 um,说明粒径分布极其不均匀。LAC-1制成的颗粒(Fig.5A)表面光滑饱满,而STA-1,TRE-1和-CD-1制成的颗粒表面“褶皱”明显,“凹陷”增多,表面粗糙度增加(Fig.5B~D),有利于降低粒子间粘附力,提高流动性和分散性。

Fig.5不同颗粒的NSD扫描电镜图A:一水合乳糖LAC-1(×3000);B:可溶性淀粉STA-1(×5 000);C:海藻糖TRE-1(×3000);D:环糊精CD-1(×3 000)
Table 2不同辅料制成的纳微颗粒的粒径比较结果(n=3)
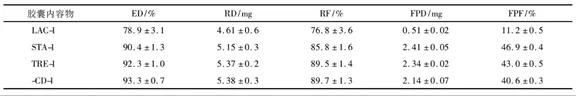
用新一代级联撞击器(NGI)测得的体外沉积结果Table 3显示,以STA-1,TRE-1,CD-1为辅料制备的颗粒喷射剂量(ED)均高于90%,回收率RF(%)高于85%,可吸入百分比FPF(%)值高于40%,满足肺部递送干粉的要求。
Table 3 不同辅料制成的纳微颗粒的体外肺沉积效果(n=3)
因此,以环糊精、可溶性淀粉和海藻糖作为辅料,通过纳米喷雾干燥技术可制得粒径在肺部吸入范围内的纳微颗粒,还可改善药物颗粒的流动性,具有良好的体外沉积行为,提高药物的肺部递送效率。
4. 结语
喷雾干燥因其技术较为成熟,具备多种优势,被广泛用于工业生产中,在肺部干粉吸入制剂领域也得到了广泛研究,可用于制备各种传统的和新的剂型。通过改变设备的系统组成、工艺参数以及料液的组成和性质可显著影响最终产物的特性,应根据其最终用途合理设计试验参数。总而言之,随着仪器的更新和技术的发展,喷雾干燥技术在制药工业领域中具有十分广阔的应用前景。
参考文献
[1]安振华.喷雾干燥技术的应用综述[J].中国粉体工业,2020(04):1-3.
[2]Alaa Hamed Salama. Spray drying as an advantageous strategy forenhancing pharmaceuticals bioavailability[J]. Drug Delivery and Translational Research,2020,10(1).
[3]Alejandro Sosnik,Katia P. Seremeta. Advantages and challenges of thespray-dryingtechnology for the production of pure drug particles and drug-loadedpolymericcarriers[J]. Advances in Colloid and Interface Science,2015,223.
[4]万锋 .喷雾干燥技术在新型制剂设计与生产中的应用 [J].药学进展,2019,43(03):174-180.
[5] Takashima Y, Saito R,NakajimaA,et al.Spray-drying preparation of microparticles containing cationic PLGA nanospheresas gene carriers for avoiding aggregation of nanospheres. Int J Pharm 2007;343:262-9
[6]陈娟,杨志强,张坤,潘凤,王杏林.纳米喷雾干燥技术的特点及其在药物制剂领域中的应用[J].中国新药杂志,2017,26(05):519-524.
[7]Yang M.Spray drying pharmaceuticals[J].Eur Pharm Review,2011,16(6):64-68.
[8]Islam M I U, Langrish T A G. The effect of different atomizing gases and drying mediaon the crystallization behavior of spray-dried powders[J]. Drying Technology,2010, 28(9):1035-1043.
[9]傅胜,施湘君.喷雾干燥技术在制备固体分散体中的应用研究进展[J].浙江化工,2020,51(07):22-25.
[10] Brinkmann-tretienes U, Barnert S,Bauer-brandl A.Single step bottom-up processto generate solid phospholipidnano-particles[J].Pharm Dev Technol,2014,19(3) :326-332.
[11]徐景娜,周学海,杨敏,郭志红,李志万,孙亮,韩英,肺部吸入制剂的研究概况,药物评价研究,42(2019)2305-2308.
[12]Angelika Jüptner,Regina Scherlie.Spray Dried Formulations for Inhalation-MeaningfulCharacterization of Powder
Properties[J].Pharmaceutics,2020,12(1)
[13]Z. Liang, R. Ni, J.Zhou, S.Mao,Recent advances in controlled pulmonary drugdelivery, Drug DiscovToday, 20(2015) 380-389.
[14]王丽丽,祝美华,刘正平,张建强,肺部给药新剂型国内外研究进展,中国新药与临床杂志, 35 (2016) 171-177.
[15] Belotti S,Rossi A,ColomboP,et al.Spray dried amikacin powder for inhalation incystic fibrosis patients:A qualityby design approach for product construction[J].International Journal ofPharmaceutics, 2014,471(1-2):507-515.
[16] F. Emami, S.J. Mostafavi Yazdi, D.H. Na,Poly(lacticacid)/poly(lactic-co-glycolic acid) particulate carriers forpulmonary drug delivery,Journal of Pharmaceutical Investigation, 49 (2019) 427-442.
[17]Chow A H L,Tong H H Y,ChattopadhyayP,etal.Particle engineering for pulmonary drug delivery[J] .Pharm Res,2007,24(3):411-437.
[18] Weers J G, Miller D P, Tarara T E. Spray-Dried PulmoSphere Formulations forInhalation Comprising Crystalline Drug Particles [J]. AAPSPharmSciTech, 2019, 20(3): 103.
[19]郭静,李浩莹.纳米喷雾干燥技术在药物研究中的应用研究进展[J].中国医药工业杂志,2013,44(4):399-403.
[20]徐恩宇,姜俊峰,徐颖,王洋,李浩莹.用于肺部药物递送的纳米喷雾干燥粉雾剂[J].中国新药杂志,2016,25(19):2262-2267.

来源:药事纵横


