您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-10-17 11:23
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
凡恩世FIC双抗获FDA临床批件。凡恩世公司DLL3/CD47双抗PT217的I期临床试验申请获FDA批准,拟评估用于小细胞肺癌(SCLC)和其他神经内分泌癌患者的安全性和有效性。PT217是凡恩世创新双特异性抗体平台PACbody™开发的一款“first-in-class”抗体,这种不需要蛋白质工程来构建天然IgG结构的双特异性抗体专有方法,使得该抗体分子保持具有卓越CMC特性的天然结构。2022年6月,FDA已授予PT217孤儿药资格,拟用于SCLC的治疗。
国内药讯
1.海思科环泊酚获批新适应症。海思科静脉麻醉1类创新药环泊酚注射液(HSK3486)的新适应症获国家药监局批准,用于妇科门诊手术的镇静及麻醉。HSK3486是一款GABAA受体激动剂,可通过作用于GABAA受体介导的氯离子通道,增加电流的传导,引起神经元的超极化,以达到抑制中枢神经系统产生麻醉的作用。该新药已获批的适应症包括消化道内镜检查中的镇静,全身麻醉诱导、支气管镜检查中的镇静、全身麻醉诱导和维持、重症监护期间的镇静。
2.辉瑞JAK抑制剂新适应症在华获批上市。辉瑞枸橼酸托法替布片的新适应症获国家药监局批准,推测适应症为「用于活动性银屑病关节炎的治疗」。枸橼酸托法替布片是一款JAK抑制剂,目前在全球已获批类风湿性关节炎、溃疡性结肠炎和银屑病关节炎、幼年特发性关节炎和强直性脊柱炎等适应症。2019年9月,正大天晴开发的托法替布获批上市,为该品种国内首个仿制药。
3.协和麒麟CCR4单抗在华获批上市。协和麒麟莫格利珠单抗获国家药监局批准上市,用于既往接受过至少一次全身性治疗的蕈样肉芽肿(MF)或Sézary综合征(SS)成人患者的治疗。莫格利珠单抗是FDA批准上市的首个CCR4靶向生物药。CCR4通过与相应配体结合可以调节调节性T细胞和NK细胞等免疫细胞的功能,同时在CTCL细胞表面过表达的CCR4可作为特异性治疗靶点,实现对肿瘤细胞的靶向杀伤。
4.科济BCMA靶向CAR-T拟纳入优先审评。科济药业BCMA CAR-T产品泽沃基奥仑赛注射液(CT053)获CDE拟纳入优先审评,拟用于既往接受过至少一种免疫调节剂和蛋白酶体抑制剂治疗失败的复发或难治性多发性骨髓瘤患者。公布于《Haematologica》上的IIT试验结果显示,中位随访为17.4个月时,总缓解率达到87.5%,其中完全缓解率为79.2%。此前,该新药已获FDA和EMA授予孤儿药资格、再生医学先进疗法以及优先药物。
5.复星凯特CAR-T新适应症拟纳入优先审评。复星凯特CAR-T疗法「阿基仑赛注射液」新适应症申请获CDE拟纳入优先审评,用于二线治疗大B细胞淋巴瘤成人患者。阿基仑赛(Yescarta)是国内首款获批的CAR-T,靶向CD19跨膜蛋白,已获批用于二线或以上系统性治疗后复发或难治性LBCL患者。在ZUMA-7试验中,Yescarta用于二线治疗较标准二线治疗显著提高患者的无事件生存期(8.3个月v2.0个月)。
国际药讯
1.艾伯维乌帕替尼在日获批用于UC治疗。艾伯维口服JAK抑制剂乌帕替尼在日本获批新适应症,用于传统治疗效果不佳的中重度溃疡性结肠炎(UC)患者的诱导缓解和维持治疗。在U-ACHIEVE和U-ACCOMPLISH诱导研究中,乌帕替尼的临床缓解率为26%(vs5%)和33%(vs4%);在U-ACHIEVE维持治疗研究中,乌帕替尼的临床缓解率分别为42%和52%,而安慰剂仅有12%。该新药用于UC的上市申请已获CDE受理,有望在近期获批。
2.血友病基因疗法向FDA重报BLA。FDA受理BioMarin公司AAV5基因疗法valoctocogene roxaparvovec(valrox)重新递交的生物制品许可申请(BLA),用于治疗严重血友病A成人患者,预计明年3月31日之前做出回复。valrox旨在通过单次输注,向患者体内递送凝血因子VIII功能基因,恢复VIII的产生,从而消除或减少静脉VIII输注需求。在GENEr8-1试验中,valrox可使患者的凝血因子VIII使用率和需要接受治疗的年出血率分别降低了99%和84%(p<0.001)。该新药有望成为FDA批准用于这类患者的首款基因疗法。
3.长效GLP-2激动剂Ⅱ期临床积极。VectivBio公司GLP-2激动剂apraglutide治疗短肠综合征(SBS-IF)的Ⅱ期临床结果积极。中期分析显示,一周一次apraglutide治疗6个月后,患者在所需静脉输注支持体积上有平均50%的下降,其中该指标至少有20%下降的患者比例高达80%(n=4/5),且至少在6个月中有1天不需静脉输注支持。该试验首次验证并显示GLP-2激动剂用于连续结肠(CIC)SBS-IF患者的治疗效力。
4.癌症免疫三联疗法Ⅱ期临床结果积极。PDS Biotechnology公司HPV16靶向免疫疗法PDS0101与默克IL-12免疫调节剂M9241和PD-L1/TGF-β融合蛋白bintrafusp alfa构成的三联疗法,在治疗HPV阳性、且免疫检查点抑制剂(CPI)难治性的癌症患者的Ⅱ期临床扩展研究结果积极。历史数据中,这类患者的中位总生存期仅为3-4个月。而该项研究16个月时的随访数据显示,有66%(19/29)患者依然活着,未发现5级治疗相关不良事件(AE)。
5.法布里病创新基因疗法早期临床积极。Sangamo公司一次性输注、靶向肝脏的法布里病候选基因疗法ST-920在Ⅰ/Ⅱ期临床中获积极结果。最新随访数据显示,该疗法的总体耐受性良好,没有发生与治疗有关的严重不良事件;所有9例患者均表现出α-Gal A酶活性的持续升高(约为正常值的2-30倍),有1例患者α-Gal A的改善持续长达23个月。该基因疗法目前正准备启动Ⅲ期临床试验。
6.右美沙酮抑郁症III期临床失败。Relmada公司新型NMDA受体通道阻滞剂REL-1017(右美沙酮)用于治疗重度抑郁症(MDD)的III期研究未能达到主要终点。REL-1017组第28天时患者的MADRS10评分改善(-14.8分)较安慰剂组(-13.9分)无统计学意义。在本研究中,安慰剂组的反应高于预期,并且在某些研究中心观察到矛盾的结果,即安慰剂的效果显著优于REL-1017。目前,Relmada正在调查这些结果的背后原因。
医药热点
1.医保局:将继续采用“两票制”。10月12日,国家医保局发布《关于政协十三届全国委员会第五次会议第04377号 (医疗卫生类414号) 提案答复的函》,对“关于取消医疗机构药品耗材采购‘两票制’的提案”做出答复。国家医保局表示,目前国家组织的药品集中带量采购共采购294种药品,占公立医疗机构化学药和生物药年采购金额的35%,地方也探索了部分品种的集采,但尚有大量的品种未被覆盖;医疗机构药品耗材采购“两票制”仍发挥着重要作用,目前并不适合取消“两票制”。
2.上海规范公立互联网医院复诊服务收费。上海市医保局、卫健委联合发布关于推进上海市“互联网+”医疗服务价格管理的通知。通知明确,公立医疗机构开设的互联网医院,由不同级别医务人员提供的互联网复诊服务,均按照实体医疗机构“普通门诊诊查费”项目的价格标准执行。医疗机构向患者提供不属于诊疗活动的服务以及非医务人员提供的服务,不得作为医疗服务价格项目向患者收费。此外,在前期试点的基础上,试行“互联网远程特约高级专家诊察费”“互联网远程会诊费”等互联网特需医疗服务价格项目,实行市场调节价管理。
3.南京建成全国首家体育医院。10月15日,南京市体育医院在南京市中医院挂牌成立。这是全国首家以三级甲等综合医院为依托的体育医院,将以“运动促进健康中心、运动康复中心、运动医学科”三中心为基础,建设集一楼层的体检中心、二楼层的专家门诊区、功能检查区和运动教学区、三楼层的治未病中心和运动处方门诊区等综合服务为一体的体育医院核心区,为各类人群提供国民体质监测、体适能检测、体质健康检查、中医健康干预、运动干预等五大类服务。
评审动态
1. CDE新药受理情况(10月14日)
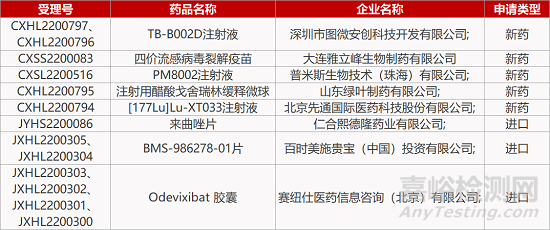

来源:药研发


