指示剂是化学试剂中的一类。在一定介质条件下,其颜色能发生变化、能产生浑浊或沉淀,以及有荧光现象等。常用它检验溶液的酸碱性;滴定分析中用来指示滴定终点;环境检测中检验有害物。一般分为酸碱指示剂、氧化还原指示剂、金属指示剂、吸附指示剂等。
指示剂分类
1、酸碱指示剂
指示溶液中H+浓度的变化,是一种有机弱酸或有机弱碱,其酸性和碱性具有不同的颜色。
以甲基橙(Ka=10-3.4)为例,溶液的pH<3.1时,呈酸性,具红色;ph>4.4时,呈碱性,具黄色;而在pH3.1~4.4,则出现红黄的混合色橙色,称之为指示剂的变色范围。不同的酸碱指示剂有不同的变色范围。
2、混合酸碱指示剂
注:混合酸碱指示剂要保存在深色瓶中。
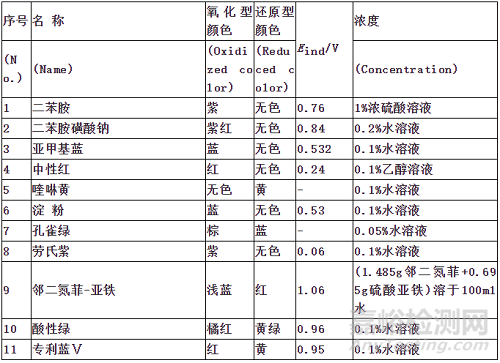
3、氧化还原指示剂
氧化还原指示剂用于氧化还原法容量分析。下表列出一些在教学和工作中经常使用的部分氧化还原指示剂。
4、络合指示剂
在络合滴定中,通常都是利用一种能与金属离子生成有色配合物的显色剂来指示滴定过程中金属离子浓度的变化,此种显色剂称为金属离子指示剂,即络合指示剂。
5、吸附指示剂
吸附指示剂对滴定条件的要求:指示剂的吸附能力弱于待测离子。
吸附指示剂是一类有机染料,用于沉淀法滴定。当它被吸附在胶粒表面后,可能是由于形成了某种化合物而导致指示剂分子结构的变化,从而引起颜色的变化。在沉淀滴定中,可以利用它的此种性质来指示滴定的终点。
吸附指示剂可分为两大类:一类是酸性染料,如荧光黄及其衍生物,它们是有机弱酸,能解离出指示剂阴离子;另一类是碱性染料,如甲基紫等,它们是有机弱碱,能解离出指示剂阳离子。
6、荧光指示剂
滴定和确定浑浊液体和有色液体的pH可以使用荧光指示剂。在滴定过程中荧光色变不受液体颜色和其透明度的影响,因此常被选用。
指示剂作用原理
在实际工作中,肉眼是难以准确地观察出指示剂变色点颜色的微小的改变。人们目测酸碱指示剂从一种颜色变为另一种颜色的过程,只能在一定的pH变化范围内才能发生,即只有当一种颜色相当于另一种颜色浓度的十倍时才能勉强辨认其颜色的变化。在这种颜色变化的同时,介质氢灭菌生物指示剂的pH值则由一个值变到另一个值。
溶液的颜色变化范围称为指示剂的变色范围即变色域。在变色范围内,当溶液的pH值改变时,碱色成分和酸色成分的比值随之改变,指示剂的颜色也发生改变。指示剂的变色范围约2个pH单位。由于人的视觉对各种颜色的敏感程度不同,加上在变色域内指示剂呈现混合色,两种颜色互相影响观察,所以实际观察结果与理论值有差别,大多数指示剂的变色范围小于2个pH单位。
指示剂的用量问题
双色指示剂的变色范围不受其用量的影响,但因指示剂本身就是酸或碱,指示剂的变色要消耗一定的滴定剂,从而增大测定的误差。对于单色指示剂而言,用量过多,会使用变色范围向pH值减小的方向发生移动,也会增大滴定的误差。例如:用0.1mol/LNaOH滴定0.1mol/LHAc,pHsp=8.5,突跃范围为pH8.70-9.00,滴定体积若为50mL,滴入2~3滴酚酞,大约在pH=9时出现红色;若滴入10~15滴酚酞,则在pH=8时出现红色。显然后者的滴定误差要大得多。
指示剂用量过多,还会影响变色的敏锐性。例如:以甲基橙为指示剂,用HCl滴定NaOH溶液,终点为橙色,若甲基橙用量过多则终点敏锐性就较差。
常用指示剂的配制(供参考)
(具体配制方法以实验标准为准)
1、二苯胺磺酸钠指示液:取二苯胺磺酸钠0.2g,加水100mL使溶解,即得。
2、二苯偕肼指示液:取二苯偕肼1g,加乙醇100mL使溶解,即得。
3、双硫腙指示液:取双硫腙50mg,加乙醇100mL使溶解,即得。
4、石蕊指示液:取石蕊粉末10g,加乙醇40mL,回流煮沸1小时,静置,倾去上层清液,再用同一方法处理二次,每次用乙醇30mL,残渣用水10mL洗涤,倾去洗液,再加水50mL,煮沸,放冷,滤过,即得。变色范围pH4.5~8.0(红→蓝)。
5、甲酚红指示液:取甲酚红0.1g,加0.05mol/L氢氧化钠溶液5.3ml使溶解,再加水稀释至100mL,即得。变色范围 pH7.2~8.8(黄→红)
6、甲酚红-麝香草酚蓝混合指示液:取甲酚红指示液1份与0.1%麝香草酚蓝溶液3份,混合,即得。
甲基红指示液取甲基红0.1g,加0.05mol/L氢氧化钠溶液7.4mL使溶解,再加水稀释至200mL,即得。变色范围 pH4.2~6.3(红→黄)。
7、1g/L(0.1%) 甲基红指示剂的配制方法
所需药品:甲基红。
用途:配制甲基红-溴甲酚绿混合指示剂。
配制方法:称取1g甲基红,用1000mL无水乙醇溶解。
8、甲基红-亚甲蓝混合指示液:取0.1%甲基红的乙醇溶液20mL,加0.2%亚甲蓝溶液8mL,摇匀,即得。
9、甲基红-溴甲酚绿混合指示液:取0.1%甲基红的乙醇溶液20mL,加0.2%溴甲酚绿的乙醇溶液30mL,摇匀,即得。
10、0.1%(1g/L)甲基橙指示液:取甲基橙0.1g,加水100mL使溶解,热溶解,冷却后过滤备用。变色范围 pH3.2~4.4(红→黄)。
说明:每100 mL滴定液加1滴。加的量太多,反而不明确。本指示液适用于弱碱或氨、氢氧化钙、氢氧化锶、氢氧化钡、氢氧化镁的滴定,不适用于弱酸,例如氢氰酸、碳酸、亚砷酸、硼酸、铬酸、有机酸的滴定,因此滴定强酸时,这些酸共存是没有影响的。硝酸能破坏甲基橙,故不适用,但可加入过量的碱再进行滴定。甲基橙也用于乙醇溶液的滴定。
11、甲基橙-二甲苯蓝FF混合指示液:取甲基橙与二甲苯蓝FF各0.1g,加乙醇100mL使溶解,即得。
12、邻二氮菲指示液:取硫酸亚铁0.5g,加水100mL使溶解,加硫酸2滴与邻二氮菲0.5g,摇匀,即得。本液应临用新制。
13、茜素磺酸钠指示液:取茜素磺酸钠0.1g,加水100mL使溶解,即得。变色范围 pH3.7~5.2(黄→紫)
14、荧光黄指示液:取荧光黄0.1g,加乙醇100mL使溶解,即得。
15、钙黄绿素指示剂:取钙黄绿素0.1g,加氯化钾10g,研磨均匀,即得。
16、钙紫红素指示剂:取钙紫红素0.1g,加无水硫酸钠10g,研磨均匀,即得。
17、姜黄指示液:取姜黄粉末20g,用冷水浸渍4次,每次100mL,除去水溶性物质后,残渣在100℃干燥,加乙醇100mL,浸渍数日,滤过,即得。
18、结晶紫指示液:取结晶紫0.5g,加冰醋酸100mL使溶解,即得。
19、酚酞指示液:0.1%(1g/L)酚酞指示剂的配制方法
0.1% 的酚酞指示剂是指100mL溶液使用 0.1g 的酚酞。
配置方法:称量 0.1g 酚酞,然后用少量95%乙醇或者无水乙醇溶解,定量转移至100mL容量瓶后再用乙醇定容稀释到100mL即可。
0.5%(5g/L)酚酞指示剂的配制方法
取 0.5g 酚酞,溶于乙醇,用乙醇稀释至 100mL,无需加水。变色范围 pH8.3~10.0(无色→红)。
说明:本指示液对酸敏感,例如,对碳酸变色,可用来检查是否含碳酸气。适用于强碱滴定无机酸、有机弱酸,也适用于乙醇溶液的滴定。强酸滴定弱碱(例如氨)不适合。硅酸和铝存在,对本溶液变色无妨碍。与浓碱接触红色消失。
20、铬黑T指示剂(5g/L)的配制方法 :称取0.50g铬黑T和4.5g氯化羟胺,溶于乙醇中,用乙醇稀释至100mL,贮存于棕色瓶中。可保持数月不变质。
21、5g /L淀粉指示液:取可溶性淀粉0.5g,加水5mL搅匀后,缓缓倾入100mL沸水中,随加随搅拌,继续煮沸2分钟,放冷,倾取上层清液,即得。本液应临用新制。
22、碘化钾淀粉指示剂的配制方法 :取碘化钾 0.2g ,加新制的淀粉指示液100mL使溶解。
23、硫酸铁铵指示液:取硫酸铁铵8g,加水100mL使溶解,即得。
24、溴酚蓝指示液:取溴酚蓝0.1g,加0.05mol/L氢氧化钠溶液3.0mL使溶解,再加水稀释至200mL,即得。变色范围 pH2.8~4.6(黄→蓝绿)。
25、溴麝香草酚蓝指示液:取溴麝香草酚蓝0.1g,加0.05mol/L氢氧化钠溶液3.2mL使溶解,再加水稀释至200mL,即得。变色范围 pH6.0~7.6(黄→蓝)。
26、麝香草酚酞指示液:取麝香草酚酞0.1g,加乙醇100mL使溶解,即得。变色范围 pH9.3~10.5(无色→蓝)。
27、麝香草酚蓝指示液:取麝香草酚蓝0.1g,加0.05mol/L氢氧化钠溶液4.3mL使溶解,再加水稀释至200mL,即得。变色范围 pH1.2~2.8(红→黄);pH8.0~9.6(黄→紫蓝)。