今日头条
兴齐眼药改良型伏立康唑上Ⅰ期临床。兴齐眼药2.2类化药伏立康唑滴眼液针对真菌性角膜炎适应症的Ⅰ期临床首例受试者入组。伏立康唑属于广谱的三唑类抗真菌药,能抑制真菌麦角甾醇的生物合成,对念珠菌、曲霉菌等真菌均具有杀菌作用。该项试验拟通过健康受试者的单次及多次给药,评估伏立康唑滴眼液在健康受试者中的安全性、耐受性和药代动力学特征。
国内药讯
1.康方PD-1/VEGF双抗肺癌Ⅱ期临床见刊。康方生物PD-1/VEGF双抗依沃西单抗注射液(AK112)联合化疗治疗晚期非小细胞肺癌(NSCLC)的Ⅱ期临床研究结果发表于《柳叶刀》子刊eClinical Medicine上。结果显示,AK112联合化疗一线治疗晚期NSCLC,治疗EGFR-TKI进展的EGFR突变的晚期非鳞NSCLC,以及治疗经PD-1抑制剂联合含铂双药化疗治疗进展的晚期NSCLC,均具有良好的抗肿瘤活性和安全性,为该患者群体提供潜在的新治疗选择。目前,该药的上市申请已获得CDE受理。
2.辉大眼科基因疗法获罕见儿科疾病认定。辉大基因基于CRISPR基因编辑技术开发的新型眼科基因治疗药物HG004获得FDA授予罕见儿科疾病认定,用于治疗由RPE65突变引起的遗传性视网膜疾病。HG004旨在利用重组腺相关病毒载体将功能性人类RPE65基因递送到视网膜,以恢复RPE65的功能。此前,该公司已在中美两国取得HG004的临床批件,计划同步开展国际多区域临床试验。
3.信达PD-1/IL-2双抗临床前研究见刊。信达生物PD-1/IL-2双特异性抗体融合蛋白IBI363的临床前核心机制研究结果发表在Nature子刊Nature Cancer上。研究显示,该产品IL-2臂采用α-biased设计,在提高疗效的同时降低IL-2相关毒性,而PD-1结合臂可以实现对PD-1的阻断和IL-2的选择性递送;IBI363能同时阻断PD-1/PD-L1通路和激活IL-2通路,更高效地实现对肿瘤特异性T细胞的靶向和激活。目前IBI363在中国和澳大利亚针对晚期实体瘤或淋巴瘤开展I期临床。
4.映恩Trop2-ADC授权BioNTech。映恩生物宣布与BioNTech达成新的合作协议,将其专有DITAC平台开发的第三代Trop2靶向ADC药物DB-1305的全球范围内(不包括中国大陆、香港及澳门)的商业化权利授予BioNTech公司。目前,DB-1305正在Ⅰ/Ⅱ期临床在评估用于实体肿瘤的治疗潜力。今年4月,映恩生物已与BioNTech达成独家许可协议,授予BioNTech在全球(不包括中国大陆、香港和澳门地区)开发、生产及商业化两款ADC(DB-1303和DB-1311)的权利。
5.亚宝药业引进山西大学1.1类中药。亚宝药业与山西大学就后者开发的1.1类中药“柴归颗粒”签订技术转让协议。柴归颗粒主治疏肝解郁,健脾养血,适用于轻、中度抑郁症并属肝郁脾虚证者。根据协议,山西大学需完成IIa期临床试验并向亚宝药业提供试验总结报告;如果试验结果符合预期,亚宝药业将负责后续的开发工作。此项交易金额为2600万。
6.启明医疗人工肺动脉瓣膜获批临床。启明医疗宣布其自主研发的经导管人工肺动脉瓣膜置换(TPVR)系统VenusP-Valve的研究性器械豁免(IDE)申请获得FDA完全批准,即将在美国开展临床研究。VenusP-Valve是III类心血管植入类医疗器械,已于去年4月获得欧盟CE MDR认证。VenusP-Valve欧洲三年期随访数据显示,64例接受TPVR手术的患者(尚有部分患者由于新冠疫情未能计入)手术成功率为100%,全因死亡率及手术再干预率均为0。
国际药讯
1.安斯泰来C5抑制剂眼科适应症获批上市。安斯泰来补体C5抑制剂avacincaptad pegol玻璃体内注射液(Izervay)获FDA批准上市,用于治疗年龄相关性黄斑变性(AMD)引起的地图样萎缩(GA)。在两项III期临床(GATHER1和GATHER2)中,与假性注射相比,Izervay治疗在基线至12个月内GA面积的平均增长率分别显著降低35%(p=0.0050)与18%(p=0.0039)。此前,该疗法曾被FDA授予用于治疗GA的突破性疗法认定。
2.第五代头孢抗生素在美报NDA。Basilea公司第五代头孢抗生素ceftobiprole(头孢比罗酯)已向FDA提交新药申请,用于治疗金黄色葡萄球菌菌血症(SAB)、急性细菌性皮肤和皮肤结构感染(ABSSSI)和社区获得性细菌性肺炎(CABP)。在III期ERADICATE研究中,头孢比罗酯治疗SAB患者的效果非劣效于达托霉素(69.8%vs68.7%);在TARGET研究中,头孢比罗酯用于ABSSSI患者的缓解率非劣效于万古霉素联合氨曲南治疗(91.3%vs88.1%);在III期研究中,头孢比罗酯在CABP患者中的临床治愈率非劣效于头孢曲松联合利奈唑胺治疗方案(86.6%vs87.4%)。华润三九拥有该新药的中国权益。
3.晖致每月1次MS新药在美报NDA。晖致与Mapi Pharma开发的长效注射制剂GA Depot(醋酸格拉替雷,40mg)用于治疗复发型多发性硬化症(MS)的新药申请(NDA)获FDA受理,PDUFA日期为2024年3月8日。在Ⅲ期临床中,与安慰剂相比,GA Depot使患者的年复发率显著降低了30.1%。格拉替雷是一款MHC-II调节剂,原研产品由梯瓦开发,商品名为Copaxone,已于1996年在美国获批用于治疗多发性硬化症。
4.FIC社恐新药III期研究积极。Vistagen公司潜在“first-in-class"鼻喷雾剂PH94B(fasedienol)治疗社交恐惧症(SAD)的III期PALISADE-2研究结果积极。与安慰剂相比,PH94B治疗显著改善患者的主观焦虑量表评分(-13.8分vs-8.0分),显著提高患者的临床应答率(40.6%vs18.6%);此外,PH94B的耐受性良好,未见报告严重不良事件。蔼睦医疗拥有该产品在中国、韩国和东南亚地区的开发和商业化权益。
5.基孔肯雅病毒疫苗达Ⅲ期临床主要终点。Bavarian Nordic公司基于佐剂病毒样颗粒(VLP)的基孔肯雅病毒候选疫苗CHIKV VLP(PXVX0317)用于成人和青少年接种的Ⅲ期临床达到所有共同主要终点。单次接种后第22天,有98%疫苗接种者中可诱导强烈的基孔肯雅中和抗体;而且有86%的受试者在接种后6个月仍具有达血清保护性的中和抗体水平。CHIKV VLP总体良好耐受性,不良事件主要为轻中度。
6.HER2靶向CAR-IMANs临床前研究积极。LIfT BioSciences公司基于第二代N-LIfT平台开发的靶向HER2的CAR-中性粒细胞疗法,在离体患者类肿瘤模型中的临床前研究结果积极。研究显示,与未经修饰的免疫调节性α中性粒细胞(IMANs)相比,HER2 CAR-IMANs的肿瘤杀伤力增强了4倍,有望实现所有实体肿瘤治疗的完全缓解潜力。今年5月,该公司已对外宣布其中性粒细胞输注疗法IMAN在临床前表现出对胰腺癌类肿瘤的有效杀伤。
医药热点
1.上海市发布医疗纠风工作要点。8月7日,上海市卫健委联合13部门发布《关于印发上海市2023年纠正医药购销领域和医疗服务中不正之风工作要点的通知》,公布本年度上海市医疗纠风的工作要点,以及13部门任务分工表、医疗机构行风建设自查自纠表。《工作要点》指出要整治行业组织存在的不正之风问题。重点是各级各类行业组织或学(协)会在工作或推进业务主管部门委托事项过程中的不正之风问题,尤其关注新型、隐蔽的,以“捐赠”、学术活动、举办或参加会议等名义变相摊派,为非法输送利益提供平台,违规接受捐赠资助等问题。
2.华西四院引进29款新药。8月7日,四川大学华西第四医院发布通知,拟公开引进29款新药以满足临床用药需求。29个拟引进的新药中,独家品种占比超过30%,包括7款化学药和2款中成药。其中,开喉剑喷雾剂(儿童型)是贵州三力制药的独家儿科中成药,对手足口病、咽喉炎、扁桃体炎、疱疹性咽峡炎、口腔溃疡等儿童常见的呼吸道感染性疾病治疗有明显优势。
3.跨国药企2023H1营收Top10出炉。根据跨国药企2023第二季度财报,2023上半年营收Top10依次是:强生(502.76亿美元,+6%)、罗氏(342.25亿美元,-2%)、辉瑞(310.15亿美元,-42%)、默沙东(295.22亿美元,-3%)、诺华(265.75亿美元,5%)、艾伯维(260.90亿美元,-7%)、赛诺菲(237.48亿美元,4%)、百时美施贵宝(225.37亿美元,-4%)、阿斯利康(222.95亿美元,4%)、葛兰素史克(181.65亿美元,-2%)。
评审动态
1. CDE新药受理情况(08月02日)
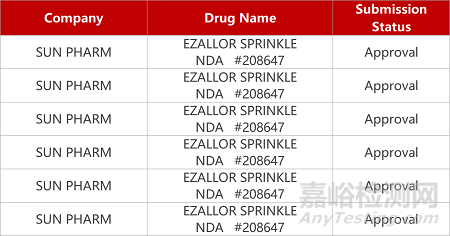
2. FDA新药获批情况(北美08月04日)