今日头条
鞍石c-MET抑制剂获批上市。鞍石生物旗下浦润奥生物c-Met抑制剂1类新药伯瑞替尼肠溶胶囊获国家药监局批准上市,用于治疗具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌(NSCLC)患者。在Ⅱ期临床中,伯瑞替尼总体缓解率ORR为75%,DCR为96.2%,mDoR为15.9个月。此前,该新药已被CDE纳入突破性治疗品种和优先审评通道。
国内药讯
1.亿腾引进心血管创新药报新NDA。亿腾医药从Amarin公司引进的二十碳五烯酸乙酯软胶囊(Icosapent Ethyl,唯思沛)新适应症上市申请获CDE受理,与他汀类药物联合使用,用于确诊心血管疾病或糖尿病伴≥2种其他心血管疾病危险因素,合并高甘油三酯血症的成年患者,以预防和降低心血管事件风险(包括心血管死亡、心肌梗死、卒中、冠状动脉血运重建和不稳定型心绞痛需住院治疗)。此前,该产品已获批用于降低重度高甘油三酯血症成年患者的甘油三酯水平。
2.赛诺菲补体C1s抑制剂拟纳入突破性品种。赛诺菲1类生物制品BIVV020注射液获CDE拟纳入突破性治疗品种,拟用于治疗慢性炎性脱髓鞘性多发性神经根神经病(CIDP)。BIVV020(SAR445088)是一款补体C1s抑制剂,目前正在概念验证Ⅱ期临床中评估用于治疗CIDP成人患者的安全性和耐受性。该项研究中国主要研究者为复旦大学附属华山医院赵重波主任医师。
3.甫康「奈拉替尼」获批胃癌脑转移Ⅱ期临床。甫康药业泛HER酪氨酸激酶抑制剂马来酸奈拉替尼片获国家药监局批准开展Ⅱ期临床,评估用于HER2阳性晚期胃食管癌脑转移成人患者的有效性与安全性。该产品由Puma公司原研,已于2017年获FDA批准用于HER2阳性早期乳腺癌曲妥珠单抗辅助治疗后的强化辅助治疗。2020年4月,北海康成引进的原研产品获批中国上市,商品名为贺俪安。
4.康宁杰瑞HER2双抗ADC早期临床积极。康宁杰瑞HER2双抗ADC药物JSKN003(KN026-ADC)治疗HER2表达晚期实体瘤经治患者的澳大利亚I期研究(JSKN003-101)结果积极。数据显示,JSKN003总体ORR为46.7%,DCR为90.0%;其中HER2低表达乳腺癌患者的ORR为40.0%,HER2高表达乳腺癌患者的ORR为75.0%;临床中,没有患者发生药物相关严重不良事件。
5.中国抗体制药CD22单抗报老年痴呆IND。中国抗体制药CD22抗体药物舒西利单抗(suciraslimab,SM03)的新药研究申请获CDE受理,该公司计划在中国开展治疗早期症状性阿尔茨海默病(AD)的Ⅰ期临床,评估suciraslimab用于治疗AD导致的轻度认知障碍或轻度痴呆的安全性与初步疗效。今年4月,该新药已在治疗类风湿关节炎(RA)的III期临床(SM03-RA-III)达到主要终点。suciraslimab用于治疗RA的上市申请目前正接受CDE监管审查。
国际药讯
1.BMS新一代ROS1/NTRK抑制剂获批上市。Turning Point公司(已被百时美施贵宝收购)新一代ROS1/NTRK抑制剂Repotrectinib(瑞普替尼)获FDA批准上市,用于治疗ROS1阳性局部晚期或转移性非小细胞肺癌(NSCLC)患者,商品名为Augtyro。在I/II期TRIDENT-1研究中,ROS1 TKI初治队列中,全球cORR为79%,中国亚组cORR为91%;在既往接受过1个前线ROS1 TKI+1个前线化疗的经治队列中,全球cORR为42%,中国亚组cORR为67%。再鼎医药拥有repotrectinib的大中华区权益。
2.FDA批准首款抗菌CLS上市。FDA批准CorMedix公司导管锁定溶液(CLS)DefenCath(牛磺罗定和肝素)上市,专门用于减少患有肾功能衰竭的成人患者通过中心静脉导管(CVC)接受长期血液透析时发生的与导管相关的血流感染(CRBSIs)。这是FDA批准的首款抗菌CLS。在Ⅲ期临床LOCK-IT-100中,与肝素相比,DefenCath作为CLS将CRBSIs风险降低71%。
3.甲状旁腺功能减退症新药重新报NDA。Ascendis公司基于与FDA在A类会议中的沟通结果,重新向FDA递交其长效甲状旁腺激素前药TransCon PTH(palopegteriparatide)上市申请,用于治疗成人甲状旁腺功能减退症(HP)。此次,Ascendis公司提交了新的TransCon PTH的生产控制策略,旨在保证TransCon PTH药品或设备均一的递送剂量。在Ⅲ期临床中,TransCon PTH组患者实现不依赖常规治疗并保持血清钙水平在正常范围内的比例较安慰剂组更高(78.7%vs4.8%)。
4.LENZ公司融资推进老花眼新药Ⅲ期临床。LENZ Therapeutics与Graphite Bio公司宣布合并成立新公司LENZ Therapeutics,并完成5350万美元的融资,用于推动新公司主打研发项目盐酸醋克利定滴眼液(LNZ100)和醋克利定溴莫尼定滴眼液(LNZ101)的Ⅲ期临床进展,评估用于改善老视人群近视力的疗效与安全性。去年10月,这两款滴眼液已在治疗老花眼的Ⅱ期临床达到主要终点,使用眼药水1小时后,两组患者的缓解率分别达到71%和56%。
5.吉利德购进BCMA-CAR-T开发许可。吉利德旗下Kite公司扩展与Arcellx公司的合作协议,行使选择权,获取Arcellx公司开发、拟用于治疗骨髓瘤的CART-ddBCMA疗法(靶向BCMA的下一代CAR-T疗法)ACLX-001的研发许可。根据协议,Arcellx公司将获得2亿美元的股权投资和8500万美元的预付款。该协议还包括CART-ddBCMA在淋巴瘤治疗进展和ARC-SparX许可相关的潜在里程碑以及其它里程碑付款。
6.新一代TCR药物公司完成A轮融资。T-Therapeutics公司宣布完成4800万英镑(约5900万美元)A轮融资,以用于发现和开发针对癌症和炎症性疾病的新型TCR治疗药物。T-Therapeutics源自剑桥大学,其专有转基因小鼠平台OpTiMus,它能生成包含几乎无限多优化TCR的TCR库,为设计开创性疗法提供基础构件。此轮融资由Sofinnova Partners、F-Prime Capital、Digitalis Ventures和Cambridge Innovation Capital领投,赛诺菲风投和剑桥大学创投基金参投。
医药热点
1.中疾控:10月新增127例猴痘确诊病例。11月16日,中国疾控中心在官网披露2023年10月猴痘疫情监测情况。2023年10月1日-31日,中国内地(不含港澳台)新增报告127例猴痘确诊病例,其中广东17例、上海16例、浙江15例、北京13例、四川12例,无重症、死亡病例。根据流行病学调查分析,98.2%病例为男性,90.0%病例明确为男男性行为人群。
2.复旦儿科新生儿科新大楼即将投用。复旦大学附属儿科医院日前透露,该院新生儿科新大楼即将投入使用,院方计划设立25间母婴同室的家庭病房,可同时为25个患儿家庭提供家庭参与式的照护服务。复旦大学附属儿科医院是国家儿童医学中心,承担着上海乃至全国大量新生儿尤其是疑难重症新生儿的医疗救治保障工作。近两年来,新生儿科每年收治体重不足1500克的极低出生体重早产儿每年多达200余例。
3.广西桂东人民医院腹痛中心启用。11月14日,广西壮族自治区桂东人民医院举行腹痛中心揭牌启用仪式。腹痛中心建设围绕“以患者为中心”的理念,整合涵盖涉及腹痛的所有相关专业(包括消化内科、普通外科、急诊科、泌尿外科、重症医学科、心血管内科、妇科、产科、麻醉科、介入室、影像科等科室),搭建一站式快速诊治平台,为急性腹痛患者进行全面、精准的诊疗服务。
评审动态
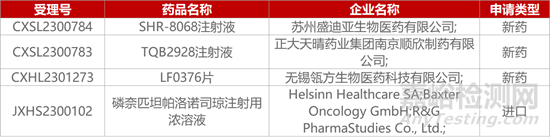
1. CDE新药受理情况(11月16日)
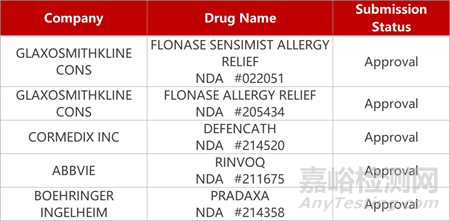
2. FDA新药获批情况(北美11月15日)