您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-12-27 08:40
对于应用于皮肤的外用药品,生物等效性(BE)通常是基于可比性临床终点研究来确定的。 但是,此类研究昂贵且耗时,可能涉及数百至数千名患者,研究终点需要数周至数月才能显现。为了评估外用药品BE研究的更具创新性和成本效益的科学有效方法,FDA 药物审评与研究中心(CDER)的研究人员以及麻省总医院,哈佛医学院和麻省理工学院的研究人员进行了首次同类研究[1],评估使用无创受激拉曼散射显微镜(SRS)评估外用产品生物利用度和 BE。该研究建立了初步可行性以及在实施SRS评估外用产品生物利用度和BE测量时提高可靠性和专属性的方法。
对于系统性作用的药品,药物利用度的速率和程度可以通过具有药代动力学(PK)终点的BE研究来有效地证明。全身 PK 研究是通过抽血或其它生物体液取样以及测定药物浓度直接进行的,许多口服仿制药产品已由此通过 ANDA 途径获得批准。相比之下,对于应用于皮肤的局部作用的外用药品,药物在体循环中可能无法测量。即使可检出,也不能假定全身 PK 必然反映皮肤PK,因为体循环通常在皮肤作用部位的下游,并且一些来自皮肤的药物在到达体循环之前可能独立分布到其它生物区室。几十年来,人们已经充分了解评估局部用仿制药的皮肤生物利用度或 BE 相关的挑战,并广泛讨论更有效的替代 BE 方法。迄今为止,已经提出了各种基于体外和体内皮肤PK(cPK)的技术,例如体外渗透试验,皮肤微量透析,皮肤开放式微量灌注和胶带剥离,但这些方法也都存在挑战.
非侵入性光学工具,如荧光显微镜、共聚焦拉曼光谱和SRS显微镜,显示出可用于cPK研究的前景。共聚焦拉曼光谱(CRS)能够通过药物化学结构产生的内在分子振动来检测药物,并且不需要标记(例如,放射性标记)。然而,CRS 的自发拉曼信号本质上是微弱的,从而限制了对组织结构中发生的动态变化进行高分辨率成像的能力。像 CRS 一样,SRS是一种通过化学结构检测药物的非破坏性光学方法。SRS 基于同时使用两个针对分子的特定拉曼活性振动的脉冲激光源。当两个来源的频率差异与样品中的分子振动共振相匹配时,产生的信号比通过自发拉曼方法获得的信号大几个数量级。SRS的特点是空间和时间分辨率高。重要的是,信号不受背景干扰(包括自体荧光),并且信号强度与分子浓度成线性比例,从而能够对整个组织的药物进行定量成像。
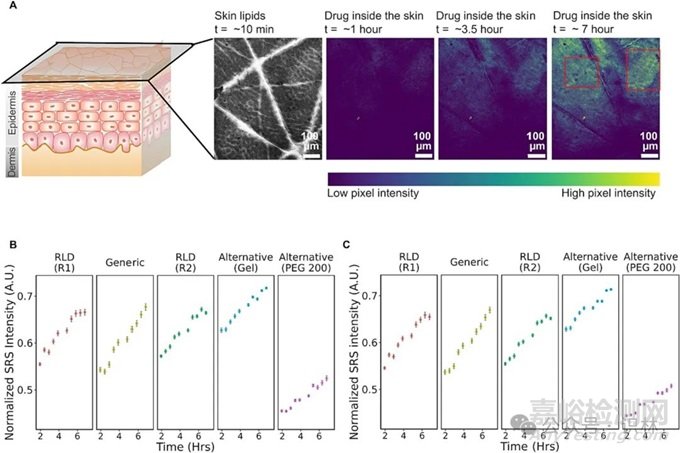
CDER 研究人员提出了一种基于 SRS 成像和使用聚合物标准参照进行信号归一化评估外用BE的新方法。使用他扎罗汀(一种治疗轻中度斑块状牛皮癣,寻常痤疮和光老化的局部外用药)的市售配方研究了拟议方法的概念证明。用于研究的是分别作为参照上市药品(RLD)的 Tazorac® 乳膏 0.1% 和仿制药他扎罗汀乳膏,以及替代配方(Tazorac® 0.1% 凝胶)。对归一化强度与时间曲线(AUC)下的 cPK 参数和峰值药物浓度进行统计学比较,以调查(1)RLD 和仿制药之间的局部BE; (2) 参比制剂的他扎罗汀渗透率与阴性对照以及单独治疗组相比。
实施了两组使用 0.1% 乳膏(RLD)的实验,其结果分别标记为 R1 和 R2(见图B)。R1 和 R2 之间的分析有助于显示实验之间的差异以及其如何影响 BE 的评估。R1 和 R2 的值符合预期的 BE 标准。此外,比较 RLD(R1)和仿制药,这些值也在[0.8,1.25]范围内,表明两种产品之间的预期 BE。另一种含有聚乙二醇作为载体的制剂被证明与 RLD 不是生物等效的。值得注意的时,比较 RLD(R1)和替代配方(Tazorac® 0.1%凝胶),富含脂质的细胞间片区域和缺乏脂质的角质细胞空间的值都在[0.8,1.25]范围内。这表明尽管成分不同,上皮层产品的 cPK 仍在可接受的BE范围内。
这些结果共同证明了 SRS 成像评估外用产品 BE 的潜在能力。此外,开发的 SRS 方法能够研究从皮肤的不同微观结构计算的 BE cPK参数。在特定的微观结构区域建立 BE 的能力对于通过特定的渗透途径更好,更快地开发产品具有巨大的潜力。
该技术目前的局限性包括分析敏锐度的穿透深度,其中一些通过目前的方法得到改善,但对于许多外用产品来说仍然是现实问题。
[1] Iliopoulos, F., Tu, D., Pence, I. J., Li, X., Ghosh, P., Luke, M. C., ... & Evans, C. L. (2024). Determining topical product bioequivalence with stimulated Raman scattering microscopy. Journal of Controlled Release, 367, 864-876.

来源:识林


