您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-05-28 08:31
干法制粒的研发包括处方和工艺两部分,两者均能对制剂的理化性质产生重大影响。处方部分需要重点关注活性物质的粒径、晶型及晶癖等,功能性辅料如崩解剂、润湿剂的种类、用量及加入方式等,工艺部分需要重点关注送料转速、压辊转速、压辊压力、筛网目数、颗粒堆密度、粒径分布、片的硬度、包衣增重等。制剂处方工艺的不同可能会崩解出不同大小和均匀性的颗粒,显示出不同的溶出速度和程度,进而影响BE的通过率。
本文旨在深入了解影响干法制粒的处方和工艺的基础上,筛选出关键处方、工艺参数,以提高自制制剂与参比制剂的体外溶出拟合度为目的,采用正交试验设计,优化干法制粒的处方和工艺,形成科学有效的干法制粒研发策略。
1、干法制粒工艺
干法制粒工艺是将混匀的药物粉末运送到挤压区,运用机械力作用在对旋轧辊间挤压物料,再将压缩成片状或块状的物料粉碎成所需粒径的颗粒。
2、研发策略
(1)处方
①初始处方设计

本品为4类仿制药,采用干法制粒工艺制备的薄膜包衣片。
具体工艺包括:
1)混合:将处方量的API与甘露醇(过60目筛)、微晶纤维素(过60目筛)、十二烷基硫酸钠、低取代羟丙基纤维素(过60目筛)混合均匀(搅拌转速50r/min,10min);
2)干法制粒:送料转速25rpm,压辊转速8rpm,压轮压力2.5MPa,预整粒50rpm、终整粒转速80rpm,20目筛网整粒。
3)总混:整粒后的物料与硬脂酸镁(过60目)1:1手动混合1min,再与低取代羟丙基纤维素(过60目)混合均匀(搅拌转速50r/min,10min);
4)压片:理论片重200mg,重量差异±4.5%,目标硬度:100 N (80 N ~120N);
5)包衣:目标增重:2.5%(2.0%~3.0%);
②关键物料分析
1)活性成分
活性物质的粒径、晶型等,直接影响制剂的溶出速度和程度。根据参比制剂公开的处方信息,采用与参比制剂相同的晶型,参比制剂公开的处方信息未显示活性物质的具体粒径范围,咨询原料药厂家并结合相关专利信息,活性物质的粒径范围缩小至20um~40um,需要根据小试数据验证这一粒径范围。
2) 填充剂-甘露醇、微晶纤维素
填充剂作为制剂处方的重要组成部分,主要作用是用来改善物料的性能,如改善流动性,从而便于分装,改善可压性,从而便于压片,增加体积助制剂成型。
根据参比制剂公开的处方信息,该制剂的填充剂包括甘露醇和微晶纤维素。甘露醇的性质非常稳定,与活性成分相容性良好,具有低吸湿性和良好的可压性。微晶纤维素的性质也非常稳定,与大多数药物不起作用,原辅料相容性优异,流动性、可压性好,结合力强,对药物有较大的容纳量,可用于粉末直压工艺。参比制剂公开的处方信息显示甘露醇的用量为50mg/片、微晶纤维素的用量为120mg/片。
3) 崩解剂-低取代羟丙基纤维素
崩解剂作为制剂处方的重要组成部分,主要作用是使片剂在胃肠液中迅速裂碎成细小颗粒。崩解剂具有很强的吸水膨胀性能,能够瓦解片剂的结合力,使片剂从一个整体的片状物裂碎成许多细小的颗粒,加快片剂中主药的溶解和吸收。
根据参比制剂公开的处方信息,该制剂的崩解剂是低取代羟丙基纤维素。低取代羟丙基纤维素具有很大的表面积和孔隙度,它有很好的吸水速度和吸水量,崩解后的颗粒细小,利于药物的溶出。参比制剂公开的处方信息显示低取代羟丙基纤维素用量占素片4%,即用量为8mg/片,参比制剂公开的工艺信息显示,低取代羟丙基纤维素采用内外加入方法,内外加入具体数量未显示。
4) 表面活性剂-十二烷基硫酸钠
表面活性剂作为制剂处方的特殊组成部分,在制剂阶段对药物粉末有增加黏合性和润滑性的作用,从而改善物料的性能,以便后续制粒工艺的进行,在治疗阶段对制剂有增溶和助溶作用,从而改善药物的生物利用度。
根据参比制剂公开的处方信息,该制剂的表面活性剂是十二烷基硫酸钠。十二烷基硫酸钠是分子中带有性质不同的亲水基和疏水基的两亲结构化合物,是一种在药物制剂中常用的增溶剂和助溶剂。在片剂中加入适量的十二烷基硫酸钠可提高片剂的润湿性能,加速水分的透入,增大药物的溶出速度,使片剂较快的崩解。参比制剂公开的处方信息显示十二烷基硫酸钠用量占素片5%,即用量为10mg/片,参比制剂公开的工艺信息显示,十二烷基硫酸钠采用内外加入方法,内外加入具体数量未显示。
5) 润滑剂-硬脂酸镁
润滑剂作为制剂处方的重要组成部分,主要作用是降低颗粒之间摩擦力从而改善粉末流动性,便于药物粉末分装或压片。
根据参比制剂公开的处方信息,该制剂的润滑剂是硬脂酸镁。硬脂酸镁为疏水性润滑剂,易与颗粒混匀,压片后片面光滑美观。用量一般为0.1%~1%,用量过大时,由于其疏水性,会造成片剂的崩解(或溶出)迟缓。参比制剂公开的处方信息显示硬脂酸镁的用量为2mg/片。
6) 包衣剂-胃溶型薄膜包衣预混剂
包衣剂作为制剂处方的重要组成部分,主要作用是改善制剂外观、增加制剂稳定性、掩盖不良嗅味等。
根据参比制剂公开的处方信息,该制剂的包衣剂是胃溶型薄膜包衣预混剂。胃溶型薄膜包衣预混剂为色泽均匀的颗料型粉未,无臭、无味,常作为中、西药物固体制剂、丸剂、颗粒剂的胃溶型包衣材料。参比制剂公开的处方信息未显示胃溶型薄膜包衣预混剂的用量,通过对参比制剂分析,素片包衣后增重约2.5%,即用量为5mg/片。
7)小结
通过对以上六种原辅料的分析,可知填充剂-甘露醇、微晶纤维素的处方量已确定,润滑剂-硬脂酸镁的处方量已确定,通过对参比制剂分析,包衣剂-胃溶型薄膜包衣预混剂的处方量已确定。
需要考察的参数有活性成分的粒径范围,崩解剂-低取代羟丙基纤维素内外加入的具体量,表面活性剂-十二烷基硫酸钠内外加入的具体量。采用科学的正交试验设计,通过考察工艺的顺畅性,溶出曲线的拟合性,从而筛选出活性成分的粒径范围,崩解剂-低取代羟丙基纤维素内外加入的具体量,表面活性剂-十二烷基硫酸钠内外加入的具体量。
③正交试验
1)正交试验设计

2)正交试验数据
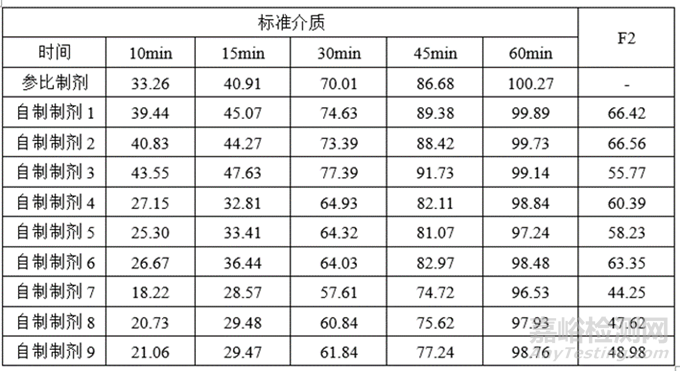
3)正交试验分析
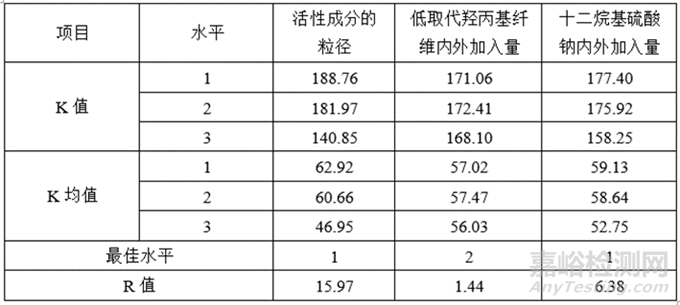
4)最佳水平试验设计

5)最佳水平试验数据
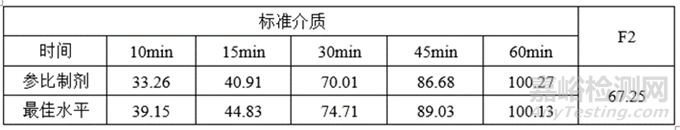
6)根据R值优化试验设计-筛选活性成分的粒径范围

7)优化后的试验数据-筛选活性成分的粒径范围
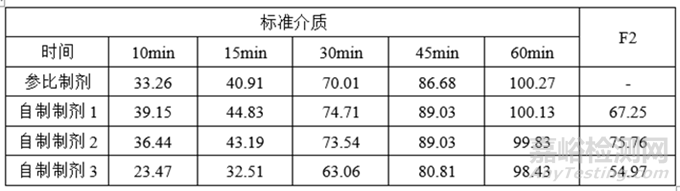
④处方确定
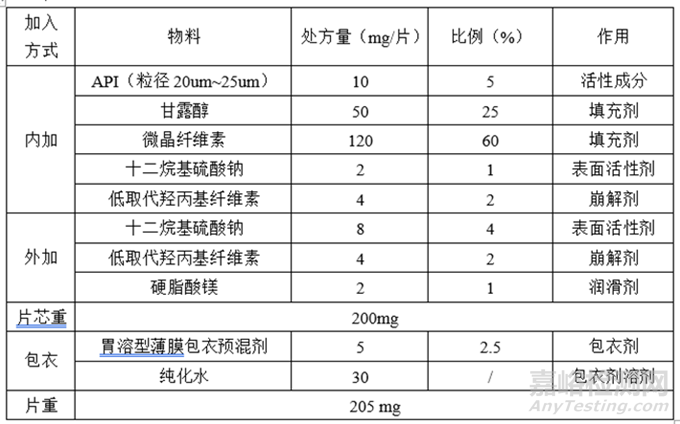
(2)工艺
①初步工艺
具体工艺包括:
1)混合:将处方量的API与甘露醇(过60目筛)、微晶纤维素(过60目筛)、十二烷基硫酸钠、低取代羟丙基纤维素(过60目筛)混合均匀(搅拌转速50r/min,10min);
2)干法制粒:送料转速25rpm,压辊转速8rpm,压轮压力2.5MPa,预整粒50rpm、终整粒转速80rpm,20目筛网整粒。
3)总混:整粒后的物料与硬脂酸镁(过60目)1:1手动混合1min,再与低取代羟丙基纤维素(过60目)混合均匀(搅拌转速50r/min,10min);
4)压片:理论片重200mg,重量差异±4.5%,目标硬度:100 N (80 N ~120N);
5)包衣:目标增重:2.5%(2.0%~3.0%);
②关键工艺参数(CPPs)分析
1)送料转速
送料转速是指将物料运送到进料区的速度,物料间隙中的气体在进料区排出,称预排气,排气效果有送料转速和压辊转速共同决定,送料转速/压辊转速比值越大,排气效果越好。送料转速与压辊转速、压辊压力协同作用影响干法制粒的颗粒性能,在工艺可接受的情况下,倾向于使用更大的送料转速以提高生产效率。
2)压辊转速
压辊转速是指压辊运转的速度,压辊转速决定了物料通过轧合区的速度,影响物料的排气效果和压实性,压辊转速快:排气效果差、压实性差、再次可压性好,压辊转速慢:排气效果好、压实性好、再次可压性差。压辊转速是制约干法制粒生产效率的绝速步骤,在工艺可接受的情况下,倾向于使用更大的压辊转速以提高生产效率。
3)压辊压力
压辊压力是指压辊施加在物料上的力,直接影响物料的压实程度,压辊压力小:压出的片/块易碎、细粉多、再次可压性好、溶出快,压辊压力大:压出的片/块易硬、细粉少、再次可压性差、溶出慢,在工艺可接受的情况下,倾向于使用更小的压辊压力,以保证后续工序的顺利进行。
4)压辊间隙
压辊间隙是指两个压辊间的最近点距离,直接影响压出的片/块的厚度,压辊间隙与压辊间物料所受的压力大小及压辊间隙通过的物料数量密切相关,压辊间隙属于被动调节值。
5)粉碎速度
粉碎速度是指压出的片/块在粉碎室被切割刀粉碎的速度,粉碎速度直接影响颗粒的粒度分布和颗粒形态,需根据工艺要求并结合筛网目数进行考察。
6)筛网目数
筛网目数是指干法制粒机筛网孔直径的大小,直接影响颗粒的粒度分布,筛网过大:颗粒粒度过大、形态不规则,筛网过小:细粉过多、流动性差,需根据工艺要求并结合粉碎速度进行考察。
通过对以上6个关键工艺参数并结合小试研发数据进行分析,可知压辊间隙属于被动调节值,送料转速、压辊转速、粉碎速度和筛网目数经试验验证,工艺稳定可靠。
自制制剂溶出速度快于参比制剂,拟通过增加压辊压力从而降低自制制剂的溶出速度,进而提高自制制剂与参比制剂的体外溶出拟合度。
③试验
1)试验设计
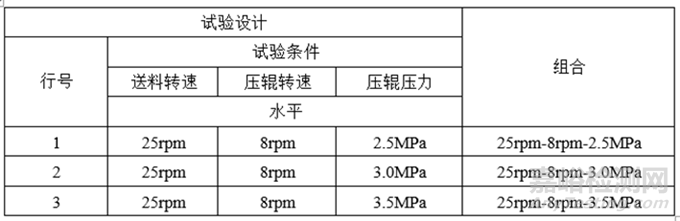
2)试验数据
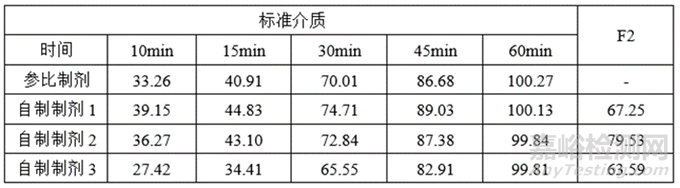
④工艺确定
具体工艺包括:
1)混合:将处方量的API与甘露醇(过60目筛)、微晶纤维素(过60目筛)、十二烷基硫酸钠、低取代羟丙基纤维素(过60目筛)混合均匀(搅拌转速50r/min,10min);
2)干法制粒:送料转速25rpm,压辊转速8rpm,压轮压力3.0MPa,预整粒50rpm、终整粒转速80rpm,20目筛网整粒。
3)总混:整粒后的物料与硬脂酸镁(过60目)1:1手动混合1min,再与低取代羟丙基纤维素(过60目)混合均匀(搅拌转速50r/min,10min);
4)压片:理论片重200mg,重量差异±4.5%,目标硬度:100 N (80 N ~120N);
5)包衣:目标增重:2.5%(2.0%~3.0%);
3、处方工艺
①处方工艺

具体工艺包括:
1)混合:将处方量的API与甘露醇(过60目筛)、微晶纤维素(过60目筛)、十二烷基硫酸钠、低取代羟丙基纤维素(过60目筛)混合均匀(搅拌转速50r/min,10min);
2)干法制粒:送料转速25rpm,压辊转速8rpm,压轮压力3.0MPa,预整粒50rpm、终整粒转速80rpm,20目筛网整粒。
3)总混:整粒后的物料与硬脂酸镁(过60目)1:1手动混合1min,再与低取代羟丙基纤维素(过60目)混合均匀(搅拌转速50r/min,10min);
4)压片:理论片重200mg,重量差异±4.5%,目标硬度:100 N (80 N ~120N);
5)包衣:目标增重:2.5%(2.0%~3.0%);
②溶出数据

4、总结
在对影响干法制粒的处方和工艺深入了解的基础上,通过对干法制粒处方和工艺的深入分析,筛选出相应的关键物料属性和关键工艺参数。先采用正交试验设计对本产品的关键物料属性进行优化和确认,形成本品的处方,在确定了本品处方的基础上,对本品关键工艺参数进行优化,形成本品的工艺,最终通过科学有效的干法制粒研发策略确定了本品的处方和工艺。
5、参考文献
1.国家食品药品监督管理总局《普通口服固体制剂溶出曲线测定与比较指导原则》(2016 年 3 月).
2.国家食品药品监督管理总局《普通口服固体制剂溶出度试验技术指导原则》(2015 年 2 月).
3.国家食品药品监督管理总局《已上市化学药品药学变更研究技术指导原则(试行)》溶出曲线研究的问答(2022 年11 月).
4. 《固体口服制剂的研发-药学理论与实践》邱怡虹、陈义生、张光中等著.

来源: 药事纵横


