您当前的位置:检测资讯 > 监管召回
嘉峪检测网 2018-07-25 20:12
近日药监局公布4家企业主动召回6种医疗器械,本次召回主要原因条形码无法正常运转、产品无屏障可能存在缺陷、“远程紧急端点按钮”线路可能安装错误、产品过期、生产过程可能被污染。具体情况如下:

DiaMed GmbH.对全自动血型分析仪IH-1000主动召回
2018年07月24日 发布
伯乐生命医学产品(上海)有限公司报告,由于发现将条形码无法读取的试剂装载到安装有软件04.07.02版本的全自动血型分析仪时,第一种试剂可以按照要求加样,但不需要加样的其他所有孔也会被全部加样,生产商DiaMed GmbH.对全自动血型分析仪IH-1000(注册证编号:国械注进20163402578)主动召回。召回级别为三级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
附件:医疗器械召回事件报告表
2018年7月23日

附件



ConvaTec lnc.对腹内压监测包主动召回
2018年07月24日 发布
康维德(中国)医疗用品有限公司报告,由于产品无菌屏障可能存在潜在的针孔缺陷,生产商ConvaTec lnc.对腹内压监测包(注册证编号:国械注进20182661529)主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
附件:医疗器械召回事件报告表
2018年7月23日

附件


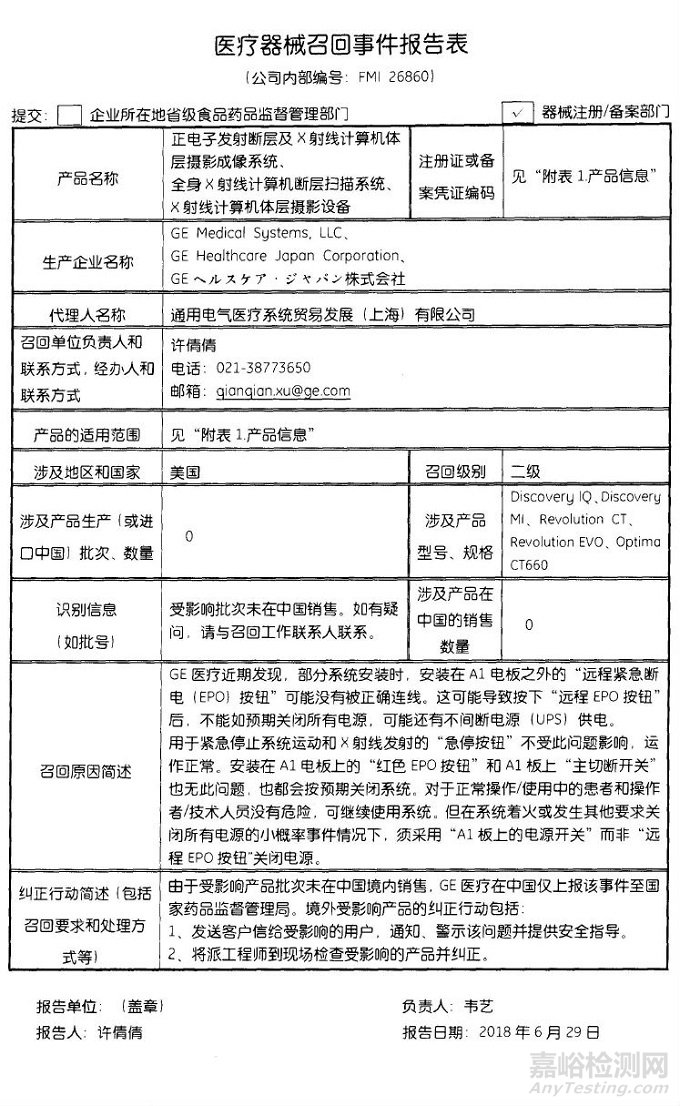
通用电气医疗系统贸易发展(上海)有限公司对正电子发射断层及X射线计算机体层摄影成像系统等主动召回
2018年07月24日 发布
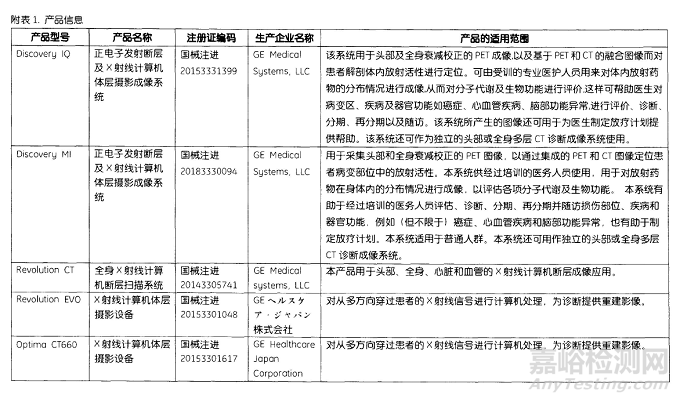
通用电气医疗系统贸易发展(上海)有限公司报告,由于安装在A1电板之外的“远程紧急断电(EPO)按钮”可能没有被正确连线,通用电气医疗系统贸易发展(上海)有限公司对正电子发射断层及X射线计算机体层摄影成像系统(国械注进20153331399、国械注进20183330094)、全身X射线计算机断层扫描系统(国械注进20143305741)和X射线计算机体层摄影设备(国械注进201533301048、国械注进20153301617)主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
附件:医疗器械召回事件报告表
2018年7月23日

附件

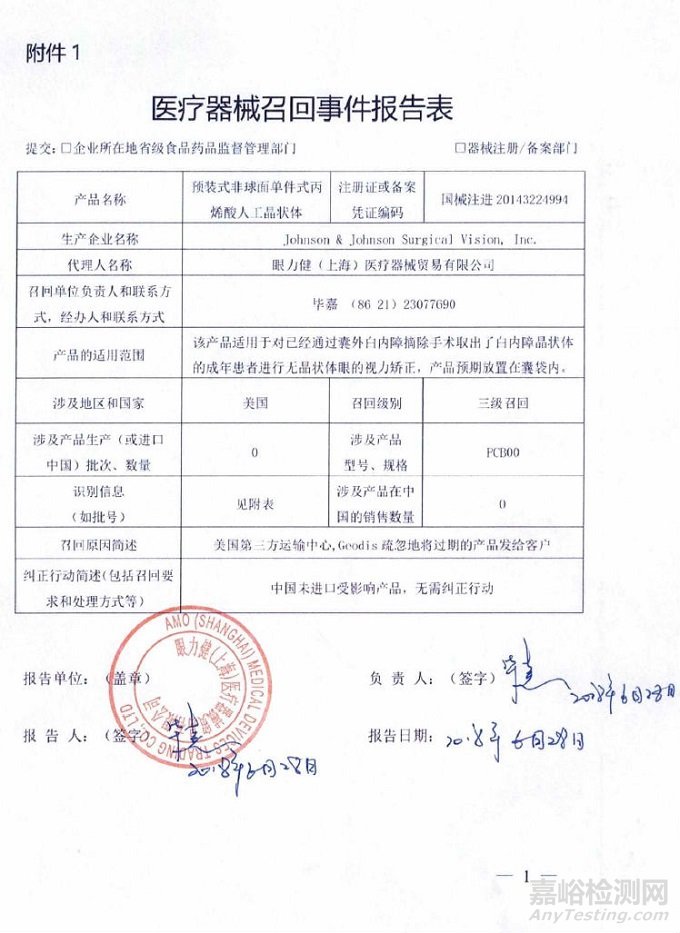
Johnson & Johnson Surgical Vision, Inc. 对预装式非球面单件式丙烯酸人工晶状体主动召回
2018年07月24日 发布
眼力健(上海)医疗器械贸易有限公司报告,由于第三方运输中心将过期的产品发给客户,生产商Johnson & Johnson Surgical Vision, Inc.对预装式非球面单件式丙烯酸人工晶状体(注册证编号:国械注进20143224994)主动召回。召回级别为三级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
附件:医疗器械召回事件报告表
2018年7月20日



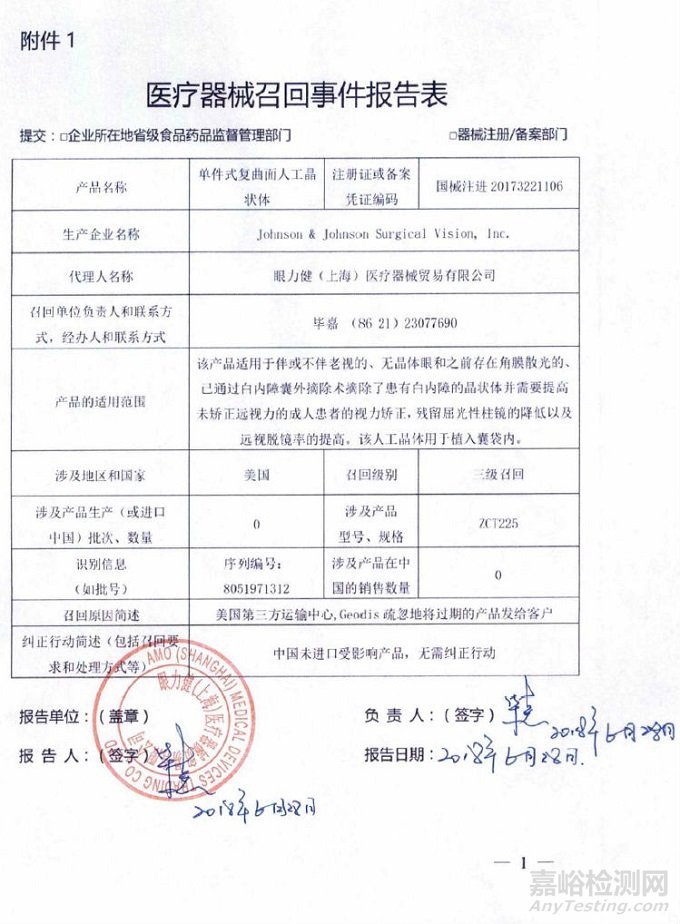
Johnson & Johnson Surgical Vision, Inc.对单件式复曲面人工晶状体主动召回
2018年07月24日 发布
眼力健(上海)医疗器械贸易有限公司报告,由于第三方运输中心将过期的产品发给客户,生产商Johnson & Johnson Surgical Vision, Inc.对单件式复曲面人工晶状体(注册证编号:国械注进20173221106)主动召回。召回级别为三级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
附件:医疗器械召回事件报告表
2018年7月20日


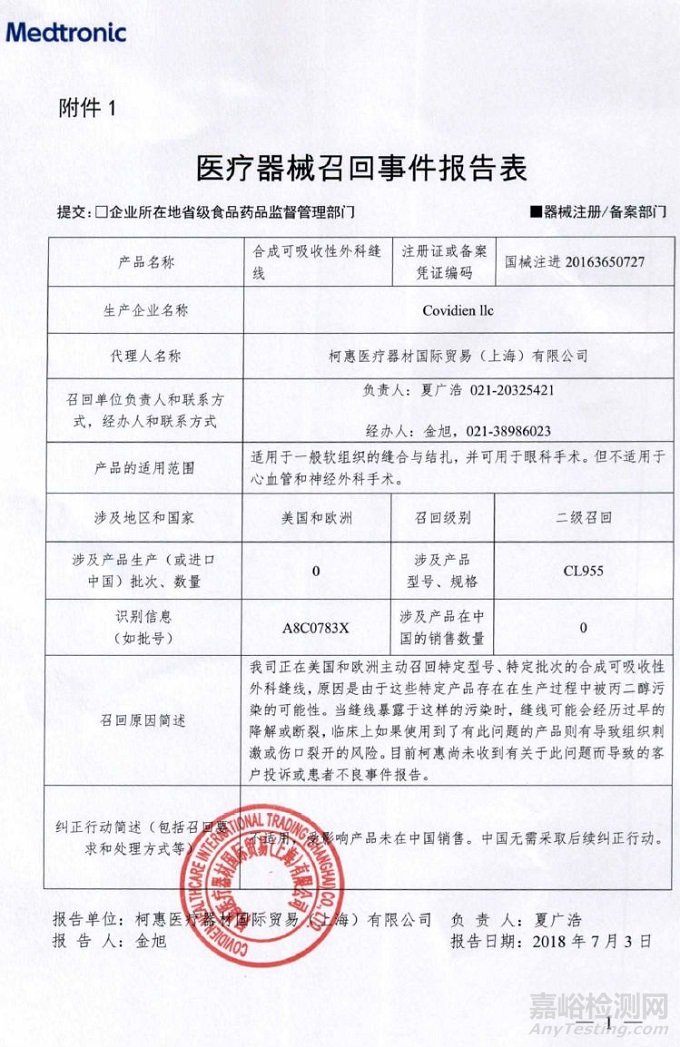
Covidien llc对合成可吸收性外科缝线主动召回
2018年07月24日 发布
柯惠医疗器材国际贸易(上海)有限公司报告,由于产品存在生产过程中被丙二醇污染的可能性,生产商Covidien llc对合成可吸收性外科缝线(注册证编号:国械注进20163650727)主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
附件:医疗器械召回事件报告表
2018年7月20日


来源:国家药监局


