您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2019-05-07 16:52
一各国药典温度的对比
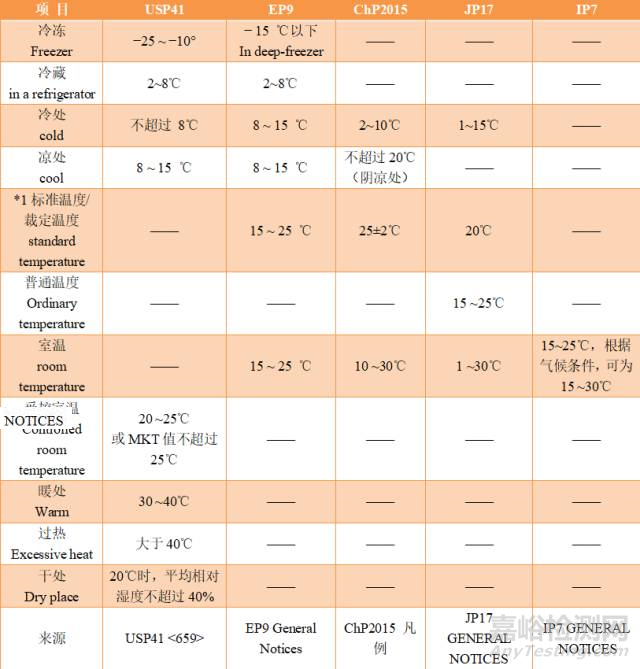
*1)标准温度、裁定温度是指,当出现结果不一致时,应在裁定温度下进行试验来判定最终结果。
二通用药典分析方法试验温度规定
很多理化的分析项目,例如pH测定,旋光度测定法,相对密度测定,溶解性测定法,受温度影响较大,故各国药典在通用分析方法章节,,规定了具体的实验温度,以下对相应分析方法的实验温度进行了归类总结。
1、pH值测定法
|
药 典 |
来 源 |
规 定 |
|
USP41 |
<791>pH |
除非专论另有规定, pH应在25±2℃范围内测定。 |
|
EP9 |
2.2.3 Potentiometric Determination of pH |
除非专论另有规定,pH应在20~25℃测定。 |
|
ChP2015 |
专论未注明 |
凡例规定:试验温度未注明者,系指在室温下进行(10 ~30℃)。 |
|
JP17 |
2.54 pH Determination |
样品溶液与校正液的温度差值在2℃以内。 |
|
IP7 |
1.13 Determination of pH |
校正溶液, 指示剂 和参比电极 和样品溶液的温度差值必须在2℃以内。 |
2、旋光度测定
|
药 典 |
来 源 |
规 定 |
|
USP41 |
<781> OPTICAL ROTATION |
25℃的条件下测定 |
|
EP9 |
2.2.7 Optical rotation |
如无特殊规定,温度均应调节至20土0.5℃ |
|
ChP2015 |
0621 旋光度测定法 |
如无特殊规定,温度均应调节至20土0.5℃ |
|
JP17 |
2.49 Optical Rotation Determination |
20℃或25℃,按专论项下规定。 |
|
IP7 |
1.4 Determination of optical rotation and specific rotation |
按专论项下规定, 通常为 20-25C |
3、相对密度测定
|
药 典 |
来 源 |
规 定 |
|
USP41 |
<699> Density of solids |
除另有规定外,测量过程温度应为15~30℃,测量过程前后温度变化不得过2℃。 |
|
EP9 |
2.2.5 Relative Density |
指在相同的温度、压力条件下,一定体积供试品重量与相同体积水的重量之比。除另有规定外,温度为20℃。 |
|
ChP2015 |
0601 相对密度测定法 |
除另有规定外,温度应为20度。 |
|
JP17 |
2.56 Determination of Specific Gravity and Density |
按专论项下规定。 |
|
IP7 |
1.3 Determination of mass density, relative density and weight per millilitre |
温度为20℃测定。 |
4、溶解性测定法
|
药 典 |
来 源 |
规 定 |
|
USP41 |
Reference Tables: Description and Relative Solubility |
没有规定 |
|
EP9 |
5.11Characters sectionin monograph |
在25℃±0.5℃下测定 |
|
ChP2015 |
凡例 项目与要求 |
于25℃±2℃下测定 |
|
JP17 |
General Notice 30 |
在20℃±5℃下测定 |
|
IP7 |
General Notices: Solubility |
除非另有规定,于20℃下测定 |
三平均动力学温度MKT
1、定义及公式
平均动力学温度(mean kinetic temperature):单一的推导温度。如果在相同特定的时期将原料药或制剂维持在该温度下,和同时经历较高和较低的情况相比,该推导温度可以对原料药或制剂提供相同的热挑战。
在为一个特定的时期估计平均动力学温度时,MKT 的计算根据下式(Arrhenius方程):
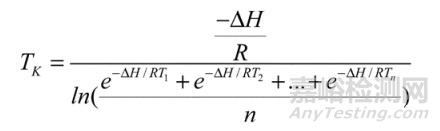
Tk为MKT值;
H为激活热量,83.144 kJ·mole-1;
R为普遍气体常量8.3144 × 10-3 KJ/mole/K
T1为第一时间段的最高温度与最低温度平均值,单位为K,K与℃之间的换算关系为273.1+℃;
T2为第二时间段的最高温度与最低温度平均值,单位为K;
Tn为第n时间段的最高温度与最低温度平均值,单位为K;
n为时间段的数目,例如n周或n月;
е 为自然对数的底数,为无限不循环小数,约为2.71828。
2、USP受控温度(controlled room temperature)关于MKT的规定
工作环境温度保持恒定并控制在20~25℃范围内,但以下情况也认为符合规定。
如果平均动力学温度(MKT)不超过25℃,药房,医院,仓库或运输过程温度在15~30℃间偏移也是可以允许的。短期的温度升至40℃但时间不超过24小时是允许的。如果生产商经过确认,温度超过40℃,也可以接受。
3、USP41<1079>储存及分发的MKT
药品的放置是药品的储存及分发规程的一部分,药品的分发及供应链也许会出现温度超标签规定的贮存要求,该规定的贮存要求是根据稳定性研究得到的。药品不是存放于仓库条件下,就是处于运输模式,存放温度均有可能超出可接受的温度范围。每次存放温度的偏移均需要评估确定对最终产品的影响。评估的方式必须科学合理并有书面的完整的技术证明来阐明药物不受影响。其中一种药品储存超过相应标签的存储条件的分析方法是MKT值的计算。
由于MKT值是药品的累积的热应力,因此它被认为是一种考虑到交通运输过程的可接受的存储方式,必须通过确定产品的稳定性极限,在遇到的温度范围内遵循一阶动力学来证明MKT值的计算是合理的。 ICH稳定性测试指南将MKT定义为一个“单一”的推断温度(derived temperature),是指药品在一个固定的周期内温度保持不变受到的热量挑战与一定周期内,温度出现高低起伏受到的热量挑战相同。
MKT用于评估短时间的温度偏移对产品质量潜在的影响是非常有用的。然而,了解任何一次短时间偏移温度的上限和下限也是非常必要的。如果这些极端温度是超出可用的稳定性数据,除了MKT值计算,其他的都不好来证明样品质量不受偏移温度影响。虽然在计算过程中温度较高,但对非冷冻产品的MKT的计算可能不会产生一个可接受的温度,尽管该产品可能不会被掺假。在较高的温度下,降解的动力学可能发生变化,或者可能发生新的降解反应;在较低的温度(接近冰点),可能发生相变,会对某些药物产品的质量产生负面影响(例如,某些蛋白质和疫苗)。具体例子的计算,详见USP<1160>章节。

来源:AnyTesting


