您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-01-09 11:51
所谓“药妆品”,翻译自英文单词“cosmeceutical”,由化妆品(cosmetic)和药品(pharmaceutical)组合而成。现在普遍认为,“药妆品”概念由美国化妆品化学家协会创始人之一Raymond Reed于1961年提出。1984年,Albert Kligman在该协会的全国科学会议上对“药妆品”概念进行了进一步的详细介绍。2005年,Albert Kligman发表文章认为,“药妆品”可被看作功能性化妆品或活性化妆品。近年来,由于商业营销等原因,此概念在化妆品行业较受追捧,加之国内外产品分类差异、混售化妆品和药品的“药妆店”渠道等客观因素的误导,使得部分消费者也开始热衷于关注所谓“药妆品”这一产品类别,并将其理解为具有药物作用或可用于疾病状态皮肤的化妆品。
事实上,虽然“药妆品”概念诞生已久,但由于这种命名方式具有一定的迷惑性和误导性,不利于消费者做出正确的健康选择,始终未被监管部门普遍接受。通过近年来对全球化妆品法规的追踪对比,认为普遍不存在“药妆品”的法规概念。与此相反,尽量避免化妆品和药品概念的混淆,是一直以来的监管趋势,也是监管部门的普遍共识。
一、化妆品的定义和相关产品分类
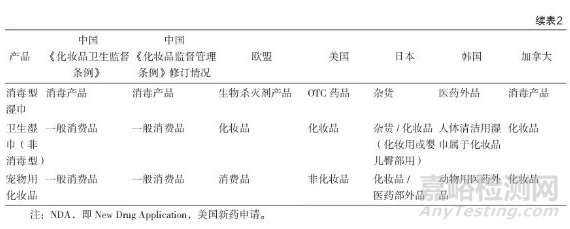
“药妆品”概念兴起的重要原因之一,就是不同国家或地区产品分类的差异,部分产品类型容易产生错误理解。为方便监管和控制风险,监管部门在法规中对化妆品、药品及相关产品进行明确定义和分类,部分国家或地区还会对化妆品进一步分类管理。化妆品定义的对比见表1;根据相关研究以及近年来化妆品法规追踪结果,部分边缘产品的分类对比见表2。
1.中国
在我国,化妆品和药品之间的界线较为明确。根据我国现行《化妆品卫生监督条例》第十二条、第十四条规定,化妆品标签、小包装或者说明书上不得注有适应症,不得宣传疗效,不得使用医疗术语,化妆品的广告宣传不得宣传医疗作用。目前,我国化妆品分为特殊用途化妆品和非特殊用途化妆品。根据《化妆品监督管理条例》修订情况,将来依然会根据风险高低实行化妆品分类管理,其中特殊化妆品的范围缩小,预计将保留染发、烫发、祛斑美白、防晒、防脱发产品,同时在特殊化妆品中增加“宣称新功效”化妆品。
2.欧盟
在欧盟《化妆品法规1223/2009》中,除做出化妆品定义外,前言第6条还指出,化妆品与药品、医疗器械、生物杀剂之间存在明确界线,主要通过施用部位和使用目的等进行区别;第2章第2条规定,注射、口服、吸入或植入的产品不属于化妆品。在欧盟的监管体系中,化妆品不再划分亚类,化妆品与药品界线明确,不存在介于化妆品与药品之间的过渡类别,也不存在“药妆品”的定义和类别。
3.美国
美国《联邦食品、药品和化妆品法》颁布于1938年,由于当时化妆品行业整体发展水平较低,法规中化妆品的定义相对较为简单和保守,部分在我国作为化妆品管理的产品,如防晒、去屑、祛痘等产品,在美国作为OTC药物管理。在美国食品药品管理局官方网站上,设有“拒绝进口产品报告”(Import Refusal Report)一栏,其中拒绝进口化妆品常见原因之一为“该产品为新型药品,未进行新药申请”,这正是由于化妆品范畴和产品分类的差异所导致的。
在美国,允许同时符合化妆品和药品定义的产品存在,例如防晒日霜、去屑洗发水等,但应同时符合化妆品和药品的相关规定。需要注意的是,这种产品并不等于“药妆品”,美国食品药品管理局在其官方网站上明确表示不承认“药妆品”概念。
4.日本
与我国、欧盟、美国等情况不同,日本除化妆品与药品外,还有一类医药部外品。根据日本《医药品、医疗器械等品质、功效及安全性保证等有关法律》(简称《药机法》,原《药事法》)规定,医药部外品共有三类:第一类主要包括除臭、防痱、防脱、脱毛等产品;第二类主要包括驱虫产品等;第三类为具有特定作用、由日本厚生劳动省指定的产品,共计27项,包括染发、烫发产品,此外,第25项为“除满足化妆品的定义,同时用于防止痤疮、皮肤粗糙、接触性皮炎、冻疮等,或用于皮肤、口腔消毒杀菌等目的的产品”,这类产品通常被认为是日本的“药用化妆品”。事实上,日本法规中没有“药用化妆品”的官方定义,只是作为一类产品的俗称被广泛使用和接受,以至于后期直接引用于法规中,如《药用化妆品功效成分清单》。
日本的所谓“药用化妆品”应在上市前通过医药部外品许可审批,审批的重点在于功效、安全和质量规格。其功效成分通过以下两种形式的列表严格管理,列表以外的功效成分需随产品进行严格的新原料审批:一是日本厚生劳动省于2008年发布的《药用化妆品功效成分清单》;二是“别纸规格”,为保护知识产权,企业单独获批的功效成分可选择不对外公开,由厚生劳动省掌握。通过许可审批的产品可在包装上标注“药用”“医药部外品”等字样,由于部分产品包装与普通的化妆品较为相似,因此,消费者常误认为日本存在所谓“药妆品”。但实际上,日本所谓“药用化妆品”在本质上是一种医药部外品,并非公众所理解的具有药物作用的化妆品。
5.韩国
与日本相似,韩国除化妆品、医药品外,存在一类医药外品,但其定义和范围与日本的医药部外品存在差异,其中不存在“药用化妆品”一类产品。2017年之前,染发、脱毛、防脱等产品在韩国均属于医药外品,现已调整为化妆品。目前,仅有少部分韩国医药外品在我国作为化妆品管理,如抑汗除臭类产品。此外,根据韩国《化妆品法》,韩国化妆品进一步分为一般化妆品和机能性化妆品。机能性化妆品原本主要包括美白、抗皱、防晒、助晒产品,在2017年之后,增加染发、脱毛、防脱、缓解粉刺、缓解特应性皮炎干燥、缓解萎缩纹等产品。
6.加拿大
加拿大化妆品和药品之间界线明确,较为特别的是,在加拿大存在一类“介于化妆品和药品之间的产品”(Products at the Cosmetic-Drug Interface,PCDI)概念,主要包括药品、天然健康产品、化妆品等。这类产品并非“药妆品”,企业应根据相关指南,进一步明确产品的具体类别,从而对应所适用的监管法规。
二、监管手段和相关启示
根据上述化妆品及相关产品的定义和分类,部分“边缘产品”在不同的国家或地区可能被划入不同的产品类别。随着国际贸易全球化的日益发展以及产业科技的不断进步,化妆品与药品或其他健康产品的区分已成为全球监管部门普遍面临的监管问题。为应对产品分类问题以及衍生出的“药妆品”等违规宣称问题,监管部门可采取必要的监管手段,引导行业正面发展。近年来,化妆品法规追踪研究结果显示,总体监管趋势是进一步明确化妆品和药品界限,减少化妆品的医疗色彩,其中部分监管手段值得我国参考借鉴。
1.明确违规概念
明确“药妆品”等属于违规概念,进行官方公告或解读,可以直接有效地引导企业公众避免错误认识。例如,在美国食品药品监督管理局官方网站上,专门就“药妆品”问题进行声明:《食品、药品和化妆品法》不承认这类产品,“药妆品”这一概念在法律上不具有任何意义[11]。2019年6月27日,我国台湾地区发布“卫授食字第1081605206号”,规定在进口化妆品的外包装或容器上,如有“药用”“药”“医药”“Medicate”或等同意义的字样,应注明“本产品属化妆品,不具医疗效能”。
2010年11月,原国家食品药品监督管理局曾发布《关于加强化妆品标识和宣称日常监管工作的通知》(食药监办许[2010]135号),要求各地对标识和宣称“药妆”“医学护肤品”等夸大宣传、使用医疗术语的违规行为加强监管。2019年1月,国家药品监督管理局发布“化妆品监督管理常见问题解答(一)”,再次明确“对于以化妆品名义注册或备案的产品,宣称‘药妆’‘医学护肤品’等‘药妆品’概念的,属于违法行为”。该项政策解读发布后,立即引发行业广泛热议,有效遏制了近期炒作“药妆品”等违规概念的不良风气。
2.发布分类指南
化妆品的定义和分类虽已在监管法规中进行规定,但在实际操作中,部分产品的分类问题仍然可能存在,可通过指南或产品举例等方式进一步予以明确。例如,为帮助区分化妆品和药品,欧盟发布有专门的官方指南,并在此基础上,于2013年发布产品分类指导手册,在判断产品类别时,应根据上述指南和手册,针对具体实际情况逐案进行分析。加拿大卫生部在官方网站上对部分产品进行了分类举例,其中明确防晒产品(包括带有SPF值的彩妆品)、痤疮皮肤护理产品、美白产品等不属于化妆品。此外,为指导企业更好地对PCDI产品进行分类,加拿大卫生部还发布了相关指南。
随着行业的不断创新发展,宣称新功效、使用新原料、选用新型包装展示形式的产品将不断涌现,都将可能加剧产品分类问题的出现,亟待相关规范或指南的出台。2018年1月,原国家食品药品监督管理总局公开对《化妆品分类规范》征求意见。《化妆品分类规范》基本涵盖了市场流通的化妆品产品类型,对于企业判断产品类别和自我对照约束具有积极的指导意义。建议我国监管部门对该规范进一步研究细化并适时发布,同时设置增补修订机制,在规范和矫正企业行为的同时,保留创新空间,保护企业研发创新的积极性。
3.调整产品分类
在一些国家或地区,化妆品和药品之间存在过渡性质的产品类别(如日本、韩国的医药部外品、医药外品),其中部分产品易与化妆品混淆,不利于政府监管。在韩国的医药外品中,原本包括染发、脱毛、防脱产品;2017年1月,韩国发布《化妆品法施行规则》修订案,将上述产品调整为机能性化妆品,不再作为医药外品管理。这种产品分类的调整,降低了相关产品的医疗色彩,避免给消费者带来误导。
此外,随着科学认识的发展和监管条件的成熟,部分产品类别也需要适时进行调整。例如,止汗剂原本在加拿大作为药物管理,2009年,加拿大卫生部发布了一项关于止汗剂的产品分类评估。根据该评估结果,在符合相关要求、且用于减少一般腋下出汗时,铝基的止汗剂产品可作为化妆品管理,用于多汗症、具有更为持久效果的止汗产品,仍作为药品管理。根据监管环境的变化,应及时对产品分类进行适当调整,在方便监管的同时,也能避免因分类问题产生不必要的误导。
根据我国《化妆品监督管理条例》修订情况,部分实际上不适宜作为化妆品管理的产品,如美乳、健美产品等,预计将从化妆品范围中删除。事实上,根据表2产品分类对比结果,这两类产品在其他国家或地区大多作为药品管理,《化妆品监督管理条例》中的相应调整将有助于明确化妆品“非医疗作用”的定位。
4.修改不当类别名
在我国台湾地区化妆品中,曾有一类“含有医疗或毒剧药品的化妆品”,常被简称为“含药化妆品”,主要包括防晒、染发、烫发、止汗除臭、美白、去屑等功效化妆品。由于这种命名方式容易产生歧义,2018年12月我国台湾地区发布《特定用途化妆品成分名称及使用限制表》草案,取代了原《化妆品含有医疗或毒剧药品基准》,将“含药化妆品”更名为“特定用途化妆品”。
出于监管需要,部分国家或地区将化妆品进一步分类,对宣称一定功效、高风险产品进行特殊分类管理,在对该类产品命名时,应特别注意,避免类别名称的误导。我国目前称为“特殊用途化妆品”,实际在做出此种分类时,并非重点考虑产品的宣称和用途,而是由于宣称有一定功能的产品,往往具有相对较高的风险,因此需进行特殊监管。根据《化妆品监督管理条例》修订情况,预计将改名为“特殊化妆品”,进一步突出依据风险高低进行分类和管理,弱化宣称和用途的概念。
三、总结和展望
通过对比不同国家或地区化妆品的定义和相关产品分类,结合近年来监管趋势,监管部门普遍认为化妆品不应具有医疗作用,与药品之间的界线较为明确。即使是医药部外品等几种容易引起误解的产品类型,与所谓“药妆品”也有本质区别。“药妆品”概念大多不符合相关法规要求,视作违法违规宣传。
在我国监管体系下,所谓“药妆品”并不会增加产品安全和功效方面的保证,相反将产生消费误导、增加监管难度、有违公平竞争。为了保护消费者切身利益,营造良好的产业和竞争环境,建议我国监管部门继续保持对相关违法违规行为的打击力度,特别是加强上市后的监督检查;同时,进一步加强培训宣贯、科普宣传相关工作,引导公众客观认识相关产品,扭转错误认知。
作为化妆品企业,应严格遵守相关法规要求,规范产品宣称,通过合规、正当、合理的方式进行创新和竞争。在进出口贸易中,应尤其注意产品在不同国家或地区的分类问题。对于在生产国或地区被归为医药部外品、医药外品或药品的产品,如作为化妆品向我国进口,应首先考虑是否符合我国化妆品的定义和相关规定,并严格按照化妆品相关监管要求进行进口和销售,不得借机宣传“药妆品”等概念;对于出口产品,也应当充分理解和尊重对方的各项监管规定,例如防晒产品在向美国或加拿大出口时,应符合相关药品监管法规,并作为药品接受监管,否则也将影响产品的合规贸易。
此外,在打击违法违规宣称的同时还应意识到,公众近年来对“药妆品”概念的关注,实际上体现了对于功效型化妆品需求的日益增长。在消费者的迫切需求下,监管部门应当鼓励和引导企业进行科学合理的功效宣称和验证。根据目前《化妆品监督管理条例》修订情况,未来我国将加强对于化妆品功效宣称的管理。2018年1月,中国食品药品检定研究院官网发布《化妆品功效宣称评价指导原则》(征求意见稿),公开向社会征求意见。
一方面,我国在化妆品功效管理领域的发展可期,但另一方面,由于我国化妆品行业起步较晚,虽然近年来高速增长,但目前仍与行业发达国家或地区存在较大差距,特别是在功效验证的基础研究、方法应用、监督管理等方面较为薄弱。为顺应行业和科技的发展,做足技术储备,建议我国监管和技术支撑部门应进一步加强国际间合作与交流,研究借鉴该领域先进的科研和管理经验,对化妆品功效验证方法进行统一细致的梳理、研究、论证和验证,并加快标准方法的研究制定。同时,积极引导企业进行科学客观、公平有效的宣称和验证,积极引导企业加强研发投入与科技投入,在突出企业主体责任的同时,充分保护企业的自主创新和消费者的消费权益。以《化妆品监督管理条例》修订和相关各项配套法规政策为契机,促进我国化妆品行业市场的长期良性健康发展。



来源:Internet


