您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-04-16 17:59
近日,国家药品监督管理局发布消息,批准了Cook Ireland Limited生产的优先产品“药物洗脱外周血管支架”注册。这是我国首个批准的外周药物洗脱支架。该产品由预装支架和输送系统组成,含有注射器配件。适用于治疗参照血管直径为4-9mm的膝上股腘动脉的症状性病变。据悉,该产品可支撑病变残留狭窄,减少球囊扩张后的弹性回缩发生;紫杉醇涂层可抑制血管平滑肌细胞增殖,预期降低再狭窄发生。这能够优化目前现有外周血管疾病治疗方案,更好地满足临床需求。
今日器审中心发布了该产品的注册技术审评报告,我们一起来了解一下临床前做了哪些研发实验。
一、产品结构及组成
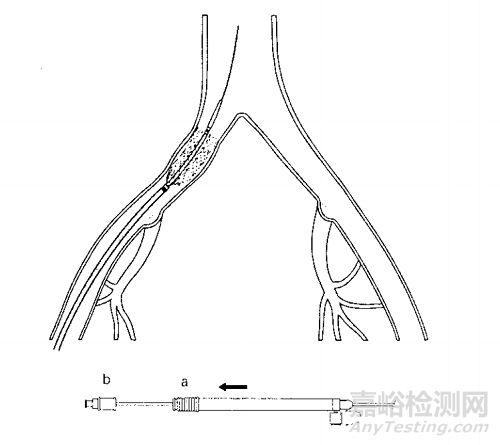
该产品由预装支架和输送系统组成,含有注射器配件。支架由镍钛合金经激光雕刻工艺制成,表面涂覆紫杉醇药物涂层,药物剂量密度3μg/mm2,支架每个末端具有4个不透射线黄金标记。产品环氧乙烷灭菌,一次性使用。
二、产品适用范围
该产品适用于治疗参照血管直径为4-9mm的膝上股腘动脉的症状性病变。为避免累及股总动脉,支架的近端应置于股浅动脉起始部位以下至少1cm处;为避免累及膝下动脉,支架的远端需置于股骨上髁水平以上位置。
三、作用机理
药物洗脱外周血管支架是一种由镍钛合金制成的自膨式支架,表面涂覆紫杉醇药物涂层。支架由激光雕刻制成,设计用于在血管内展开后,支架对血管内腔将产生一种向外的径向力,从而在支架植入区域保持血管通畅;紫杉醇预期降低再狭窄发生率。
四、临床前研究
(一)产品性能研究
1. 产品技术要求研究
输送系统:
1、尖端构型
2、外观
3、耐腐蚀性
4、断裂力 /结合强度
5、无泄漏
6、输送系统的尺寸
7、轮廓 /直径测试
8、可视性
9、水合性
10、接头
11、通过性能
12、模拟使用/追踪性
13、支架释放力
14、柔顺性(弯曲/打折)
15、推送性
16、侧路灌洗口配合使用性能
17、还原物质
18、重金属
19、酸碱度
20、蒸发残渣
21、紫外吸光度
支架:
22、外观
23、径向力
24、疲劳耐久性能
25、可视性
26、支架的尺寸
27、支架自由表面积
28、弯曲 /打折
29、显微结构
30、支架长度变化率
31、涂层微粒试验
32、镍钛合金相变温度
33、支架化学成分
34、耐腐蚀性
35、紫杉醇药物涂层的要求
36、溶剂残留量
37、涂层完整性
注射器:
38、外观
39、注射器的标尺
40、标尺的刻度容量线
41、标尺上的计量数字
42、标尺的印刷
43、外套
44、按手间距
45、活塞
46、锥头
47、滑动性能
48、器身密合性
49、容量允差
50、残留容量
51、可萃取金属含量
52、酸碱度
53、易氧化物
支架系统:
54、无菌
55、热原
56、环氧乙烷残留量
2. 产品性能评价
产品性能评价包括支架平台轴向、弯曲、扭转和搏动疲劳性能 ,重叠支架疲劳性能、涂层牢固度 、有限元分析、紫杉醇涂层鉴别和总含量、紫杉醇涂层体外释放、紫杉醇内外释放相关性、MRI兼容性等研究报告。
(二)生物相容性
该产品由支架、输送系统和注射器组成,其中支架为植入器械,与循环血液长期接触;输送系统为外部接入器械,与循环血液短期接触;注射器不直接接触患者。申请人依据GB/T16886 系列标准对支架和输送系统进行了生物相容性评价;同时依据GB 15810-2001 对注射器进行了生物相容性评价。结果表明产品的生物相容性风险可接受。具体评价项目详见表3。
表3 生物相容性评价项目表
|
评价项目 |
支架 |
输送系统 |
注射器 |
|
细胞毒性 |
√ |
√ |
/ |
|
致敏试验 |
√ |
√ |
/ |
|
刺激性/皮内反应 |
√ |
√ |
/ |
|
急性全身毒性 |
√ |
√ |
√ |
|
亚慢性毒性 |
√ |
/ |
/ |
|
遗传毒性 |
√ |
/ |
/ |
|
植入 |
√ |
/ |
/ |
|
溶血 |
√ |
√ |
√ |
|
血栓形成 |
√ |
√ |
/ |
|
凝血 |
/ |
√ |
/ |
来源:嘉峪检测网


