您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2021-11-20 03:22
国家药品监督管理局发布的无源植入性医疗器械货架有效期注册申报资料指导原则 (2021年修订版)(征求意见稿)中指出无源非植入性医疗器械有关货架有效期注册申报可根据实际情况参照执行,为无源非植入性医疗器械货架有效期验证提供了指南。
指导原则第3部分货架有效期验证内容中提到,包装系统性能检测包括包装完整性、包装强度和微生物屏障性能等检测项目,其中,包装完整性检测项目包括染色液穿透法测定透气包装的密封泄漏试验、目力检测和气泡法测定软性包装泄漏试验等,包装强度测试项目包括软性屏障材料密封强度试验,无约束包装抗内压破坏试验等。此外,指导原则中也有提及包装的稳定性和微生物屏障性能。企业在做无菌医疗器械包装验证时,可以根据需要参考选择上述检测项目,检测标准可参考表 1。
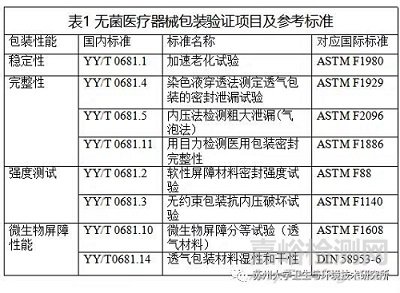
本文讨论的是无菌医疗器械包装验证中的主要物理性能的检测要点。此外,运输试验是对产品单个运输包装的检测,本次不讨论。除运输试验外,无菌医疗器械包装验证试验用到的包装中可以添加医疗器械产品,也可以不添加。
主要物理性能检测的要点
加速老化试验
实际老化程序为确保无菌屏障系统包装材料和包装完整性不随时间而降解提供了最佳数据,是产品研发阶段必须进行的研究,但由于产品更新换代较快,加速老化试验为实现缩短研发时间,加快注册资料提交,使新产品在短期内投放市场提供了可能。为确保加速老化试验真实反映实际老化的结果,实际老化的研究必须与加速老化同步进行,实际老化的时间必须进行至产品标称的货架寿命。如果加速老化数据没有问题,但是实际老化数据有问题,则需要申请注册变更。
加速老化试验是在加温加条件下进行的,对于湿度敏感的材料要进行湿度控制。这些条件对包装本身具有一定的挑战,会在加速老化后发生材料断裂、封口张开等情况,此时需要与实时老化的数据进行比较,再确定产品的有效期限。
密封强度试验
密封强度试验不仅用于评价剥离性和包装完整性,还能用于测量包装过程中形成稳定密封的能力。
包装密封强度测试的第1步,确定对包装 4 个边中的哪个边进行测试。虽然标准中未规定选择的方法,但通常应选择企业自封的边进行测试,如果包装形式是组合袋或顶头袋的卷材,可以只验证自封的 1 个边,其他 3 个卷材预封边可以在进货检验时进行测试;如果包装形式是吸塑盒,则 4 个边均应进行测试。
包装密封强度测试的第 2 步,裁样,即将包装封口裁切成宽度为 15 mm 或 25 mm 的长方形样品,优先采用15 mm试验宽度。裁切位置应该在测试边上随机选取,尽量覆盖密封边的各个部位。
包装密封强度测试的第3步,用拉伸试验机测试包装的封口强度。标准 YY/T 0681.2 软性屏障材料的密封强度检测是开放型的标准,只规定了检测的方法,并未给出判定的标准,需要企业自己验证适合自己产品的判定标准。
密封强度的值过小或过大均不宜,过小,容易在使用前发生包装封口张开,破坏无菌屏障;过大,容易造成开启时材料掉屑,污染包装内的产品。
无约束包装抗内压破坏试验
无约束包装抗内压破坏检测为评价包装是否因受到压差作用而导致破坏提供了快捷的评价方法,包含胀破、蠕变和蠕变至胀破3个试验。 需要经过航空运输的医疗器械产品,均需要做无约束包装抗内压破坏的测试,真空包装可以免除此项。对带有透气材料的包装进行无约束包装抗内压破坏测试时,应在试验前先将透气材料一面进行屏障封堵,封堵的方法包含标签或胶带粘贴和在透气材料上涂抹非固体封堵剂。一般实验室会选择用胶带粘贴透气材料的方式,粘贴时应注意包装的边缘不能有胶带折叠覆盖,否则会影响密封的破裂。
染色液穿透法测定透气包装的密封泄露试验
染色液穿透法是测试包装封口是否严密的最直观的方法,即利用染色液的穿透性检验包装封口是否有漏点。顶头袋两种材料拼接的部位和信封式密封包装的中间接缝处容易发生密封泄漏。
内压法检测粗大泄露(气泡法)试验
内压法检测粗大泄漏是将测试的包装浸在水下约2.5 cm,向包装内充气,当达到已知 250 μm 缺陷处开始有气泡排出的压力时,保持一定的时间,检测包装上是否存在破损的方法。当检测透气包装材料时,一般在包装材料表面施加阻隔剂,包装浸没在水下至少5s之后开始施加空气。本试验方法适用于非常大或长的包装材料,此类包装材料不适合采用其他任何测试包装完整性的试验仪器。
目力检测试验
目力检测是检验员的目力从距离产品30~45 cm 处进行密封检验,检验内容包括包装的整个密封区域的完整性和一致性。密封区域可能出现的缺陷:(1)窄封区容易在产品储存和运输过程中发生破损,影响包装内产品的无菌状态;(2)过封区容易影响包装的打开,导致使用不便。
总之,无菌医疗器械包装是保障无菌医疗器械产品安全有效的重要组成部分。包装材料的选择和包装形式的确定需要在研发阶段根据产品的特性、生物相容性及灭菌方式等进行确认。对选定后包装的验证内容除了上述主要物理性能外,根据实际需要还可进行软包装材料上印刷墨迹和涂层化学阻抗评价,涂胶层重量、软性屏障膜抗揉搓性能、软性屏障和复合膜抗慢速戳穿性能等检测,以及包装的运输试验和微生物屏障性能评价,以保证包装可以为无菌医疗器械提供良好的无菌屏障至产品使用前的最后一刻。

来源:苏州大学卫生与环境技术


