您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2021-12-06 22:58
摘要
随着社会的变革、经济的发展、新一轮科技产业革命的兴起、全球市场一体化进程的提速,医疗器械产业的生产方式以及营销模式正在悄然改变,导致医疗器械产业链的延伸以及日趋复杂的态势。医疗器械产品安全涉及人民群众的健康权益,是重大的民生问题,使得公众对医疗器械的安全有效也提出了新的需求。
质量管理体系(Quality Management System,QMS)是指在质量方面指挥和控制组织的管理体系。质量管理体系是组织内部建立的、为实现质量目标所必需的、系统的质量管理模式。它将资源与过程结合,以过程管理方法进行的系统管理,根据企业特点选用若干体系要素加以组合,它可以有效的进行质量改进,提高产品质量水平。因此,为了进一步确保产品质量,我们有必要在公司内部确切的落实质量管理体系。
同时,法规对于运行质量管理体系也提出了明确要求:
《医疗器械监督管理条例 739号》第八十六条(二)中明确规定:未按照经注册或者备案的产品技术要求组织生产,或者未依照本条例规定建立质量管理体系并保持有效运行,影响产品安全、有效的由负责药品监督管理的部门责令改正,没收违法生产经营使用的医疗器械;情节严重的,责令停产停业。
本文就关于医疗器械行业的质量管理体系运行的一些知识要点进行分享。
一、相关术语、概念
1.质量:一组固有特性满足要求的程度。
固有特性:必须履行的、明示的、或隐含的需求或期望。
产品质量就是产品的实用性,即产品在使用时能成功地满足用户需求的程度。—朱兰(美国著名质量管理专家)

3.管理:通过计划、组织、激励、领导、控制等手段,结合人力、物力、财力、信息等资源,以期高效的达到组织目标的过程。
管理是计划、组织、领导、控制的总和。

4.体系:若干有关事物或某些意识相互联系的系统而构成的一个有特定功能的有机整体:如工业体系、思想体系、作战体系等。
管理体系:建立方针和目标并实现这些目标的体系。
质量管理体系QMS:在质量方面指挥和控制组织的管理体系。
二、相关标准
1. ISO(International Organization for Standardization):非政府性的国际标准化组织。
2. ISO13485:2016。1996年ISO发布了ISO13485:1996《质量体系—医疗器械—ISO9001应用的专用要求》标准,该标准不是独立标准,而是要和ISO9001:1994标准联合使用的标准。2003年ISO/TC210修订1996版ISO13485标准后,发布了ISO13485:2003《医疗器械 质量管理体系 用于法规的要求》标准,该标准是专用于医疗器械领域的独立标准。目前ISO/TC210已正式于2016年3月1日发布实施第三版的ISO13485标准,这就是ISO13485:2016。
3. YY/T0287-2017。国家食品药品监督管理总局将ISO13485:2016转化为YY/T0287-2017/ISO13485《医疗器械 质量管理体系用于法规的要求》作为国家标准发布实施。
质量管理体系的基石
1. 八项原则
1)以顾客为焦点
我们依存于顾客,体系的目的是达到顾客满意,以获得效益。
2)领导作用
质量管理是一把手工程,宗旨和方向从上往下传达和贯彻。
3)全员参与
质量是全员的事情,人人都是质量管理的主角。
4)过程方法
过程是输入转化成输出,以及其中有效配置资源,得到高效产出的活动。
5)系统管理方法
系统是管理相互关联的过程,以提高效率。
6)持续改进
充分理解和运用戴明环(PDCA),保持改进。
7)基于事实的决策方法
数据和信息的分析是提供决策的基础,靠事实说话、靠数据说话。
8)与供方互利的关系
强调与供应商的合作共赢,不能只讲控制。
质量管理体系过程模式图


»组织必须从增值的角度对过程进行策划并使其在受控条件下运行。
QMS的过程中:物流是根本,信息流是关键。
— 生产制造型企业的管理一切围绕着“三流”进行,即:物流、信息流和资金流。
— 物流必须不断增值,企业才能生存与发展。
— 信息流的作用与价值在于能确保和促进物流的增值。
— QMS中的支持过程 都必须确保产品实现过程内的物流是增值的。
资源是过程中的活动所必须的条件。
四、文件
1. 文件的价值:沟通意图、统一行动。
1)满足顾客要求及质量改进
2)提供适宜的培训
3)重复性和可追溯性
4)提供客观证据
5)评价质量管理体系的有效性和持续的适宜性
2. 文件架构
1)一级文件:质量手册、方针及目标。明确表明公司的质量管理体系运作中的总宗旨与总目标,是全公司的质量计划。
2)二级文件:程序文件。指导员工如何进行以及完成质量手册内容所表达的方针及目标的文件。
3)三级文件:规章制度、作业指导书、等指令文件。是指详细说明特定作业是如何运作的文件。部门内部各类作业指导书、工作指令、规章制度、工艺流程、验规范以及以各种形式出现的要求作业人员按其操作、指导生产、保证质量的一系列文件与资料。
4)四级文件:质量记录。用于证实产品或服务是如何依照所定要求运作的文件。通常指部门内部使用的各类报告记录以及相关部门之间的表单、单据。

3. 建立、实施、保持和改进质量管理体系的步骤:
a) 确定顾客的需求和期望。
b) 建立组织的质量方针和质量目标。
c)确定实现质量目标必需的过程和职责。
d)确定和提供实现质量目标必需的资源。
e)规定测量每个过程的有效性和效率的方法。
f)应用这些测量方法确定每个过程的有效性和效率。
g) 确定防止不合格并消除产生原因的措施。
h) 建立和应用持续改进QMS的过程。
4. 质量方针和质量目标
1)作用:质量方针和质量目标的建立—为企业提供了关注的焦点。
质量方针和质量目标确定了期望的结果,并帮助企业利用其资源得到这些结果。
2)相互关系:质量方针为建立和评审质量目标提供了框架。
质量目标需与质量方针和持续改进的承诺相一致,是可测量的。
五、过程方法
系统地识别和管理组织所应用的过程,特别是这些过程之间的相互作用,称为“过程方法”。
1. 系统地识别组织所应用的过程(策划)

2. 识别和确定过程之间的相互作用
1)各个过程之间的联结关系。
2)过程的输出与下一个/几个过程的输入的关系与影响。
3)过程之间衔接的方法与资源需求。
3. 管理过程及过程的相互作用
1)确定管理过程活动的职责、权限。
2)确定为确保过程有效运行和控制所需的准则和方法。
3)过程使用的资源。
4)过程之间的接口(通过沟通的方法)。
5)监视、测量和分析过程。
6)实施必要的措施,实现过程的持续改进。
4. 过程方法的优点
1)可以实现对过程的连续控制
2)过程方法运用PDCA(策划—实施—检查—改进)模式,获得对过程持续改进的动态循环。
3)最终使企业在产品和也许的业绩、有效性、效率和成本方面得到显著的收益。
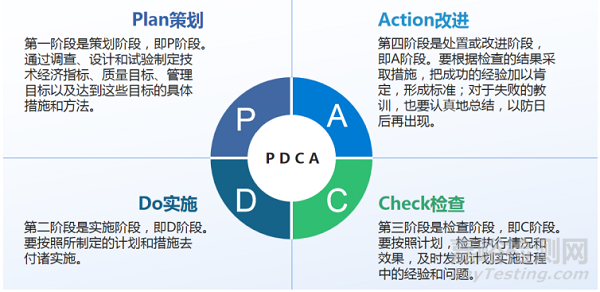
5. PDCA法
P-策划。通过调查、设计和试验制定技术经济指标、质量目标、管理目标以及达到这些目标的具体措施和方法。
D-实施。要按照所制定的计划和措施去付诸实施。
C-检查。要按照计划,检查执行情况和效果,及时发现计划实施过程中的经验和问题。
A-改进。要根据检查的结果采取措施,把成功的经验加以肯定,形成标准;对于失败的教训,也要认真地总结,以防日后再出现。
六、质量管理体系评价
1. 质量管理体系过程的评价

2. 质量管理体系的审核


3. 质量管理体系审核原则
1)客观性—审核员要以充分的证据为基础,公正、客观地评价审核对象,不能偏见、主观的给出审核结论。
2)独立性—审核员要与被审核的领域无直接责任关系,无任何利益关系,在内审中一般来说本部门人员不能审核本部门。
3)系统性—审核员要按规定的程序全面的审核和评价与审核对象有关的各项活动和结果。是有计划、有步骤、有程序正规的果冻。
4)基于证据的方法—得出的审核结论是可信的和可重现的。
参考文献
1、《医疗器械监督管理条例 》739号令
2、《YY/T 0287-2017 医疗器械 质量管理体系用于法规的要求》
3、《ISO 13485:2016 医疗器械 质量管理体系用于法规的要求》

来源:德大器械产业管家


