您当前的位置:检测资讯 > 科研开发
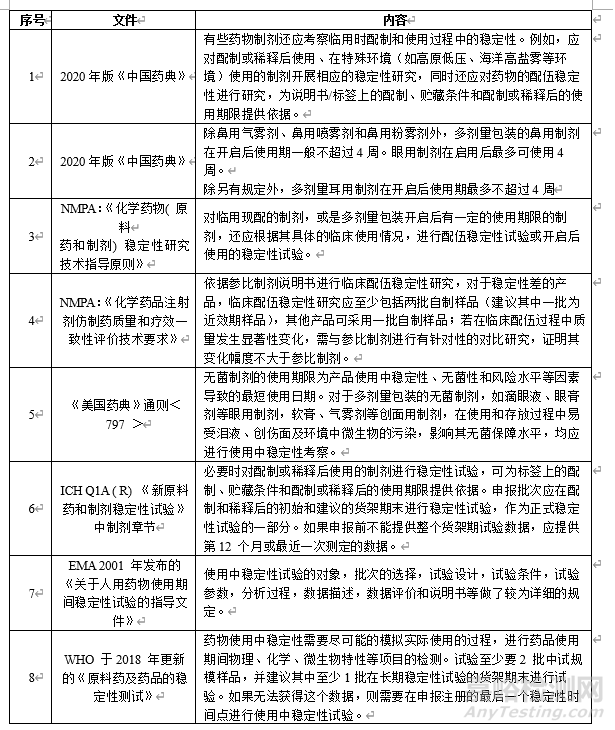
嘉峪检测网 2022-07-11 21:35
什么是使用中稳定性试验?
使用中稳定性试验( in-use stability testing)是为确定药物临床使用或患者使用期间的放置条件和开启后的使用期限、保证药物制剂在一定使用期间内的稳定而进行的试验。如果药品包装在多次使用的容器中(例如,药片在瓶中或药膏在软管中),通常需要进行使用中的稳定性试验。
哪些药物要进行使用中稳定性研究?
(1)多剂量包装的药物,在使用过程中需要重复多次打开封口使用。如滴眼剂、口服溶液剂、口服混悬剂、口服乳剂、糖浆剂、软膏剂、凝胶剂和部分口服固体制剂等。
(2)需要在临床前重新配制的药物,如注射用的冻干粉,需要用水、氯化钠注射液、葡萄糖注射液等溶媒配伍稀释后使用的注射液。
(3)另外还有一些具有功能性刻痕的口服片剂,应根据《化学仿制药口服片剂功能性刻痕设计和研究技术指导原则( 试行) 》,对片剂分割后部分进行使用过程中的稳定性研究。
(4)某些高阻隔包装的药物,如铝塑泡罩外加双铝袋包装的药物,加高阻隔双铝袋的目的通常为了防潮、避光,实际使用过程中除去了双铝袋,需要考察使用中稳定性。
使用中稳定性研究怎么做?
(1)样品批次的选择
根据国内外现有法规,一般选择至少两批稳定性研究的样品,其中至少一批为近效期的样品。并在申报资料中承诺,在样品近效期时将进行使用中稳定性试验。
(2) 试验方案的设计
做过几个药物的使用中稳定性试验方案,感觉内容真是千差万别,各具特色。即使都是注射液剂型,方案差异也很大。但总的来说,使用中稳定性的试验条件、时间点和检测指标,一定要根据药物临床使用方法和要求来设计。
(3) 检测方法的验证
一定要注意,使用中稳定性试验使用的检测方法需要进行验证。切不可因为检测方法与验证过的成品检测方法类似,就不进行方法验证了。一是为了获取科学可靠的试验数据,二是不做方法验证有可能会被审评老师发补哦。比如测定注射液与溶媒配伍后的有关物质,检测方法的检测限和定量限的验证非常关键。本着科学的原则评估和进行必要的方法验证项目。
(4)试验结果分析
一般来说,考察结果如果符合设定的限度,说明满足临床使用中的稳定性要求。如果结果不符合设定的限度,必要时进行参比制剂使用中稳定性对比研究,综合分析是否需要在说明说中明确使用稳定性规定。
案例一:某注射液一致性评价中使用中稳定性研究
参比制剂说明书内容:在输注之前必须用 5%葡萄糖注射液或 0.9%氯化钠注射液稀释至浓度为 0.2mg/mL至 2.5mg/mL的输注液。其它药物不能加入输注液中。如果未立即使用,输注液在 2-8℃ 条件下贮藏时间不应超过 24 小时,或在室温条件下(25℃)贮藏时间不超过 6 小时。
关键词划重点,两种配伍溶液5%葡萄糖注射液和 0.9%氯化钠注射液,两个配伍浓度0.2mg/mL和 2.5mg/mL,两种放置条件和考察时间:2-8℃放置考察24 小时,25℃放置考察6小时。所以设定的试验条件如下:
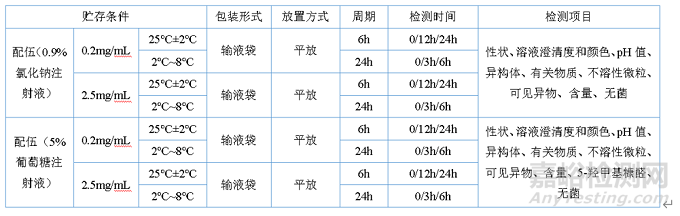
其他需要稀释配伍使用的注射液或者冻干粉剂型的使用中稳定性研究均可按照这样的思路去设计试验方案。
案例二:某口服混悬剂使用中稳定性研究
某口服混悬剂,规格:150ml/瓶 ,其使用说明书内容:
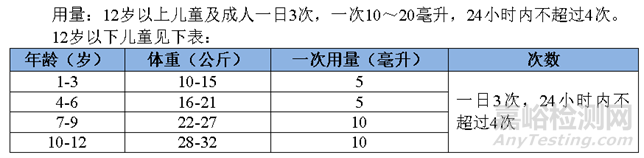
使用中稳定性研究方案和测试过程如下:
初始研究:分析未开瓶样品。
第1周:使用操作:用前摇动瓶子使产品均匀。用量杯或量筒内倒出约5mL该产品。一天操作一次,第1个星期选择任意3天操作。
第2周:分析瓶中剩余样品。
第3周:使用操作:用前摇动瓶子使产品均匀。用量杯或量筒内倒出约5mL该产品。一天操作一次,第3个星期选择任意3天操作。
第4周:分析瓶中剩余样品。

每次倾倒操作之后,样品会被置于稳定箱(25°C/60% RH)。一旦样品被倾倒,将会以立式存放。
综合两瓶研究结果,得出使用中稳定性0、2周、4周、6周、8周的稳定性数据。

来源:Internet


