您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-11-17 12:19
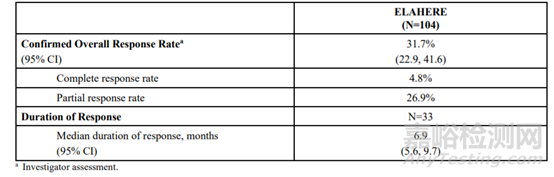
11月14日,FDA加速批准ELAHERE(Mirvetuximab soravtansine-gynx)用于叶酸受体α(FRα)阳性,铂耐药上皮性卵巢癌、输卵管癌或原发性腹膜癌的成年患者,这些患者之前接受过一至三种全身治疗方案。ELAHERE是一种抗体药物偶联物(ADC),FDA说明书显示,在一项有104名铂耐药的卵巢癌患者参与的临床试验中,总缓解率为31.7%,其中完全缓解率为4.8%,部分缓解率为26.9%,中位持续缓解时间是6.9个月,临床终点数据尚未成熟。
ELAHERE的初步疗效数据
这是一款全新的卵巢癌疗法,也是卵巢癌治疗领域的第一款ADC,Mirvetuximab 是一种IgG1,可靶向于叶酸受体α,而小分子部分是一种微管抑制剂,该产品只需三周注射一次。11月15日,华东医药公告显示,该产品为其子公司与ImmunoGen合作研发项目,已经于2021年3月在中国已经获批IND,正处于临床研究阶段,计划在2023年下半年向NMPA递交BLA申请。

来源:药事纵横


